Einleitung
Die Wadenmuskulatur trägt wesentlich zum Vortrieb beim Gehen bei 1. Nach einer Amputation der unteren Extremität können Carbonfederfüße den Wegfall der Wadenmuskulatur zum Teil durch die „Federwirkung“ kompensieren. Diese sogenannten energierückgebenden Füße, in der Literatur häufig als „energy storing and returning (ESAR) prosthetic feet“ bezeichnet, haben eine zwei- bis dreimal höhere Leistungsrückgabe als simple SACH-Füße („solid ankle cushion heel“) 2. Allerdings erreichen auch ESAR-Füße keine physiologische Leistungsrückgabe 3, da es sich dabei um passive Systeme handelt 4. Neben der Leistungsgenerierung in der späten Standphase kontrolliert die Wadenmuskulatur auch die Progression der Tibia beim Überrollen des Unterschenkels über das Sprunggelenk (häufig als „2nd rocker“ bezeichnet 5 6). Durch eine Verformung der Carbonfedern weisen auch ESAR-Füße diese „tibiale“ Progression auf, wenn auch nicht im physiologischen Ausmaß. Silverman et al. berichteten z. B., dass durch das limitierte Bewegungsausmaß eines ESAR-Prothesenfußes der Vortrieb des Körperschwerpunktes reduziert und abgebremst wird 7. De Asha et al. berichteten von einem ähnlichen bremsenden Effekt beim Einsatz eines konventionellen ESAR-Prothesenfußes. Gleichzeitig kam es zu einer Reduktion der zuvor beschriebenen Bremswirkung beim Einsatz eines Prothesenfußes mit einem hydraulischen Knöchelgelenk 8. Die anfangs genannten Aspekte – die Leistungsgenerierung im Sprunggelenk zum Ende der Standphase sowie die Kontrolle der tibialen Progression – sind potenziell konkurrierende Anforderungen an Prothesenfüße. Für die tibiale Progression bzw. Dorsalflexion in der mittleren Standphase wird eine hohe Flexibilität des Prothesenfußes gefordert. Auf der anderen Seite ist für eine hohe Leistungsgenerierung ein adäquates Sprunggelenkmoment und damit in der Regel eine hohe Steifigkeit zum Ende der Standphase notwendig. Diese konkurrierenden Eigenschaften werden auch von Fey et al. und von Adamczyk et al. als Problem bei ESAR-Prothesenfüßen benannt 9 10.
Darüber hinaus wird die erhöhte Leistungsabgabe des prothesenseitigen Sprunggelenkkomplexes mit einer Reduktion der Belastungen auf der erhaltenen Seite in Zusammenhang gebracht. So konnten Morgenroth et al. nachweisen, dass ein experimenteller Prothesenfuß mit einer vermehrten Energierückgabe zu einer Reduktion der vertikalen Bodenreaktionskräfteund des externen Knie-Valgus-Moments während der Belastungsantwort auf die erhaltene Seite führt 11. Ein idealer Prothesenfuß sollte demnach an die Gangphasen angepasste Steifigkeiten und eine hohe Energierückgabe bieten.
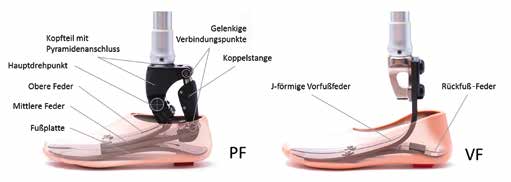
In diesem Zusammenhang scheint der neuartige Prothesenfuß „Pro-Flex“ (Össur hf, Reykjavik, Island; im Folgenden mit „PF“ abgekürzt) vielversprechend zu sein, da er eine serielle Anordnung von flexiblen Carbon-Blattfedern bietet, die über eine Gelenkkette miteinander verbunden sind. Die Position des Hauptdrehpunkts dieser Konstruktion orientiert sich an der Anatomie, weshalb dieser Prothesenfuß potenziell eine adaptive „Knöchelbewegung“ beim Gehen ermöglicht. Die funktionellen Ergebnisse in der Anwendung des PF beim Gehen wurden mit denen des konventionellen ESAR-Prothesenfußes „Vari-Flex“ (Össur hf, Reykjavik, Island; im Folgenden mit „VF“ abgekürzt) verglichen.
Methoden
Studienteilnehmer
Elf Teilnehmer (Details in Tab. 1) mit einer einseitigen transtibialen Amputation (PTTA) und dem Aktivitätsniveau „Mob. 3–4“ konnten in die Studie eingeschlossen werden. Ausschlusskriterien waren Stumpfprobleme wie Ödeme, Druckstellen oder Wunden. Die Daten von elf unversehrten, altersund geschlechtsgepaarten Probanden dienten als Referenz (REF; 2 Frauen und 9 Männer; Alter 37,2 ± 11,4 Jahre; Größe 178,9 ± 8,1 cm; Gewicht 76,4 ± 12,2 kg).
Prothesenfüße
Der zu Vergleichszwecken herangezogene VF-Fuß hat ein klassisches Design mit einer J‑förmigen Vorfußfeder und kann als Urmodell aller ESAR-Füße angesehen werden 12 (Abb. 1, VF rechts). Der neuartige PF-Fuß besteht aus mehreren seriell angeordneten Carbonblattfedern: einer Fußplatte, einer oberen J‑förmigen Feder und einer flachen mittleren Feder, die zwischen der Fußplatte und der oberen Feder angeordnet ist (Abb. 1, PF links). Die obere und die mittlere Feder sind durch eine mechanische Konstruktion über drei Drehpunkte gekoppelt. Dieser Mechanismus ermöglicht eine Rotation des Kopfteils mit dem Pyramidenanschluss um den Hauptdrehpunkt der Konstruktion.
Studiendesign
Die PTTA-Teilnehmer wurden zunächst mit dem VF-Prothesenfuß versorgt. Die Prothesen wurden dazu mit Hilfe des L.A.S.A.R Posture (Otto Bock, Duderstadt, Deutschland) und der Empfehlungen nach Blumentritt und Kollegen aufgebaut 13. Im Anschluss konnten sich die Teilnehmer für zwei Wochen mit der VF-Prothese vertraut machen. Beim untersuchten PF-Fuß handelte es sich zwar um ein Vorserienmodell, laut Hersteller bestehen aber keine Unterschiede gegenüber dem am Markt erhältlichen Prothesenfuß „ProFlex“. Da für PF keine Eingewöhnungsphase vor den Messungen eingeplant war, wurden am Tag der Datenerhebung zunächst alle PTTA-Teilnehmer auf PF umgestellt. Um sich an den PF-Prothesenfuß zu gewöhnen, hatten die Anwender im Anschluss ca. 30 bis 45 Minuten Zeit und liefen dabei ca. 1,5 km in- und außerhalb der Klinik auf wechselnden Untergründen und Hindernissen wie Treppen und Rampen. Danach wurde die Ganganalyse mit dem PF-Fuß durchgeführt. Anschließend wurden die PTTA-Teilnehmer wieder auf den VF-Prothesenfuß umgestellt; der Prothesenaufbau der vorangehenden zweiwöchigen Testphase mit dem VF-Fuß blieb dabei unverändert. Nach einer kurzen Adaptionsphase wurde am selben Tag abschließend die Ganganalyse mit der VF-Prothese durchgeführt.
Der prothetische Aufbau wurde intraindividuell zwischen den Prothesen wie folgt reproduziert: Für die VF-Prothese wurde die vertikale Laserlinie des L.A.S.A.R. Posture auf den Schaft und den Schuh bzw. den Prothesenfuß übertragen. Anschließend wurde der PF untergebaut, um als Erstes die Prothesenhöhe mit dem VF zu reproduzieren. Der PF-Aufbau wurde erneut mit dem L.A.S.A.R Posture vorgenommen; die vertikale Laserlinie wurde auf die zuvor mit dem VF markierten Linien ausgerichtet.
Datenerhebung, ‑aufbereitung und ‑analyse
Die Teilnehmer wurden mit reflektierenden Markerkugeln entsprechend der instrumentellen 3D-Ganganalyse ausgestattet. Durch die Wahl der Reihenfolge der Messungen (zunächst PF, im Anschluss VF) war es möglich, die Markerkugeln an den Teilnehmern zu belassen, da sonst die Gewöhnungsphase für den PF-Fuß nicht möglich gewesen wäre. Die Orientierung der Sprunggelenkmarker (AP = anteriorposterior; H = Höhe vom Boden) wurde zwischen VF und PF reproduziert (Abb. 2). Um die Berechnung von Kinematik und Kinetik der Prothesenfüße zum gleichen Bezugspunkt (Sprunggelenkmarker) sicherzustellen, wurde beim PF-Fuß der Hauptdrehpunkt der Gelenkkonstruktion als Zentrum angenommen (Abb. 2, AP und H); beim VF-Fuß wurde mittels eines eigens angefertigten Adapterblocks der Sprunggelenkmarker per Laserlot auf die gleiche Position wie bei der PF-Versorgung platziert (Abb. 2, VF links).
Für die Ganganalyse gingen die Teilnehmer mit ihrer bevorzugten Gehgeschwindigkeit auf einer 10 m langen Strecke. Ein 12-Kamera-System (Vicon, Oxford, GB) wurde genutzt, um die Markerbewegungen aufzunehmen. Die Bodenreaktionskräfte wurden mittels zweier Kraftmessplatten (Kistler, Winterthur, Schweiz) aufgezeichnet. Es wurde ein konventionelles Modell („Plugin Gait“) zur Berechnung von Kinematik und Kinetik der unteren Extremitäten verwendet 14 15. Um die prothesenseitige Leistungsrückgabe besser abschätzen zu können, wurden darüber hinaus die Ergebnisse zum UD-Modellansatz berechnet („unified deformable segment“ entsprechend Takahashi et al. 16). Die extrahierten Daten (siehe Tab. 2 u. 3) wurden mittels Shapiro-Wilk-Tests auf Normalverteilung getestet. Es lag keine Normalverteilung vor. Aus diesem Grund wurden Unterschiede zwischen den Konditionen und den Gruppen mittels nichtparametrischer statistischer Methoden überprüft (VF gegen PF mittels Wilcoxon-Signed-Rank-Tests für gepaarte Stichproben bzw. REF gegen PF und REF gegen VF mittels Mann-Whitney-U-Tests für ungepaarte Stichproben).
Resultate
Es zeigte sich eine signifikant geringere selbst gewählte Gehgeschwindigkeit für PF (1,33 ± 0.16 m/s) im Vergleich zu VF (1,39 ± 0,17 m/s). Die Teilnehmer der REF-Gruppe liefen im Mittel zwar etwas schneller als die PTTA-Teilnehmer (1,44 ± 0,15 m/s), jedoch war dieser Unterschied nicht signifikant im Vergleich zu beiden Prothesenfußkonditionen (REF vs. PF p = 0.151; REF vs. VF p = 0.401).
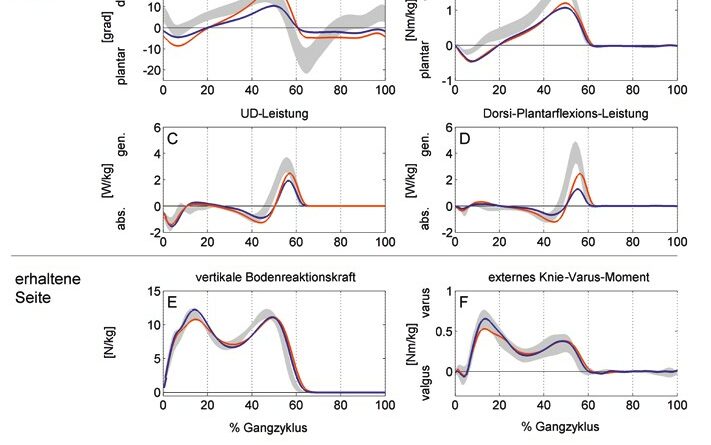
Der PF-Prothesenfuß zeigte im Vergleich zum VF-Fuß ein um 12,5° signifikant größeres Bewegungsausmaß der prothesenseitigen Dorsi-Plantarflexion (Tab. 2; Abb. 3A). Der PF-Fuß wies des Weiteren eine im Vergleich zum VF-Fuß signifikant größere maximale Dorsiflexion zum Ende der Standphase auf, die jedoch im Vergleich zu REF nicht signifikant vergrößert war (Tab. 2; A bb. 3A).
Es zeigte sich bei beiden Prothesenfüßen im Vergleich zur REF-Gruppe ein signifikant reduziertes maximales externes Dorsiflexionsmoment – beim PF-Fuß mit einer Reduktion um 28 %, beim VF-Fuß um 36 %, wobei zwischen den Prothesenfüßen kein Unterschied bestand (Tab. 2; Abb. 3B). Unabhängig vom Modellansatz („Plugin Gait“ und „UD Model“) zeigte sich beim PF-Fuß im Vergleich zum VF-Fuß eine signifikant höhere prothesenseitige Leistung (Tab. 2; Abb. 3C u. D).
Für den PF-Prothesenfuß waren das extern varisierende Kniegelenkmoment und die maximale vertikale Bodenreaktionskraft im Vergleich zum VF-Fuß sowie zur REF-Gruppe signifikant reduziert (Tab. 3; Abb. 3E u. F).
Diskussion
Der PF-Prothesenfuß kombiniert die energierückgebenden Eigenschaften von Carbonfedern mit den Vorteilen einer gelenkigen Konstruktion, die in der Summe ein erhöhtes Bewegungsausmaß bewirken soll. In dieser Studie konnte nachgewiesen werden, dass der PF-Fuß in der Tat ein ähnlich großes Bewegungsausmaß wie die REF-Gruppe aufweist. Obwohl der VF-Fuß bereits ein deutlich vergrößertes Bewegungsausmaß im Vergleich zu einfachen SACH-Füßen zeigt und dies auch in den Zusammenhang mit einer Reduktion der vertikalen Bodenreaktionskräfte auf der erhaltenen Seite gestellt wurde 17 18, ist diese Zunahme an Bewegung möglicherweise immer noch nicht ausreichend. In anderen Studien bevorzugten PTTA-Teilnehmer flexiblere Prothesenfüße gegenüber steiferen Konstruktionen 19 20. Um ein großes Bewegungsausmaß in klassischen ESAR-Prothesenfüßen zu realisieren, müsste bspw. die J‑förmige Carbonfeder des VF-Fußes deutlich flexibler sein. Dies resultiert aber höchstwahrscheinlich in einer Reduktion des effektiven Vorfußhebels, und man erhält einen eher „schwammigen“ Prothesenfuß. Hansen et al. 21 und Fey et al. 22 beschrieben die Herabsetzung des effektiven Vorfußhebels bei weichen Prothesenfüßen, indem sie Füße mit unterschiedlich steifen Vorfußfedern untersuchten. Obwohl ein hohes Bewegungsausmaß zuvor als prinzipiell vorteilhaft beschrieben wurde, kann es durchaus auch negative Effekte haben, insbesondere dann, wenn der effektive Vorfußhebel deutlich reduziert wird. Klodd et al. und Hansen et al. beschreiben eine erhöhte Belastung der erhaltenen Seite bei experimentellen Prothesenfüßen mit einem sehr flexiblen Vorderfuß 23 24. Dementsprechend muss ein Prothesenfuß nicht nur ein großes Bewegungsausmaß aufweisen, sondern auch in der Lage sein, Drehmomente aufzunehmen. Es ist bemerkenswert, dass trotz eines zuvor beschriebenen signifikanten Zuwachses im Bewegungsumfang für den PF-Fuß im Vergleich zum VF-Fuß keine reduzierten Sprunggelenkdrehmomente für den PF-Fuß festgestellt wurden. Einschränkend muss erwähnt werden, dass der Zuwachs im Bewegungsumfang des PF-Prothesenfußes hauptsächlich auf eine vergrößerte Dorsiflexion zurückzuführen ist.
Dies könnte unter Umständen bei Anwendern zur Wahrnehmung eines reduzierten Vorfußhebels führen, was auch einer der PTTA-Betroffenen als negativ beim PF-Fuß während der Untersuchung anmerkte. Positiv wurde weiter für den PF-Fuß nachgewiesen, dass er eine im Vergleich zum VF-Fuß erhöhte Leistungsrückgabe aufweist. Dies wird häufig in den Kontext der Reduktion von Belastungen auf der erhaltenen Seite gebracht, in diesem Fall das maximale externe Knie-Varus-Moment und die maximale vertikale Bodenreaktionskraft. Diese Reduktion wurde für den PF-Fuß ebenfalls nachgewiesen und wird durch die Resultate von Morgenroth et al. unterstützt 25. Insbesondere das externe Knie-Varus-Moment wird in der Literatur immer wieder mit degenerativen Kniegelenkerkrankungen – beispielsweise der Gonarthrose – in Zusammenhang gebracht 26 27.
Abschließend kann mittels dieser Studie keine allgemeingültige Wirkung für den PF-Fuß in Bezug auf eine Reduktion des Arthroserisikos nachgewiesen werden. Dazu müsste eine Patientenkohorte mit unterschiedlichen Prothesenfüßen über eine lange Zeit beobachtet werden. Die Reduktion des externen Knie-Varus-Moments für den PF-Fuß kann trotz allem per se als positiv und entlastend gewertet werden.
Limitierend ist sicherlich die unterschiedlich lange Eingewöhnungsphase für beide Füße (PF: 30–45 Minuten; VF: 2 Wochen). Von einer zweiwöchigen Testphase für den PF wurde abgesehen, da zum Beginn der Studie keinerlei Erfahrungen mit diesem Fuß vorhanden waren. Der Unterschied in der selbst gewählten Gehgeschwindigkeit von 0,06 m/s zwischen PF und VF ist ebenfalls eine Limitation, da insbesondere die Kinetik durch die Gehgeschwindigkeit beeinflusst wird. Bei der erneuten statistischen Testung der Daten mittels einer multivariaten Analyse der Kovarianz (MANCOVA) unter Einschluss der Gehgeschwindigkeit als Störgröße (Kovariate) wurden die signifikanten Unterschiede bestätigt, was die Verfasser darin bestärkt, dass diese Unterschiede auf die unterschiedlichen Eigenschaften der Prothesenfüße und nicht auf die Unterschiede in der Gehgeschwindigkeit zurückzuführen sind.
Schlussfolgerungen
Insgesamt zeigt PF im Vergleich zu VF ein deutlich größeres Bewegungsausmaß bei unverändertem prothesenseitigem Sprunggelenkdrehmoment. Gleichzeitigt zeigt PF eine höhere Leistungsrückgabe im Vergleich zu VF. Dies führt beim PF-Fuß zu einer Reduktion der Lasten auf der erhaltenen Seite. Kritisch ist anzumerken, dass die Zunahme an Bewegung beim PF im Wesentlichen auf eine vergrößerte Dorsiflexion zurückzuführen ist. Für PTTA-Betroffene, die auf einen steiferen Vorfußhebel angewiesen sind, ist PF aus diesem Grund evtl. weniger gut geeignet. Aktuell wird ein Folgeprojekt mit 17 Teilnehmern und unter Einsatz des jetzt auf dem Markt befindlichen Produkts „Pro-Flex“ abgeschlossen. In dieser Studie werden die Eingewöhnungsphasen berücksichtigt, und es werden zusätzlich die biomechanischen Effekte auf Rampen und Treppen untersucht.
Danksagung
Wir danken allen Probanden für ihre Zeit und die Teilnahme an dieser Studie. Des Weiteren danken wir Herrn Dr. Alan R. De Asha (C‑Motion, Inc., Germantown, MD, USA) für die Hilfe bei der Erstellung der englischen Originalarbeit, auf der dieser Artikel basiert 28. Schließlich bedanken wir uns für die finanzielle Unterstützung dieser Studie durch die Firma Össur hf, Reykjavik, Island.
Für die Autoren:
Dipl.-Ing. (FH) Daniel W. W. Heitzmann
Abteilung Bewegungsanalytik
Klinik für Orthopädie und Unfallchirurgie
Universitätsklinikum Heidelberg
Schlierbacher Landstraße 200a
69118 Heidelberg
daniel.heitzmann@med.uni-heidelberg.de
Begutachteter Beitrag/reviewed paper
Heitzmann DWW, Kaib T, Block J, Putz C, Wolf SI, Alimusaj M. Die Vorzüge eines neuartigen Prothesenfußes mit einem hohen Bewegungsausmaß im Vergleich zu einem konventionellen Karbonfederfuß. Orthopädie Technik, 2018; 69 (11): 30–36
| Geschlecht | Größe [cm] | Gewicht [kg] | Alter zum Zeitpunkt der Messung [Jahre] | Zeit seit Amputation [Jahre] | Amputationsursache | Liner / Anschlusstechnik | Gewohnter Prothesenfuß |
|
|---|---|---|---|---|---|---|---|---|
| 1 | ♂ | 187 | 105 | 48 | 11 | Tumor | Synergy Wave1 / pin lock | Vari-Flex1 |
| 2 | ♂ | 183 | 73 | 24,5 | 8 | Tumor | Synergy Wave1 / pin lock | Vari-Flex XC1 |
| 3 | ♂ | 191 | 89 | 55,9 | 32 | Osteomyelitis | Synergy Wave1 / pin lock | Vari-Flex XC1 |
| 4 | ♂ | 178 | 82 | 41,1 | 5 | Trauma | Seal in x 51 / Ausstoßventil / Kniekappe | Echelon2 |
| 5 | ♂ | 176 | 94 | 35,6 | 15 | Trauma | Synergy Wave1 / pin lock | Vari-Flex1 |
| 6 | ♂ | 187 | 94,3 | 43,6 | 2 | Tumor | Synergy Wave1 / pin lock | Flex-Foot Assure1 |
| 7 | ♂ | 183 | 69 | 23,7 | 4 | Tumor | Seal in x 51 / Ausstoßventil / Kniekappe | Reflex Shock1 |
| 8 | ♂ | 168 | 83 | 35,9 | 26 | Trauma | Synergy Wave1/ pin lock | Vari-Flex1 |
| 9 | ♂ | 190 | 95 | 44,2 | 4 | Trauma | Seal in x 51 / Ausstoßventil / Kniekappe | Vari-Flex XC1 |
| 10 | ♀ | 163 | 62,8 | 48,7 | 11 | Morbus Winiwarter-Buerger | Seal in1/ Ausstoßventil / Kniekappe | Vari-Flex1 |
| 11 | ♀ | 172 | 44,9 | 15,8 | -* | Dysmelie | Seal in1/ Ausstoßventil / Kniekappe | Triton3 |
| MW | 179,8 | 81,1 | 37,9 | 11,9 | 5 x Trauma 3 x Tumor 3 x weitere Ursachen | |||
| SD | 9,2 | 17,4 | 12,3 | 10,6 |
* = Die Teilnehmerin hat eine transversale Fehlbildung der unteren Extremität derart, dass diese in Form und Funktion einem Unterschenkelstumpf gleicht.
| REF (n=11) | PTTA (n = 11) | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| REF# gegen PF* | REF# gegen VF* | PF | VF | PF* gegen VF* | |||||
| MW# | SD | p | p | MW* | SD | MW* | SD | p | |
| Maximale Dorsalflexion in der Standphase [Grad] | 13.9 | (± 4.09) | 0.003 | 0.008 | 18.8 | (± 4.11) | 10.6 | (± 1.81) | < 0.001 |
| Bewegungsausmaß der Dorsi-Plantarflexion [Grad] | 31.6 | (± 4.64) | 0.171 | < 0.001 | 27.7 | (± 5.17) | 15.2 | (± 1.86) | 0.003 |
| Maximales externes Dorsiflexionsmoment [Nm/kg] | 1.69 | (± 0.15) | < 0.000 | < 0.001 | 1.22 | (± 0.22) | 1.08 | (± 0.22) | 0.004 |
| Maximale Plantarflexionsleistung [W/kg] | 4.33 | (± 0.62) | 0.001 | < 0.001 | 2.89 | (± 0.90) | 1.48 | (± 0.35) | 0.003 |
| Maximale Leistung (UD) [W/kg] | 3.28 | (± 0.53) | 0.040 | < 0.001 | 2.77 | (± 0.70) | 2.12 | (± 0.49) | 0.006 |
| REF (n=11) | PTTA (n=11) | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| REF# gegen PF* | REF# gegen CF* | NF* | CF* | NF* gegen CF * | |||||
| MW | SD | P | p | MW | SD | MW | SD | p | |
| Maximales externes Knie-Varus-Moment [Nm/kg] | 0.67 | (± 0.09) | 0.088 | 0.699 | 0.57 | (± 0.15) | 0.68 | (± 0.19) | 0.010 |
| Maximale vertikale Boden reaktionskraft [N/kg] | 11.65 | (± 0.73) | 0.065 | 0.151 | 11.03 | (± 1.56) | 12.43 | (± 1.28) | 0.004 |
von REF n = 22; * = Mittelwert aus der betroffenen Seite der PTTA n = 11).
- Entwicklung eines zum physiologischen Gangbild kongruenten polyzentrischen Knieorthesengelenks – Zwischenstand eines Forschungsprojektes — 10. April 2026
- Mikroprozessorgesteuerte stand- und schwungphasenkontrollierte Ganzbeinorthesen (SSCO): Entwicklung, Systeme und Versorgungsrealität in der orthopädietechnischen Praxis — 9. April 2026
- Gips oder Orthese bei distalen Radiusfrakturen? — 8. April 2026
- Winter DA. Energy generation and absorption at the ankle and knee during fast, natural, and slow cadences. Clin Orthop Relat Res, 1983; (175): 147–154
- Czerniecki JM, Gitter A, Munro C. Joint moment and muscle power output characteristics of below knee amputees during running: the influence of energy storing prosthetic feet. Journal of Biomechanics, 1991; 24: 63–75
- Hansen AH, Childress DS, Miff SC, Gard SA, Mesplay KP. The human ankle during walking: implications for design of biomimetic ankle prostheses. Journal of Biomechanics, 2004; 37: 1467–1674
- Herr HM, Grabowski AM. Bionic ankle-foot prosthesis normalizes walking gait for persons with leg amputation. Proceedings Biological Sciences/The Royal Society, 2012; 279: 457–464
- Perry J, Burnfield JM. Gait Analysis: Normal and Pathological Function. Thorofare, NJ: Slack Incorporated, 2010
- Rose J, Gamble JG. Human walking. Philadelphia: Lippincott Williams and Wilkins, 2006
- Silverman AK, Neptune RR. Muscle and prosthesis contributions to amputee walking mechanics: a modeling study. Journal of Biomechanics, 2012; 45: 2271–2278
- De Asha AR, Munjal R, Kulkarni J, Buckley JG. Impact on the biomechanics of overground gait of using an ‘Echelon’ hydraulic ankle-foot device in unilateral trans-tibial and trans-femoral amputees. Clin Biomech (Bristol, Avon), 2014; 29: 728–734
- Fey NP, Klute GK, Neptune RR. The influence of energy storage and return foot stiffness on walking mechanics and muscle activity in below-knee amputees. Clin Biomech (Bristol, Avon), 2011; 26: 1025–1032
- Adamczyk PG, Roland M, Hahn ME. Sensitivity of biomechanical outcomes to independent variations of hindfoot and forefoot stiffness in foot prostheses. Hum Mov Sci, 2017; 54: 154–171
- Morgenroth DC, Segal AD, Zelik KE, Czerniecki JM, Klute GK, Adamczyk PG, et al. The effect of prosthetic foot push-off on mechanical loading associated with knee osteoarthritis in lower extremity amputees. Gait Posture, 2011; 34: 502–507
- Powers CM, Torburn L, Perry J, Ayyappa E. Influence of prosthetic foot design on sound limb loading in adults with unilateral below-knee amputations. Archives of physical medicine and rehabilitation, 1994; 75: 825–829
- Blumentritt S, Schmalz T, Jarasch R. Die Bedeutung des statischen Prothesenaufbaus fur das Stehen und Gehen des Unterschenkelamputierten. Der Orthopäde, 2001; 30: 161–168
- Davis RB, Ounpuu S, Tyburski D, Gage JR. A gait analysis data collection and reduction technique. Human Movement Science, 1991; 10: 575–587
- Kadaba MP, Ramakrishnan HK, Wootten ME, Gainey J, Gorton G, Cochran GV. Repeatability of kinematic, kinetic, and electromyographic data in normal adult gait. J Orthop Res, 1989; 7: 849–860
- Takahashi KZ, Kepple TM, Stanhope SJ. A unified deformable (UD) segment model for quantifying total power of anatomical and prosthetic below-knee structures during stance in gait. Journal of Biomechanics, 2012; 45: 2662–2667
- Powers CM, Torburn L, Perry J, Ayyappa E. Influence of prosthetic foot design on sound limb loading in adults with unilateral below-knee amputations. Archives of physical medicine and rehabilitation, 1994; 75: 825–829
- Snyder RD, Powers CM, Fontaine C, Perry J. The effect of five prosthetic feet on the gait and loading of the sound limb in dysvascular below-knee amputees. Journal of Rehabilitation Research and Development, 1995; 32: 309–315
- Raschke SU, Orendurff MS, Mattie JL, Kenyon DE, Jones OY, Moe D, et al. Biomechanical characteristics, patient preference and activity level with different prosthetic feet: a randomized double blind trial with laboratory and community testing. Journal of Biomechanics, 2015; 48: 146–152
- Klodd E, Hansen A, Fatone S, Edwards M. Effects of prosthetic foot forefoot flexibility on gait of unilateral transtibial prosthesis users. Journal of Rehabilitation Research and Development, 2010; 47: 899–910
- Hansen AH, Meier MR, Sessoms PH, Childress DS. The effects of prosthetic foot roll-over shape arc length on the gait of trans-tibial prosthesis users. Prosthetics and Orthotics International, 2006; 30: 286–299
- Fey NP. The influence of prosthetic foot design and walking speed on belowknee amputee gait mechanics. Dissertation, The University of Texas at Austin, 2011. https://repositories.lib.utexas.edu/handle/2152/ETD-UT-2011–12-4686 (Zugriff am 04.09.2018)
- Klodd E, Hansen A, Fatone S, Edwards M. Effects of prosthetic foot forefoot flexibility on gait of unilateral transtibial prosthesis users. Journal of Rehabilitation Research and Development, 2010; 47: 899–910
- Hansen AH, Childress DS, Knox EH. Prosthetic foot roll-over shapes with implications for alignment of trans-tibial prostheses. Prosthetics and Orthotics International, 2000; 24: 205–215
- Morgenroth DC, Segal AD, Zelik KE, Czerniecki JM, Klute GK, Adamczyk PG, et al. The effect of prosthetic foot push-off on mechanical loading associated with knee osteoarthritis in lower extremity amputees. Gait Posture, 2011; 34: 502–507
- Sharma L, Hurwitz DE, Thonar EJ, Sum JA, Lenz ME, Dunlop DD, et al. Knee adduction moment, serum hyaluronan level, and disease severity in medial tibiofemoral osteoarthritis. Arthritis and Rheumatism, 1998; 41: 1233–1240
- Mundermann A, Dyrby CO, Andriacchi TP. Secondary gait changes in patients with medial compartment knee osteoarthritis: increased load at the ankle, knee, and hip during walking. Arthritis and Rheumatism, 2005; 52: 2835–2844
- Heitzmann DWW, Salami F, De Asha AR, Block J, Putz C, Wolf SI, et al. Benefits of an increased prosthetic ankle range of motion for individuals with a trans-tibial amputation walking with a new prosthetic foot. Gait Posture, 2018; 64: 174–180