Gleichzeitig verlangt das Vorgehen allerdings einen chirurgischen Eingriff, eine strukturierte und aufwendige Rehabilitation sowie spezifische Sonderkenntnisse seitens der Orthopädietechnik. Ebenso geht das Prozedere mit dem Risiko von oberflächlichen oder tiefen Infektionen und von Implantatlockerungen einher. Im schlimmsten Fall können diese zu einer Entfernung des Implantates und zu einer Rückkürzung des Stumpfes führen. Bevor die Entscheidung zur Osseointegration getroffen wird, müssen sich die Patientinnen und Patienten dieser Risiken bewusst sein. Im Allgemeinen wird empfohlen, vorrangig gesunden und jungen Patienten eine Osseointegration anzubieten und gleichzeitig deren Motivation, realistische Erwartungen und Compliance genau zu evaluieren. Osseointegration stellt somit eine sinnvolle Option dar, um bei einer gut ausgewählten Patientengruppe die Prothesenanbindung zu verbessern. Die Anwendung dieser invasiven Technik sollte allerdings aufgrund der Risiken sorgsam in Bezug auf individuelle Präferenzen und Vorstellungen abgewogen werden.
Einleitung
Amputationen oberhalb des Ellenbogens stellen bezüglich ihrer prothetischen Versorgung traditionell eine große Herausforderung dar. Denn im Vergleich zu Amputationen unterhalb des Ellenbogens ist es wesentlich schwieriger, die verlorene Armfunktion zu ersetzen und gleichzeitig eine stabile und komfortable Anbindung der Prothese an den Stumpf zu gewährleisten. Dies führt oft zu Unzufriedenheit der Nutzer und somit zu einer relativ hohen Ablehnungsrate der Versorgungen 1. Dieses Problem eines ggf. unbequemen Schaftes, der die Schulterbeweglichkeit einschränkt, ist insbesondere bei sehr kurzen Oberarmamputationen relevant. Bei ihnen muss oft auf ein Schaftdesign für eine glenohumerale Amputation zurückgegriffen werden. Somit verlieren diese Patienten die Möglichkeit, ihre Schulterbewegung mit der Prothese einzusetzen. Zusätzlich sind bei Schaftversorgungen oft Gurte zur kontralateralen, gesunden Seite notwendig. Dies schränkt Patienten in ihrem Alltag zusätzlich ein, was dazu beiträgt, die Prothese vermehrt als Belastung statt als Hilfestellung wahrzunehmen.
Vorteile, Risiken und daraus abgeleitete Patientenaufklärung
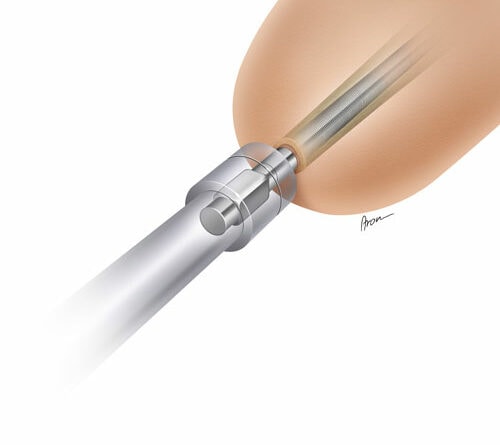
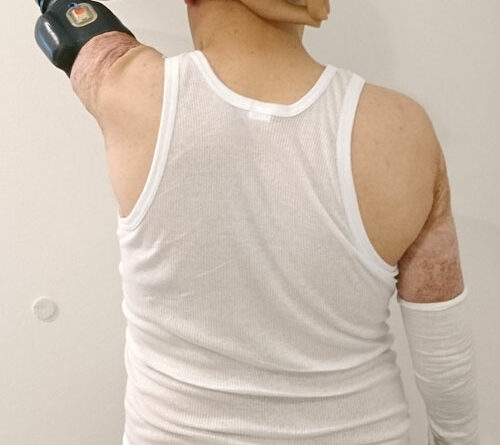
Insbesondere bei kurzen transhumeralen Amputationen bietet die Osseointegration einige Vorteile. Bei dieser invasiven Methode wird chirurgisch ein Implantat in den Oberarmknochen eingebracht, das durch die Haut hindurchtritt und als sogenanntes Abutment einige Zentimeter über das Stumpfende hinausragt (Abb. 1). An diesem Abutment kann eine Prothese fixiert werden, die dadurch über das Implantat direkt mit dem Knochen verbunden ist 2. Eine konventionelle Schaftkonstruktion kann somit prinzipiell entfallen. Durch den Wegfall eines Schaftes und vor allem eventueller Gurte oder Schulterkappen ermöglicht diese direkte Anbindung an das Skelett, dass Bewegungen im Schultergelenk unmittelbar auf die Prothese übertragen werden. Dies macht auch präzise Rotationsbewegungen in der Schulter sowie Bewegungen seitlich vom Körper und im Überkopfbereich mit der Prothese möglich, wie in Abbildung 2 dargestellt wird. Bei konventionellen Versorgungen ist dies meist nur bedingt zu bewerkstelligen.
Dieser Erhalt der Beweglichkeit im Schultergelenk vor allem bei kurzen Oberarmstümpfen ist der größte Vorteil im Vergleich zu konventionellen Schaftversorgungen. Die Länge des verbliebenen Oberarmknochens und die Knochenqualität bestimmen dabei, welches Implantat gewählt werden kann. Aktuelle Studien konnten zudem zeigen, dass Patienten mit einer Osseointegration von positiven Effekten berichten, die über die reine Funktionalität hinausgehen. So wird nach einer Osseointegration über eine gesteigerte Lebensqualität berichtet, und Patienten geben auch an, die Prothese tendenziell als eigenes Körperteil wahrzunehmen 3. Dies deckt sich auch mit den Erfahrungen des Autorenteams. Zudem wird insbesondere bei Osseointegrationen in der unteren Extremität die sogenannte Osseoperzeption – das bessere Wahrnehmen von Bewegungen und Untergrund durch das Implantat – positiv beschrieben 4. Wie relevant dies auch für die obere Extremität ist, ist Gegenstand aktueller Forschung.
Aufgrund all der genannten Vorteile erfreut sich die Osseointegration, die bei der unteren Extremität bereits wesentlich länger Anwendung findet, auch an der oberen Extremität wachsender Beliebtheit. Trotzdem darf nicht außer Acht gelassen werden, dass dieses Vorgehen mit mindestens einem chirurgischen Eingriff verbunden ist und daher auch einige Risiken mit sich bringt. Diese reichen von oberflächlichen bis tiefen Weichteilinfektionen, die bei Beteiligung des Knochens bis hin zu einer Implantatlockerung und in weiterer Folge zu einer Entfernung des Implantates führen können. Oberflächliche Infektionen sind relativ häufig, können aber gut mittels Antibiotikagabe behandelt werden. Tiefe Infektionen, also im Knochen, sind seltener und schwerer zu behandeln. Im schlimmsten Fall kann dadurch auch die Entfernung des Implantates und ggf. eine Rückkürzung des Stumpfes notwendig sein 5.
Angesichts der bislang kleinen Fallzahlen für Osseointegrationen am Oberarmniveau können die tat sächlichen Komplikationsraten jedoch noch schwer abgeschätzt werden. Tsikandylakis et al. haben Komplikationsraten bei transhumeral Amputierten über 5 Jahre nachuntersucht. Insgesamt musste das Implantat demnach bei 20 % der Patientinnen und Patienten wieder entfernt werden; 38 % waren zumindest einmal von einer Infektion betroffen 6. Dazu ist allerdings anzumerken, dass einige der Patienten nach der Explantation wieder mit einem neuen Implantat versorgt wurden und dass Infektionen in der Regel gut behandelt werden konnten. Ebenso kann davon ausgegangen werden, dass Komplikationsraten mit wachsender Erfahrung an internationalen Zentren sinken werden, bedingt durch kontinuierliche Verbesserungen der Implantate, der Operationstechnik und der Rehabilitation 7.
Dennoch zeigen diese relativ hohen Komplikationsraten, dass Patienten, die sich für eine Osseointegration entscheiden, sich dieser Risiken bewusst sein müssen. Dementsprechend ist es unbedingt notwendig, im ärztlichen Aufklärungsgespräch auf diese möglichen Komplikationen, ihr Management und die Verantwortung der Patienten bezüglich der Abutmentreinigung und des rechtzeitigen Meldens von Problemen einzugehen 8. Ebenso müssen die Rehabilitation und ihre Dauer thematisiert werden. Zudem muss, wie nachfolgend beschrieben, gemeinsam mit den Patienten überlegt werden, ob eine Osseointegration wirklich die Behandlung der Wahl ist.
Patientenauswahl
Wie bei jeder medizinischen Intervention muss also auch bei der Osseointegration zwischen potenziellem Nutzen und Risiko abgewogen werden. Da das Nutzen-Risiko-Profil zwischen den Patienten mit Amputation stark variiert, ist eine adäquate Patientenauswahl unbedingt erforderlich. Klassische Indikationen für eine Osseointegration sind die folgenden:
- traumatische Amputationen bei aktiven, jungen Patienten;
- Probleme bei der Nutzung eines gut angepassten konventionellen Schaftes, etwa durch einen sehr kurzen Stumpf;
- sehr aktive Patienten mit hohen Anforderungen und entsprechender Motivation bzw. Compliance 9.
Als Kontraindikationen gelten für einen Großteil der Experten im Feld die folgenden:
- geringe Knochendichte und Durchblutung;
- organisatorische Probleme (Beispiel: Patient lebt weit entfernt vom Behandlungszentrum und hat keine lokalen Ansprechpartner);
- Überschätzung des Nutzens;
- psychische Probleme;
- instabiles soziales Umfeld;
- geringer Eigenantrieb 10.
Genaue Kriterien für den Einschluss werden derzeit in einer internationalen Delphi-Studie unter Leitung der Hauptautorin dieses Artikels erarbeitet.
Unterschiedliche Systeme
Während alle Osseointegrationssysteme sich darin gleichen, dass sie die Prothese mit dem Knochen verbinden, kann zwischen zwei grundsätzlichen Bauarten unterschieden werden:
- jener, bei der das Implantat mit einem Gewinde in den Knochen geschraubt wird, und
- jener, bei der das Implantat mit hoher Druckeinwirkung in den Knochen eingebracht wird (“Pressfit”).
Ein Beispiel für Ersteres ist das sogenannte OPRA-System (Integrum, Schweden). Dieses besteht aus einem relativ kurzen intramedullären Implantat (Länge 6–8 cm) mit einem Gewinde an der Oberfläche. Dieser Teil wird von innen mit der Kortikalis verschraubt, um so die mechanische Stabilität zwischen Implantat und Knochen zu gewährleisten.
Ein am deutschen Markt stark vertretenes Implantat der Pressfit-Technik ist das ILP-System (ESKA Orthodynamics GmbH, Deutschland). Dieses ist deutlich länger und kommt dafür ohne ein Gewinde aus.
Während beide Systeme bereits seit vielen Jahren erfolgreich in der unteren Extremität eingesetzt werden 11, gibt es insbesondere zum ILP-System noch wenige Erfahrungsberichte bei transhumeralen Amputationen.
Operatives Vorgehen
Das operative Vorgehen bei einer Osseointegration hängt grundsätzlich vom Typ des verwendeten Implantats ab. Die Autoren haben diesbezüglich relevante Erfahrungen mit der Anwendung des OPRA-Systems in der oberen Extremität gesammelt, weshalb im weiteren Verlauf auf das operative Vorgehen bei diesem System eingegangen wird.
Zur Operationsplanung ist es sinnvoll, eine Computertomografie des Stumpfes durchzuführen – einerseits, um die Knochenqualität zu beurteilen, andererseits, um die notwendige Implantatgröße festzustellen. Bei gesunden Patienten mit guter Knochenverfassung und langem Stumpf führen die Autoren dieses Artikels mittlerweile die Implantation des OPRA-Systems im Rahmen eines einzeitigen operativen Eingriffs durch. Bei dünneren Knochen oder sehr kurzen Stumpflängen ist dagegen zu empfehlen, in einer ersten Operation nur das intramedulläre Implantat einzubringen. Im Rahmen dessen kann zudem, falls notwendig, eine chirurgische Verlängerung des Knochens vorgenommen werden. Dazu wird Knochenmaterial aus dem Beckenkamm des Patienten entnommen und am Stumpfende eingebracht. Nach einer Einheilungsphase von etwa drei Monaten wird dann in einem zweiten Eingriff der Hautdurchtritt geschaffen und das externe Abutment mit dem intramedullären Implantat verbunden. Diesem Schritt der Osseointegration kommt größte Bedeutung zu, da der Operateur hier maßgeblich zum Erfolg oder auch Misserfolg der späteren Versorgung beitragen kann.
Um Sekretionen am Port sowie das damit einhergehende Infektionsrisiko möglichst gering zu halten, muss der Weichteilmantel um den Hautdurchtritt der Prothese weitgehend reduziert werden. Im Gegensatz zu den Prinzipien der klassischen Stumpfchirurgie sollte die Haut um den Port idealerweise direkt am Knochen anliegen, um mit diesem verwachsen zu können. Subkutanes Fett muss entsprechend entfernt werden, und die Muskeln müssen um den Knochen fixiert werden. Ziel ist es, dass so wenig Relativbewegung wie möglich zwischen Haut und Prothese stattfindet. Dies ermöglicht eine stabile Verbindung zwischen Haut und Prothese und hält die Eintrittspforte für Keime somit gering. Postoperativ soll ein straffer Verband angelegt werden, um einer Schwellung des Stumpfes vorzubeugen. Zur Infektionsprophylaxe werden orale Antibiotika nach der Operation gegeben, in der Regel bis zur Nahtentfernung.
Rehabilitation bei einer Osseointegration
Rehabilitationsmaßnahmen sollten bereits vor der Operation beginnen und auf eine Kräftigung und Vergrößerung der Beweglichkeit im Schulterbereich abzielen, um später die optimale Nutzung der Prothese zu ermöglichen. Die postoperative Therapie muss unbedingt in enger Kooperation mit dem chirurgischen und orthopädietechnischen Team stattfinden und sich an den Empfehlungen des jeweiligen Implantatherstellers orientieren. Neben einem Weiterführen des Programmes für den Erhalt bzw. die Verbesserung von Kraft und Beweglichkeit steht die kontinuierliche Belastungssteigerung im Fokus. Bei der Verwendung des OPRA-Systems wird empfohlen, mit Hilfe einer speziellen Trainingsprothese drei Wochen nach der zweiten Operation mit dem Belastungstraining zu beginnen und dieses kontinuierlich zu steigern. Dabei werden wöchentlich 50 bis 100 g zum Belastungsgewicht hinzugefügt. Ebenso werden Patienten instruiert, das Implantat mit steigender Belastung axial gegen eine Waage zu drücken. Zumeist wird mit einer Belastung von 5 kg begonnen, die täglich zehnmal für zehn Sekunden auf die Waage gebracht wird. Ziel der kontinuierlichen Belastungssteigerung ist es, ein schrittweises Einwachsen des Knochens an die Implantatoberfläche zu ermöglichen. Der wichtigste Indikator für das Ausmaß der Belastung ist dabei der Schmerz, wobei eine Angabe von 5 oder mehr auf der Visuellen Analogskala (VAS) als Überlastung interpretiert wird und somit nicht provoziert werden sollte, da dies im schlimmsten Fall zu einer Lockerung des Implantats führen kann 12. Im Laufe der Rehabilitation wird dann die Belastung so lange erhöht, bis das Gewicht der Prothese inklusive gegriffener Gegenstände gut toleriert wird. Zudem wird der Patient bereits präoperativ bezüglich der notwendigen Hygiene beim Hautdurchtritt aufgeklärt, was auch während der Rehabilitation regelmäßig thematisiert wird. Je nach Beschaffenheit des Weichteilmantels wird es zu mehr oder weniger Sekretionen kommen. Sind diese ausgeprägt, ist es sinnvoll, z. B. ein Taschentuch um das Abutment zu binden. Außerdem sollten die Patientinnen und Patienten den Hautdurchtritt zumindest zweimal täglich reinigen, etwa mit Desinfektionsmittel (schleimhautverträglich) oder gängiger Kochsalzlösung.
Nach der Prothesenanpassung wird im Zuge der Therapie außerdem die Ansteuerung der Prothese trainiert. Im Wesentlichen unterscheidet sich das Prothesentraining nach einer Osseointegration im Vergleich zur konventionellen Prothesenversorgung nur darin, dass dem ergonomischen Ausnützen des gewonnenen Bewegungsausmaßes mehr Beachtung geschenkt wird. Abgesehen davon wird – wie bei konventionellen Versorgungen auch – mit dem Üben isolierter Prothesenbewegungen begonnen, später Objekte gegriffen und positioniert, und schließlich werden alltagsrelevante Bewegungsabläufe und Tätigkeiten trainiert. Bei myoelektrischen Prothesen kann außerdem ein Signaltraining mittels EMG-Biofeedbacks sinnvoll sein.
Orthopädietechnische Überlegungen
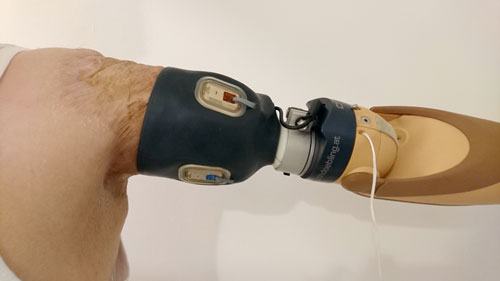
Generell können sowohl mechanische, kosmetische als auch myoelektrische Versorgungen mit einer Osseointegration kombiniert werden. Die Wahl der prothetischen Versorgung nach transhumeraler Osseointegration richtet sich daher nach den Bedürfnissen und Anforderungen der jeweiligen Patienten. Wie bereits eingangs erwähnt, muss, da die Prothese nun am Abutment fixiert werden kann, kein Schaft angepasst werden. Allerdings müssen geeignete Verbindungsteile ausgewählt und ggf. eingestellt werden. Zumeist ist dafür eine Zertifizierung über den Implantathersteller notwendig. Im Falle myoelektrischer Versorgungen ist es außerdem notwendig, die Oberflächenelektroden am Stumpf zu fixieren. Die Elektroden können dafür in einen kurzen Silikonschaft verbaut werden, der eine Öffnung für das Abutment aufweist, an dem dann die Prothese befestigt wird (Abb. 3). Alternativ können Klebeelektroden verwendet werden. Diese müssen dann von den Patienten nach jedem Anziehen der Prothese neu aufgeklebt werden. Sie erfordern dabei eine präzise Markierung der passenden Stellen, um stabile Signale zu gewährleisten.
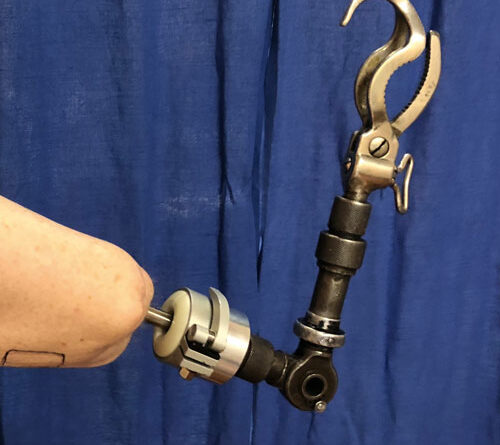
Nach der Erfahrung der Autoren nutzen Patienten nach erfolgreicher Operation und Rehabilitation ihre Prothese vermehrt im täglichen Leben, gegebenenfalls auch für handwerkliche oder landwirtschaftliche Tätigkeiten. Durch die häufige und intensive Verwendung kommt es in der Regel zu einem höheren Verschleiß der verschiedenen Komponenten. Wo es möglich ist, sollte also vorgesehen werden, eine robuste Zweitversorgung zur Verfügung zu stellen. So kann eine myoelektrische Versorgung für den Alltag in Kombination mit einer robusten mechanischen Versorgung für größeren Krafteinsatz und Outdoor-Nutzung ebenso wie unterschiedliche Endgeräte und Adapter sinnvoll sein. Ein Beispiel einer robusten mechanischen Versorgung für landwirtschaftliche Arbeit zeigt Abbildung 4. Einige Patienten wünschen sich zudem eine einfache Schlafprothese, die einen Schutz vor dem harten Abutment und auch ein entsprechendes Gewicht bietet, was viele Patienten als angenehm empfinden.
Zulassung armprothetischer Passteile
Aktuell ist kein Ellbogenpassteil auf dem Markt für Versorgungen nach einer Osseointegration zugelassen. Alle Einzelteile (Implantat, Adapter, Prothesenpassteile) sind zwar individuell CE-zertifiziert, jedoch fehlt eine gemeinsame Bewertung, wie sie für die untere Extremität bereits vorhanden ist. Seitens der Prothesen- und Implantathersteller wird aber generell eine solche Lösung angestrebt: eine Zulassung des Komplettsystems vom Implantat über den Adapter bis hin zum Ellenbogenpassteil. Dafür bedarf es einer engen Zusammenarbeit zwischen allen Herstellern sowie einer Durchführung gemeinsamer Tests und Bewertungen unter Beachtung aller regulatorischer Vorgaben. Daher können die Autoren auch nicht abschätzen, wie lange der Prozess einer Gesamtbewertung dauern wird.
Kombination mit TMR
Zur Verbesserung der Steuerung myoelektrischer Prothesen haben sich in den vergangenen Jahren selektive Nerventransfers (auch bekannt als “targeted muscle reinnervation”, TMR) etabliert. TMR hat dabei einen positiven Einfluss auf Phantomschmerzen, kann die Anzahl an gleichzeitig durchführbaren Prothesenbewegungen erhöhen und ermöglicht insgesamt eine intuitivere Kontrolle 13 14. Allerdings konnte das Autorenteam erst unlängst zeigen, dass diese Methode alleine die Ablehnungsrate nur bedingt positiv beeinflusst 15. Dies ist unter anderem dadurch begründet, dass Nerventransfers die Problematik eines ggf. unbequemen Schaftes, der die Schulterbeweglichkeit einschränkt, nicht lösen. Wird nun TMR mit Osseointegration kombiniert, kann eine intuitivere Steuerung gemeinsam mit einer angenehmen und funktionellen Anbindung der Prothese erreicht werden 16. Eine erste Fallserie von fünf Personen mit transhumeraler Amputation, die im Zentrum der Autoren sowohl TMR als auch Osseointegration erhalten haben, zeigt hierbei vielversprechende Ergebnisse, die darauf hindeuten, dass Prothesensteuerung und ‑anbindung als wesentlich natürlicher und angenehmer empfunden werden.
Operativ können dabei die Nerventransfers von entsprechend geschulten Chirurginnen und Chirurgen im Zuge der Implantation durchgeführt werden. Die anschließende Rehabilitation deckt dann sowohl die oben beschriebenen Interventionen zur Kraft‑, Beweglichkeits- und Belastungssteigerung als auch ein TMR-spezifisches Training der neu geschaffenen Myosignale ab. Besonders wichtig ist dabei das strukturierte Signaltraining mittels EMG-Biofeedback 17. Da sowohl Osseointegration als auch TMR operativ und rehabilitativ eine große Komplexität aufweisen, empfehlen die Autoren neuen Zentren, zuerst getrennt Erfahrung mit beiden Techniken zu sammeln, ehe diese gemeinsam angewendet werden. Das Autorenteam hatte bereits über 30 TMR-Operationen durchgeführt und rehabilitativ begleitet, ehe diese Technik mit der Osseointegration kombiniert wurde.
Im Rahmen der orthopädietechnischen Versorgung muss sichergestellt werden, dass alle der bis zu sechs Oberflächenelektroden präzise in einem Schaft platziert werden. Während Klebeelektroden prinzipiell ebenfalls genutzt werden können, wird eine korrekte Anbringung mit steigender Signalanzahl immer herausfordernder. Deshalb hat sich bei den Patienten der Autoren eine Versorgung mit einem kleinen Silikonschaft besser bewährt. Auch hier wird empfohlen, die Versorgung von Orthopädietechnikerinnen und ‑technikern mit Vorerfahrung durchführen zu lassen.
Fazit und Ausblick
Wenn gleich Osseointegration für transhumeral Amputierte eine relativ neue Option darstellt, erfreut sie sich aufgrund der eindeutigen Vorteile für die Patienten großer Beliebtheit. Aufgrund der noch limitierten Erfahrung und des Risikoprofils sowie der relativ aufwendigen Rehabilitation ist es jedenfalls zu empfehlen, die Indikationsstellung vorsichtig zu wählen. Die Patienten müssen entsprechende gesundheitliche Anforderungen erfüllen und sollten kooperativ sein und ausreichende Motivation mitbringen, um sowohl eine komplikationsarme Rehabilitation zu ermöglichen als auch die notwendigen Maßnahmen wie etwa regelmäßige Hygiene einzuhalten. Sofern dies gewünscht und sinnvoll ist, kann gleichzeitig auch eine kombinierte Behandlung mit selektiven Nerventransfers (TMR) erfolgen. Somit kann nicht nur die mechanische Schnittstelle zur Prothese verbessert werden, sondern auch die Prothesensteuerung einfacher und intuitiver gestaltet werden.
Für derzeitige Prothesensteuerungen mit Oberflächenelektroden kann allerdings auf eine Art Schaft noch nicht verzichtet werden, um die Elektroden am Stumpf zu fixieren. Zukünftig könnten hier implantierte Elektroden Abhilfe schaffen. Zwar werden einige Systeme bereits in der Forschung getestet, es ist aber nicht damit zu rechnen, dass sie in naher Zukunft in den klinischen Alltag Einzug halten werden 18.
Danksagung
Die Autorin und die Autoren bedanken sich bei Aron Cserveny für den Entwurf von Abbildung 1.
Für die Autoren:
Dr. scient. med. Agnes Sturma, MSc
Klinisches Labor für Bionische Extremitätenrekonstruktion
Medizinische Universität Wien
Währinger Gürtel 18–20
A‑1090 Wien, Österreich
agnes.sturma@meduniwien.ac.at
Begutachteter Beitrag/reviewed paper
Sturma A, Gstöttner C, Salminger St, Aszmann OC. Osseointegration bei transhumeraler Amputation: Vorteile, Herausforderungen und Limitationen. Orthopädie Technik, 2020; 71(8): 46–51
- Vergleichende Prüfung konventioneller und additiv gefertigter Prothesenschäfte in Anlehnung an DIN EN ISO 10328:2016 — 10. März 2026
- Easypreg – ein Faserverbundwerkstoff zum Tiefziehen — 9. März 2026
- Konservative Versorgung einer adulten Skoliose mit einem modularen Bausatz – ein Versorgungsbeispiel — 6. März 2026
- Biddiss E, Chau T. Upper-limb prosthetics: critical factors in device abandonment. Am J Phys Med Rehabil, 2007; 86 (12): 977–987
- Jonsson S, Caine-Winterberger K, Branemark R. Osseointegration amputation prostheses on the upper limbs: methods, prosthetics and rehabilitation. Prosthet Orthot Int, 2011; 35 (2): 190–200
- Lundberg M, Hagberg K, Bullington J. My prosthesis as a part of me: a qualitative analysis of living with an osseointegrated prosthetic limb. Prosthet Orthot Int, 2011; 35 (2): 207–214
- Hoffmeister T, Schwarze F, Aschoff HH [The endo-exo prosthesis treatment concept: Improvement in quality of life after limb amputation]. Unfallchirurg, 2017; 120 (5): 371–377
- Tillander J et al. Osseointegrated titanium implants for limb prostheses attachments: infectious complications. Clin Orthop Relat Res, 2010; 468 (10): 2781–2788
- Tsikandylakis G, Berlin O, Branemark R. Implant survival, adverse events, and bone remodeling of osseointegrated percutaneous implants for transhumeral amputees. Clin Orthop Relat Res, 2014; 472 (10): 2947–2956
- Tsikandylakis G, Berlin O, Branemark R. Implant survival, adverse events, and bone remodeling of osseointegrated percutaneous implants for transhumeral amputees. Clin Orthop Relat Res, 2014; 472 (10): 2947–2956
- Aschoff HH. [Transcutaneous osseointegration after limb amputation: A review over 27 years]. Unfallchirurg, 2017; 120 (4): 278–284
- Tsikandylakis G, Berlin O, Branemark R. Implant survival, adverse events, and bone remodeling of osseointegrated percutaneous implants for transhumeral amputees. Clin Orthop Relat Res, 2014; 472 (10): 2947–2956
- Aschoff HH. [Transcutaneous osseointegration after limb amputation: A review over 27 years]. Unfallchirurg, 2017; 120 (4): 278–284
- Aschoff HH. [Transcutaneous osseointegration after limb amputation: A review over 27 years]. Unfallchirurg, 2017; 120 (4): 278–284
- Li Y, Branemark R. Osseointegrated prostheses for rehabilitation following amputation: The pioneering Swedish model. Unfallchirurg, 2017; 120 (4): 285–292
- Dumanian GA et al. Targeted Muscle Reinnervation Treats Neuroma and Phantom Pain in Major Limb Amputees: A Randomized Clinical Trial. Ann Surg, 2019; 270 (2): 238–246
- Aszmann OC, Dietl H, Frey M. Selective nerve transfers to improve the control of myoelectrical arm prostheses. Handchirurgie, Mikrochirurgie, plastische Chirurgie, 2008; 40 (1): 60–65
- Salminger S et al. Outcomes, challenges and pitfalls after targeted muscle reinnervation in high level amputees. Is it worth the effort? Plast Reconstr Surg, 2019; 144 (6): 1037e– 1043e
- Myers H et al. Targeted muscle reinnervation to improve electromyography signals for advanced myoelectric prosthetic limbs: a series of seven patients. ANZ J Surg, 2020; 90 (4): 591– 596
- Sturma A, Salminger S, Aszmann O. Proximale Amputationen des Armes: Technische, chirurgische und handtherapeutische Möglichkeiten. Zeitschrift für Handtherapie, 2018; 21 (1): 18–25
- Ortiz-Catalan M, Hakansson B, Branemark R. An osseointegrated human-machine gateway for long-term sensory feedback and motor control of artificial limbs. Sci Transl Med, 2014; 6 (257): 257re6