Eine systematische Literatursuche identifizierte sieben zusätzliche Studien, deren methodische Qualität nach den Kriterien eines Cochrane-Reviews zu Prothesenpassteilen als „mittel“ einzustufen ist. Diese Studien beschreiben insgesamt 2.249 Patienten, davon 677 in der Aktivitätsklasse 2 sowie 432 mit vaskulär bedingter Oberschenkelamputation. Aus dem nun qualitativ und quantitativ deutlich verbesserten Stand der wissenschaftlichen Literatur lässt sich das Potenzial insbesondere von MPK mit Linearhydraulik ableiten, auch oder gerade bei besonders vulnerablen Patientengruppen zur Verbesserung von Sicherheit, Mobilität und Lebensqualität beizutragen. Darüber hinaus lässt sich die Kosteneffizienz dieser Systeme auch in dieser Patientengruppe belegen. Die Ergebnisse dieser systematischen Literaturanalyse legen nahe, die prothetische Versorgung eingeschränkter Außenbereichsgeher mit MPK heute als Standard zu betrachten.
Einleitung
Das Fehlen oder die Amputation einer unteren Extremität kann die lebensverändernde Folge von angeborenen Deformitäten, Traumata, Krebserkrankungen, peripherer arterieller Verschlusskrankheit (pAVK), diabetischer Neuropathie und anderen Erkrankungen sein. Bei oberschenkelamputierten Patienten stellt das Prothesenkniegelenk ein äußerst wichtiges Passteil dar, das sowohl die funktionelle Biomechanik des Knieswiederherstellen als auch größtmögliche Stabilität und Sicherheit der Prothese gewährleisten muss 1. In den letzten 25 Jahren hat sich die Technologie von Prothesenkniegelenken durch den Einsatz von Mikroprozessoren in der Stand- und/ oder Schwungphasensteuerung erheblich weiterentwickelt. Sie konnte dadurch den für herkömmliche Prothesenkniegelenke geltenden Gegensatz zwischen Sicherheit und Funktionsunterstützung – „je sicherer, desto weniger funktionell; je funktioneller, desto unsicherer“ – überwinden. Die überwiegende Anzahl klinischer Studien wurde mit uneingeschränkten Außenbereichsgehern (Aktivitätsklasse [AK] 3 bzw. dem US-Äquivalent Medicare Functional Classification Level [MFCL-] 3) durchgeführt. Sie belegen die größere Sicherheit bei gleichzeitig verbesserter Funktionalität von per Mikroprozessor gesteuerten Prothesenkniegelenken (MPKs) 2 3 4 beim Gehen auf ebenen 5 6 7 8 9 und unebenen Untergründen 10 1112 13, Schrägen 14 15 16 17 18, Treppen 19 20 21 22 23 und bei der Bewältigung kritischer Alltagssituationen. 24 25. Eine ganze Reihe von Studien hat dabei eine signifikante Verringerung von Stürzen und ein verbessertes Gleichgewicht gegenüber dem Gebrauch von nicht per Mikroprozessor gesteuerten Kniegelenken (NMPKs) 26 27 28 29 30 31 32 nachgewiesen. In der Zwischenzeit gilt auch die Kosteneffizienz von MPK in dieser Anwendergruppe als belegt 33 34. Bei der Versorgung mit modernen Prothesensystemen werden häufig jüngere, gesündere und aktivere Patienten bevorzugt. Damit hat die Beinprothetik einen von anderen Bereichen der Gesundheitsversorgung abweichenden Weg eingeschlagen – normalerweise wird die modernste Medizintechnik bei den ältesten und kränksten Patienten mit den größten gesundheitlichen Beeinträchtigungen eingesetzt. Dies erklärt auch, warum 80 % der lebenslangen Gesundheitsausgaben auf die zweite Lebenshälfte entfallen 35, wobei ein Großteil davon erst im letzten Jahr vor dem Tod entsteht 36 37. Heute ist der Großteil der oberschenkelamputierten Patienten älter als 65 Jahre 38 und erreicht nicht den Mobilitätsgrad eines uneingeschränkten Außenbereichsgehers 39. Dazu trägt möglicherweise auch bei, dass in der Regel Prothesenkniegelenke eingesetzt werden, die in ihrer Funktionalität deutlich eingeschränkt sind und häufig bereits vor Jahrzehnten entwickelt wurden.
Dies wirft die Frage auf, ob auch eingeschränkte Außenbereichsgeher (AK 2 bzw. US-Äquivalent MFCL- 2) einen ähnlich großen Nutzen aus dem Gebrauch von MPKs ziehen können wie uneingeschränkte Außenbereichsgeher (AK/MFCL‑3). Kannenberg et al.40 41 ermittelten in ihrer systematischen Analyse klinischer Studien zum Vergleich des Nutzens von NMPKs und MPKs bei eingeschränkten Außenbereichsgehern (AK/MFCL‑2) eine signifikante Verringerung der Stürze um bis zu 80 % und eine signifikante Verbesserung von Indikatoren für das Sturzrisiko bei Verwendung eines MPK. Die leistungsbasierten Testparameter zeigten, dass ein MPK die Patienten der Aktivitätsklasse 2 befähigen kann, in der Ebene ca. 14 bis 25 %, auf unebenem Untergrund etwa 20 % und beim Hinabgehen von Rampen bis zu 30 % schneller zu gehen. Darüber hinaus konnten die Patienten auch Aktivitäten besser bewältigen, die eigentlich typisch für die Aktivitätsklasse 3 sind. Ein interessantes Ergebnis der Analyse war allerdings auch, dass sich die klinisch relevanten objektiven Verbesserungen bezüglich Sicherheit, Funktionalität und Mobilität subjektiv im Wesentlichen nur in einer deutlichen Präferenz von 90 % für das MPK widerspiegelten. Die Ergebnisse validierter Messinstrumente zur subjektiv wahrgenommenen Sicherheit und Funktionalität der Prothese waren dagegen weniger überzeugend. Der Zweck der vorliegenden Aktualisierung der Literaturanalyse besteht darin, folgende Fragen zu klären:
- Sind in den letzten 5 Jahren neue, möglicherweise größere Studien mit MPK bei eingeschränkten Außenbereichsgehern veröffentlicht worden, die die Ergebnisse der Literaturanalyse von 2014/2015 4243untermauern oder widerlegen?
- Haben neuere Studien möglicherweise weitere Nutzenaspekte von MPK bei eingeschränkten Außenbereichsgehern untersucht, die in der Literaturanalyse von 2014/2015 noch nicht ermittelt wurden?
- Gibt es Studien zur gesundheitsökonomischen Bewertung von MPK bei eingeschränkten Außenbereichsgehern?
Methodik
Suchstrategie
Die systematische Literatursuche erfolgte am 13. Januar 2020 in den wissenschaftlichen Literaturdatenbanken Medline und Cochrane Library sowie in Google Scholar. Für die Datenbankrecherche wurden Suchbegriffe mit Bezug zu MPK und einseitig oberschenkelamputierten Personen der Aktivitätsklasse 2 bzw. des Mobilitätsgrads MFCL‑2 sowie eine Erweiterung auf vaskuläre Ätiologien verwendet. Der Datenbank-Suchlogik folgend wurden in DARE, Cirrie (jetzt NARIC Rehab Database), PEDRO und OT Seeker punktuelle ergänzende Suchen durchgeführt. Die Literatursuche beschränkte sich auf englischund deutschsprachige Publikationen im Zeitraum von 2014 bis 2020. Zusätzlich wurden die Literaturverzeichnisse der analysierten Artikel auf weitere möglicherweise relevante Publikationen durchsucht. Auswahlverfahren Zunächst wurden die Titel und Kurzzusammenfassungen (Abstracts) der ermittelten Publikationen von beiden
Autoren unabhängig voneinander auf das Vorliegen von Ein- und Ausschlusskriterien gesichtet und als (I) relevant, (II) nicht relevant oder (III) eventuell relevant bewertet.
Einschlusskriterien
Folgende Kriterien mussten zum Einschluss in die Analyse erfüllt sein: 1. Es musste sich um eine randomisierte oder nichtrandomisierte Vergleichsstudie handeln, die die Versorgung und die Ergebnisse oder die gesundheitsökonomischen Aspekte eines oder mehrerer MPK mit denen eines oder mehrerer NMPK vergleicht oder – im Falle gesundheitsökonomischer Studien – modelliert. 2. Die Studie musste über Ergebnisse von Patienten mit einseitiger Oberschenkelamputation oder Knieexartikulation und dem Mobilitätsgrad 2 (bzw. MFCL‑2) und/oder der Ätiologie „vaskuläre Erkrankung“ berichten. Die eingeschränkten Außenbereichsgeher mussten dabei entweder die Studienzielgruppe darstellen, oder die Studie musste deren Ergebnisse als eigenständige
Untergruppenanalyse oder als Rohdaten präsentieren, die eine nachträgliche (Post-hoc) statistische Auswertung zuließen. 3. Die Studie verwendete und berichtete über quantitativ unabhängig nachvollziehbare Ergebnisse validierter klinischer Testverfahren und validierter Fragebögen aus den Bereichen Sicherheit, Funktionalität und Mobilität sowie über wahrgenommene Funktionalität und Zufriedenheit mit der Prothese.
Ausschlusskriterien
Folgende Kriterien führten zum Ausschluss aus der Analyse:
- Studien mit implantierbaren Kniegelenken (totale Kniearthroplastik/ totaler Knieersatz);
- Studien mit beidseitig amputierten Patienten oder mit Patienten mit einem höheren bzw. niedrigeren Amputationsniveau als transfemoral bzw. Knieexartikulation;
- Studien, die nur Meinungen oder qualitative Bewertungen der Autoren, aber keine konkreten quantitativen Daten für eine unabhängige Bewertung beinhalteten;
- Studien, die bereits in Kannenberg et al. 2014/2015 berücksichtigt wurden;
- Duplikate.
Beurteilung der methodischen Qualität
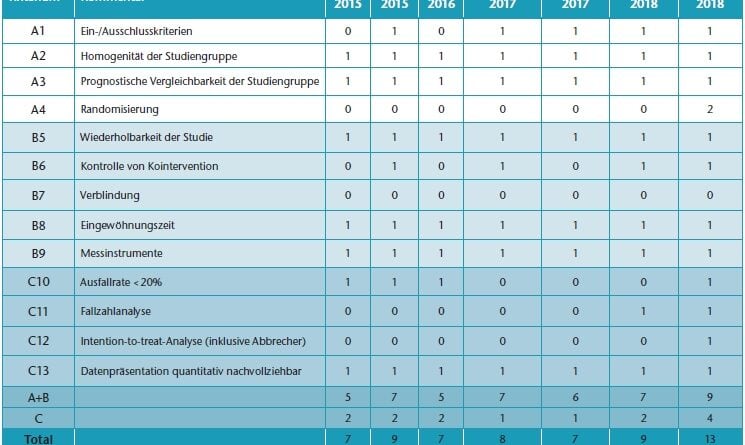
Nach der Sichtung der Publikationen in Bezug auf ihre Relevanz für diese Analyse wurden die methodische Qualität und das Risiko einer Verzerrung der Ergebnisse (Bias) separat von beiden Autoren mittels der von Hofstad et al. 44 veröffentlichten Checkliste eines systematischenCochrane-Reviews über rothetische Knöchel-Fuß-Mechanismen beurteilt. Die Checkliste von Hofstad et al. umfasst 13 methodische Qualitätskriterien, die sich auf die Patientenauswahl, die Qualität und die Wiederholbarkeit des Studiendesigns sowie auf die statistische Validität der Daten beziehen. Die identifizierte gesundheitsökonomische Studie (siehe unten) wird ohne eigene Methodenbewertung diskutiert.
Ergebnisse Literatursuche
Mittels Literaturrecherche in den Datenbanken wurden 3.220 Artikelhinweise ermittelt. Nach Ausschluss von Mehrfachtreffern und Prüfung auf Relevanz wurden 31 Artikel einer Volltextsichtung unterzogen. Sieben Artikel genügten den Einschlusskriterien. Eine weitere Publikation beschreibt ein gesundheitsökonomisches Modell zur Bewertung der Kos-teneffizienz und des Einflusses auf das Budget aus Sicht der Kostenträger in Deutschland. Im Folgenden werden die identifizierten Arbeiten kurz charakterisiert:
1. Lansade et al. 45 beschreiben eine randomisierte Cross-over- Studie in der relevanten Zielgruppe oberschenkelamputierter Probanden mit niedriger Mobilität mit einem „Kenevo“-Knie unter Verwendung validierter funktionaler und patientenbasierter Messinstrumente.
2. Kaufman et al. 46 berichten über eine prospektive Cross-over-Studie, die mit vier unterschiedlichen MPKs („C‑Leg Compact“, „Rheo Knee 3“, „Plie 3“, „Orion 2“) durchgeführt wurde. Zwischen den unterschiedlichen MPKs wurde nicht unterschieden. Neben validierten Instrumenten wurden hier auch Aktivitätssensoren eingesetzt.
3. Wong et al. 47 untersuchen den Einfluss des „C‑Leg“ auf Probanden mit vaskulärer Ätiologie in einer prospektiven Kohortenstudie unter Verwendung standardisierter klinischer Messinstrumente.
4. Mileusnic et al. 48 beschreiben in einer prospektiven Kohortenstudie den ersten Versorgungseinsatz von „Kenevo“ bei eingeschränkten Außenbereichsgehern. Zusätzlich zu validierten Instrumenten werden hier spezifisch angepasste, vergleichende Likert-Skalen eingesetzt.
5. Hasenöhrl et al. 49beschreiben im Rahmen einer Pilotstudie ein prospektives A‑B-A-Design zur Prüfung eines auf dem „Genium“ basierenden MPK-Prototyps bei eingeschränkten Außenbereichsgehern und setzen neben klinisch standardisierten Instrumenten auch eine instrumentierte Ganganalyse ein.
6. Hahn et al. 50 51 52 beschreiben in zwei unabhängigen retrospektiven Analysen Ergebnisse aus über 1.223 bzw. 899 Testversorgungen mit „C‑Leg“/„C‑Leg Compact“ bzw. „Genium“. Dazu wurden, den Empfehlungen der ehemaligen Klinischen Prüfstelle Münster 53 54 folgend, vergleichende Likert-Skalen eingesetzt. Der Einfluss auf die Untergruppen „niedrige® Aktivitätsklasse/ Mobilitätsgrad“ und „vaskuläre Ätiologie“ wurde mittels Regressionsanalysen bewertet.
7. Kuhlmann et al. 55 entwerfen ein entscheidungsanalytisches Modell (Markov State Transition Model) zur Kosteneffektivitäts- und Budgetauswirkungsanalyse aus Sicht der Kostenträger. Den Annahmen des Modells bezüglich Sturzhäufigkeit mit NMPK und Sturzvermeidung durch MPK liegen Ergebnisse der in dieser Arbeit zitierten Studien zugrunde. Zur Ermittlung der demografischen Daten der Modellpopulation und der Sturzfolgekosten wurden Daten des Instituts für das Entgeltsystem im Krankenhaus (InEK), des Statistischen Bundesamtes und der Deutschen Rentenversicherung verwendet. Die Modellpopulation betrachtet Amputierte mit MPK oder NMPK mit und ohne vaskuläre Erkrankung in einem Altersbereich ab 40 Jahren.
Beurteilung der methodischen Qualität der ermittelten Studien
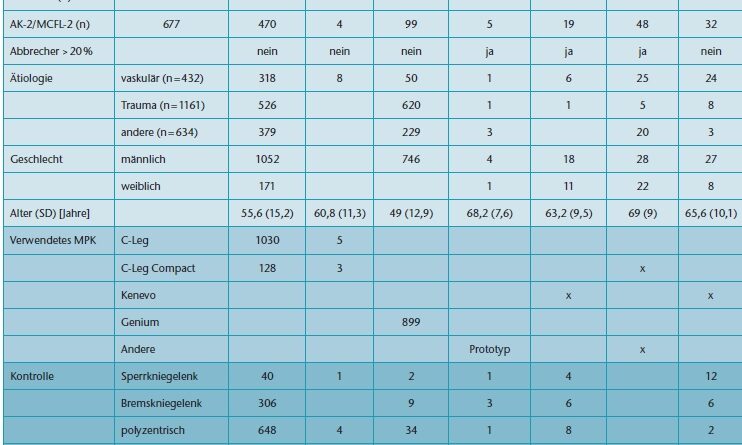
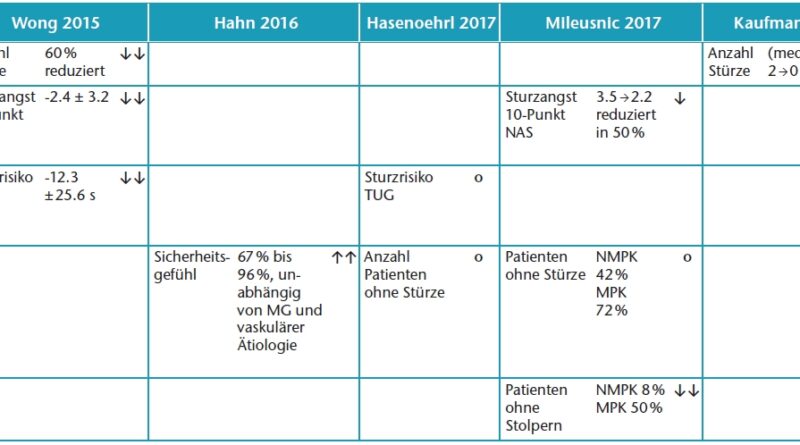
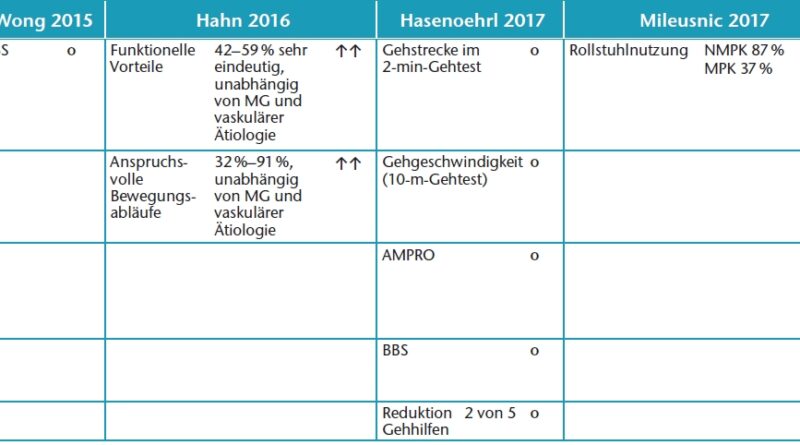
Die Ergebnisse der Bewertung der methodischen Qualität sind in Tabelle 1 dargestellt. Trotz starker Unterschiede in der Gesamtpunktzahl wurde bei allen eingeschlossenen Studien ein mittleres Qualitätsniveau festgestellt. Dies überrascht insbesondere bei der randomisierten Studie von Lansade et al. [28], deren methodische Qualität trotz des Erreichens von 13 von 14 möglichen Punkten angesichts des Fehlens einer Verblindung nur als „mittel“ einzustufen ist. Die demografischen Daten der 2.249 Patienten in den für die Analyse verwendeten Publikationen sowie Angaben zu den Studiendesigns, den verwendeten Interventions- bzw. Kontrollgelenken sind in Tabelle 2 dargestellt. In dieser Studiengruppe finden sich 692 Patienten mit Mobilitätsgrad 2; 436 Patienten weisen eine vaskuläre Erkrankung als Amputationsursache auf. In der Kosteneffizienz- und Kostenauswirkungsanalyse von Kuhlmann et al. [38] wird eine probabilistische Sensitivitätsanalyse (PSA) durchgeführt, die eine Abschätzung der Irrtumswahrscheinlichkeit des Modells und des Einflusses der unterschiedlichen Eingangsparameter erlaubt. Das Modell betrachtet 125 anhand von DRG-Angaben abgeleitete Kohorten über einen Zeitraum von 25 Jahren. Die Ergebnisse werden pro 1.000 Probandenjahre referenziert.Ergebnisse zur objektiven und subjektiv vom Patienten wahrgenommenen Sicherheit, Funktionalität und Mobilität sind in Tabelle 3 zusammenfassend wiedergegeben.
Ergebnisse zur Sicherheit
Alle klinischen Studien berichten über Ergebnisse zur Sicherheit des Prothesengebrauchs.
Wong et al. 56 und Kaufman et al. 57 berichten über eine signifikante (p < 0,05) Reduktion der Sturzanzahl während der jeweiligen Beobachtungszeiträume.
Lansade et al. 58 berichten über eine nichtsignifikante Reduktion der Sturzanzahl innerhalb des 4‑wöchigen Beobachtungszeitraums.
Wong et al. und Mileusnic et al. 59 berichten über eine Reduktion der mit einer numerischen Analogskala gemessenen Sturzangst. Dabei sind die Ergebnisse von Wong et al. signifikant (p = 0,042); die Ergebnisse von Mileusnic et al. lassen einen statistischen Trend erkennen (0.05 ≤ p [= 0,075] < 0.1).
Hahn et al. berichten in 60 von einer deutlich reduzierten Anzahl von Probanden mit Sturzangst (87 % in MG2, 95 % CI [0.871; 0.849].
Wong et al., Hasenöhrl et al. 61 und Lansade et al. berichten über den mit Sturzrisiko assoziierten Timedup- and-go-Test (TUG).
Lansade et al. berichten über eine hochsignifikante (p ≤ 0,001) und klinisch relevante Verbesserung mit „Kenevo“. Die signifikanten Ergebnisse (p = 0,043) von Wong et al. übersteigen deutlich den Minimal Detectable Change (MDC, Messfehler) von 3,6 s. Die Ergebnisse von Hasenöhrl et al. bleiben unter dem MDC und sind nicht signifikant.
Mileusnic et al. berichten über eine signifikante Reduktion der Anzahl der beobachteten Probanden mit Stolperereignissen (p = 0,044).
Hasenöhrl et al., Mileusnic et al. und Lansade et al. berichten über eine jeweils nichtsignifikante Steigerung der Anzahl von Personen, die nach MPK-Versorgung nicht mehr stürzen.
Hahn et al. berichten sowohl in 62 als auch in 63über eine signifikant höhere Anzahl von Probanden, die vergleichend eine Verbesserung ihres Sicherheitsempfindens angeben (85 % in MG2, 95 % CI [0,81; 0,88] für 64).
Während sehr wohl einzelne Probanden keine Verbesserung ihres Sicherheitsempfindens angeben, weist jedoch kein sicherheitsrelevanter Parameter einen statistisch signifikanten Effekt oder Trend zugunsten eines NMPK aus.
Ergebnisse zu Funktionalität und Mobilität
Statistisch signifikante Ergebnisse zur objektiven Bewertung von Funktionalität und Mobilität werden von 6 Studien berichtet. Dabei wurden die Ergebnisse des TUG nicht erneut gezählt. Mileusnic et al. 65 berichten über eine signifikante Reduktion der Anzahl der Probanden, die weiterhin einen Rollstuhl benutzen (p = 0,0046). Kaufman et al. 66 berichten über durch Aktivitätsmessung identifizierte signifikante Reduktionen der sitzend verbrachten Zeit (p = 0,01) und analog dazu signifikant erhöhte Bewegungsaktivität im Tagesverlauf (p = 0,02). Hahn et al. 67 68 berichten über die von den bewertenden Orthopädietechnikern dokumentierte Nutzung der Gebrauchsvorteile der MPKs. Darüber hinaus identifizierten Hahn et al. eine signifikant verbesserte Fähigkeit, komplexe Bewegungsabläufe (beispielsweise Rückwärtsgehen, Übersteigen von Hindernissen ohne Sicht, Richtungswechsel im Bewegungsablauf etc.) auszuführen, eine signifikante Reduktion der eingesetzten zusätzlichen Gehhilfen sowie eine signifikante Steigerung der Mobilitätsklasse. Während alle Studien auch über eine Anzahl Parameter berichten, für die keine signifikanten Unterschiede zwischen MPK und NMPK ermittelt wurden, ist erneut festzuhalten, dass für keinen einzigen der untersuchten Nutzenparameter ein Vorteil zugunsten eines NMPK nachweisbar war.
Wahrgenommene Funktionalität und Zufriedenheit mit der Prothese
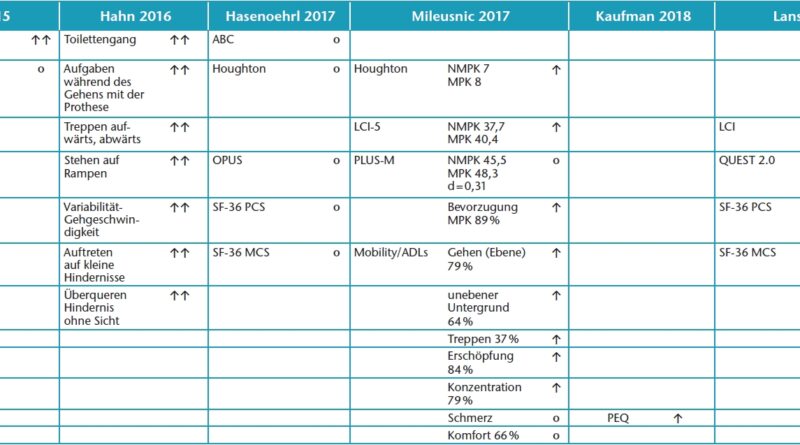
Lansade et al. 69berichten über hochsignifikante Verbesserungen der Versorgungszufriedenheit mit „Kenevo“ im validierten QUEST‑2.0‑Fragebogen (p = 0,001). Signifikante Verbesserungen berichten Lansade et al. auch bezüglich der subjektiv wahrgenommenen Mobilität mit „Kenevo“ im Locomotor Capability Index 5 (LCI‑5: p = 0,02) und im SF-36 Mental Component Score (MCS: p = 0,03). Kaufman et al. 70 ermitteln signifikante Verbesserungen der Zufriedenheit mit der Prothesenfunktionalität im Prosthesis Evaluation Questionnaire (PEQ: p = 0,01), während Wong et al. 71 eine signifikante Verbesserung des mittels Activity-specific Balance Confidence (ABC) Scale gemessenen Gleichgewichtsempfindens mit dem MPK feststellen konnten. Hahn et al. 72 73 sehen signifikante Verbesserungen in einer Reihe von Wahrnehmungskategorien, wobei die Perzeption des Toilettengangs als besonders aussagekräftig ermittelt wurde. Von den Patienten selbst berichtete Verbesserungen durch das MPK mit dem statistischen Charakter eines Trends werden von Lansade et al. für den SF-36 Physical Component Score (körperliche Leistungsfähigkeit) und von Mileusnic et al. 74 für die Houghton Scale (Prothesennutzung), den LCI‑5 (Ausführung von Aktivitäten des täglichen Lebens), die vergleichende Beurteilung verschiedener Gangsituationen und die Prothesenpräferenz ermittelt. Keine Verbesserungen in der Patientenwahrnehmung werden berichtet von Wong et al. für die Houghton Scale, von Hasenöhrl et al. 75 für die Houghton Scale, die ABC Scale, den OPUS-Fragebogen (Aktivitäten des täglichen Lebens) und die beiden SF- 36-Summenscores sowie von Mileusnic et al. für Schmerz und Komfort. Auch im Bereich der subjektiv von den Patienten wahrgenommenen Funktionalität und Zufriedenheit mit der Prothese wurden keine Parameter oder Kategorien identifiziert, in denen ein Vorteil zugunsten eines NMPK zu erkennen gewesen wäre.
Kosteneffizienz
Kuhlmann et al. 76ermittelten eine Verringerung der sturzbezogenen Hospitalisierungen bei Patienten mit nichtvaskulär bedingter Amputation von 134 auf 20 und bei vaskulär bedingter Amputation von 146 auf 23 pro 1.000 Patientenjahre. Für den Einsatz eines MPK wurde eine Vermeidung von 15 bzw. 14 Stürzen mit Todesfolge im gleichen Referenzzeitraum ermittelt. Die Basiswerte für die Kosten pro zusätzlichen QALY (Quality Adjusted Life Year) betragen 16.123 Euro für Patienten ohne und 20.332 Euro für Patienten mit Diabetes mellitus. Diese Werte liegen deutlich unterhalb des von der WHO für Kosteneffizienz vorgeschlagenen Vergleichswerts eines Pro- Kopf-BIP (Bruttoinlandsprodukt pro Kopf; in Deutschland im Jahr 2018 ca. 40.000 Euro). Die PSA ermittelte eine moderate Unsicherheit des Modells und erlaubt die Ermittlung der Kosteneffizienz mit 97- bis 99-prozentiger Wahrscheinlichkeit. Sollte eine vollständige Umstellung aller neuen Oberschenkelamputierten auf hydraulische MPKs erfolgen und 50 % der prävalenten Population ebenfalls umgestellt werden, so betrügen die Auswirkungen auf das deutsche Kostenträgerbudget (Budget-Impact- Analyse) in einem Zeitraum von 4 Jahren in Summe 93 Mio. Euro, d. h. unter 25 Mio. Euro pro Jahr. Dabei geht das Modell in seiner Simulationslogik davon aus, dass es noch keine MPK-versorgten Patienten gäbe, d. h., der reale Einfluss wäre um einiges geringer.
Diskussion
Die vorliegende Aktualisierung einer systematischen Analyse der Fachliteratur wurde mit der Fragestellung durchgeführt, ob einseitig oberschenkelamputierte Personen, die einer vulnerablen Patientengruppe angehören – d. h. solche mit Mobilitätsgrad AK/ MFCL‑2 oder insbesondere vaskulärer Ätiologie –, einen Nutzen aus der Verwendung eines mikroprozessorgesteuerten Prothesenkniegelenks ziehen können, wie dies für aktivere Patienten mit Mobilitätsgrad AK/MFCL- 3 77 78 79 80 81 82 83 84 85 86 87 88 89 90 91 bereits seit Längerem nachgewiesen ist.
In diesem Zusammenhang wurden 7 zusätzliche Peer-Review-publizierte Studien ermittelt, die den Nutzen von MPKs in dieser Patientengruppe untersucht haben. Alle verfügen über eine mittlere methodische Qualität. Dabei ist zu berücksichtigen, dass es in der Prothetikforschung erhebliche Hindernisse gegenüber anderen Bereichen von Medizinprodukten gibt. Dazu zählt wie in diesem Falle die praktische Unmöglichkeit einer Verblindung. Damit muss selbst die eigentlich exzellente methodische Qualität der Arbeit von Lansade et al. 92 allein aufgrund der fehlenden Verblindung als nur „mittel“ eingestuft werden.
Sicherheit
Die objektive und subjektiv wahrgenommene Sicherheit ist die Grundlage für einen umfassenden Gebrauch der Prothese im Alltag und für eine verbesserte Funktionalität und Mobilität 93 9495. Die von Kannenberg et al. 96 97 ermittelte signifikante 80-prozentige Reduktion von Anzahl und Häufigkeit unkontrollierter Stürze im Vergleich zu NMPKs 98 99 mit „C‑Leg“ konnte durch Wong et al. 100 und Kaufman et al. [29] 101erneut bestätigt werden.
Lansade et al. 102 weisen ebenfalls eine reduzierte Sturzanzahl aus, die aber keine statistische Signifikanz erreicht. Dies ist auf den vergleichsweise kurzen Beobachtungszeitraum (4 Wochen) zurückzuführen.
Hahn et al. 103 104, Wong et al. und Mileusnic et al. 105 berichten über eine signifikante Reduktion der Angst vor Stürzen. Kaufman et al. berichten, dass 30 % der Patienten nach der Versorgung mit einem MPK aus Angst vor Stürzen die Rückversorgung auf ihr ursprüngliches NMPK ablehnten und aus der Studie ausschieden. Die Furcht vor Stürzen hat einen signifikanten Einfluss auf die Lebensgestaltung, da die Betroffenen in der Regel aktiv Situationen mit Sturzrisiko vermeiden. Dies hat häufig einen Rückzug von sozialen Aktivitäten und eine erhebliche Einschränkung der Lebensqualität zur Folge.
Bereits Burnfield et al. 106 stellten in ihrer Studie eine signifikante Verringerung der für den Timed-up-andgo- Test (TUG) benötigten Zeit fest, die fast doppelt so groß war wie die von Resnik et al. 107 berichtete Messfehlertoleranz des Tests (MDC). Der TUG lag mit den MPKs sogar unter dem Schwellenwert von 19 Sekunden, der nach Dite et al. 108 ein Risiko für wiederholte Stürze bei Unterschenkelamputierten anzeigt. Lansade et al. bestätigen dieses Ergebnis in hochsignifikanter Weise – sowohl in der sogenannten Intention-to-Treat-Analyse (inklusive Studienabbrecher) als auch in der Per-Protocol-Analyse (ohne Studienabbrecher). Wong et al. bestätigen dieses Ergebnis in ihren Untersuchungen ebenfalls.
Hasenöhrl et al. 109 stellen zwar keine Veränderungen fest, sie beschränken sich allerdings aufgrund der sehr kleinen Gruppengröße und der großen Heterogenität nur auf eine beschreibende Darstellung.
Hahn et al. berichten sowohl für „C‑Leg“/„C‑Leg Compact“ 110 als auch für „Genium“ 111von einer signifikanten Verbesserung des Sicherheitsgefühls der Patienten. In 112 wird dies differenziert in Bezug auf verschiedene Gangsituationen berichtet. Dabei bestätigen die Regressionsanalysen in beiden Arbeiten diese Effekte auch für die niedrigen Mobilitätsgrade und die Ätiologie „vaskuläre Erkrankung“.
Hasenöhrl et al., Mileusnic et al. und Lansade et al. berichten jeweils über eine in den jeweiligen Studien nichtsignifikante Zunahme der Anzahl der Personen, die mit einem MPK nicht mehr stürzen. Mileusnic et al. berichten außerdem über eine signifikante Erhöhung der Anzahl von Personen, die mit „Kenevo“ nicht mehr stolpern.
Zusammenfassend zeigen alle Studien sowohl bezüglich der validierten leistungsbasierten Sicherheitsparameter als auch hinsichtlich der Skalen für die von den Patienten subjektiv wahrgenommene Sicherheit des Prothesengebrauchs einen erheblichen Sicherheitsgewinn durch ein MPK. Daraus kann geschlossen werden, dass die untersuchten hydraulischen MPKs die Sicherheit des Prothesengebrauchs bei einseitig oberschenkelamputierten Personen mit Mobilitätsgrad AK/MFCL‑2 und/oder vaskulärer Ätiologie im gleichen Ausmaß verbessern können wie bei Patienten mit höherem Mobilitätsgrad. Die dafür maßgeblich ausschlaggebenden bauartbedingten Unterschiede im Sicherheitsprofil verschiedener Kniepassteile wurden ausführlich von Blumentritt 113 und Kannenberg 114 115 beschrieben. Darüber hinaus sei der Hinweis gestattet, dass sich auch MPKs in ihrer Bauart, Sicherheit und Funktionalität zum Teil deutlich unterscheiden 116 117 118 119 120 . Die hier dargestellten Untersuchungsergebnisse wurden ganz überwiegend mit MPKs mit Linearhydraulik zur Stand- und Schwungphasensteuerung, das heißt „C‑Leg“, „Genium“ und „Kenevo“, erzielt. Der manifestierte Sicherheitsgewinn und hier insbesondere die reduzierte Sturzanzahl und damit die Verringerung der Sturzfolgekosten sind im Zusammenspiel mit der signifikanten Steigerung der Lebensqualität der maßgebende Faktor für die nachgewiesene Kosteneffizienz von MPKs in dieser besonders vulnerablen Patientengruppe 121. Somit ist auch der Anteil von Sturzereignissen mit tödlichem Ausgang in dieser Patientengruppe durch den Einsatzgeeigneter MPKs deutlich reduziert. Die seit 2014 neu publizierte Evidenz bestätigt damit die Ergebnisse früherer Untersuchungen in beeindruckender Weise in einer deutlich größeren Population.
Leistungsbasierte Funktionalität und Mobilität
Auch im Bereich der leistungsbezogenenFunktion und Mobilität setzt sich die Bestätigung der von Kannenberg et al. 122 123 identifizierten Ergebnisse fort.
So berichten Hahn et al. 124 125 über ähnliche Verbesserungen in der Zuordnung der Mobilitätsgrade wie Kahle et al. 126 sowie Hafner und Smith 127 . Jeweils 50 % der der Mobilitätsklasse 2 zugeordneten Patienten erreichen mit einem MPK den Wechsel in die Mobilitätsklasse 3.
Kaufman et al. 128 berichten über eine höhere Tagesaktivität und eine verringerte Zeit im Sitzen, während Mileusnic et al. 129 sogar über eine signifikant reduzierte Zahl von Probanden berichten, die neben der Prothese noch einen Rollstuhl nutzen. Man kann diese Verbesserungen durchaus so interpretieren, dass der zuvor erwähnte Verlust an Gangsicherheit ausgeglichen oder so weit abgemildert wurde, dass die Patienten ihr Aktivitätsniveau allgemein verbessern konnten.
Hahn et al. 130 131 berichten über eine erhöhte Anzahl von Patienten mit der Fähigkeit, die Gebrauchsvorteile des MPK zu demonstrieren. Diese grundsätzliche Fähigkeit ist dabei unabhängig vom Mobilitätsgrad. Das Fehlen eines Einflusses des Mobilitätsgrades wird von Hahn et al. [35]132 neben einer Korrelations- und Regressionsanalyse auch anhand einer grafischen Darstellung der zusammengefasstenMessungen der funktionellen Vorteile aufgezeigt. So ist sichtbar, dass das allgemeine Niveau im Mobilitätsgrad 2 zwar geringer ist, viele Patienten jedoch die Kriterien für einen funktionellen Zugewinn trotzdem erfüllen. Bei der Betrachtung komplexer Bewegungsmuster (Treppen hinauf und hinunter, Rückwärtsgehen, Übersteigen von Hindernissen etc.) zeigt sich dagegen, dass der Einfluss des Mobilitätsgrades am größten ist. Je nach Aufgabe beträgt er pro Mobilitätsgrad zwischen 0.32 und 2.29 Punkte Unterschied auf einer 5‑Punkt-Likert- Skala (p < 1E-24). Das heißt konkret, dass einige der besonders komplexen Manöver wie beispielsweise das alternierende Treppaufgehen nur von Patienten mit höheren Mobilitätsgraden bewältigt wird.
Während Hasenöhrl et al. 133 aufgrund der Eigenschaften ihrer spezifischen Kohorte trotz einer vergleichsweise hohen Anzahl an gemessenen Parametern keine Unterschiede zwischen den MPKs und mechanischen Kniegelenken feststellen konnten, berichten auch sie – ebenso wie Hahn et al. 134 – von einer Reduktion der verwendeten Gehhilfen. Gerade diese Reduktion der Gehhilfen kann ebenfalls als Indikator einer erhöhten Sicherheit gewertet werden, die aber gleichzeitig mit einer Reduktion der im Testverfahren gemessenen Gehgeschwindigkeit einhergehen kann.
Subjektiv wahrgenommene Funktionalität und Zufriedenheit
Während Kannenberg et al. 135 136 noch eine Diskrepanz zwischen den leistungsbasierten und den von den Patienten subjektiv berichteten Parametern in den seinerzeit ausgewerteten Studien ermittelten, ist dies in der aktualisierten Analyse so nicht mehr zu erkennen:
Lansade et al. 137 berichten über hochsignifikante Verbesserungen im QUEST 2.0 (Versorgungszufriedenheit) sowie über signifikante Verbesserungen im LCI‑5 (Aktivitäten des täglichen Lebens) und im SF-36 (Lebensqualität, psychisches Wohlbefinden) Mental Summary Score.
Kaufman et al. 138 berichten über signifikante Verbesserungen der Zufriedenheit mit der Prothese im PEQ, insbesondere in den Kategorien Fortbewegung, Erscheinungsbild und Nützlichkeit.
Wong et al. 139 berichten über signifikante Verbesserungen des Gleichgewichtsempfindens (ABC-Scale), und Hahn et al. stellen eine vom Mobilitätsgrad unabhängige Verbesserung in der Wahrnehmung diverser Aktivitätskategorien dar, wobei die Schwierigkeit des Toilettengangs als besonders sensitiver Parameter identifiziert wurde.
Mileusnic et al. 140 berichten über Trends zugunsten der MPKs in der Houghton Scale (Prothesennutzung), dem LCI‑5 und der Bewertung er Ausführung einiger spezifischer Bewegungsmuster durch die Patienten. Auffällig ist, dass sich die Verbesserungen im LCI‑5 primär in den Basisaktivitäten zeigen. Auch hier scheinen sich die sicherheitsrelevanten Aspekte des Gangbildes mit der Prothese bemerkbar zu machen. Gleichzeitig kann selbst von einem speziell auf die Bedürfnisse von Patienten mit niedrigem Mobilitätsgrad ausgerichteten hydraulischen MPK wie dem „Kenevo“ nicht erwartet werden, dass es die grundsätzlichen Mobilitätseinschränkungen infolge der Ätiologie bzw. der Morbidität vollständig kompensieren kann. Der Toilettengang und der dabei empfundene Zugewinn an Sicherheit zeigt sich in der Regressionsanalyse als besonders sensitiver Parameter, d. h., Auswirkungen von Komorbiditäten und der Effekte von MPKs zeigen sich hier sehr ausgeprägt. Schwerer betroffene Patienten empfinden in dieser Situation den Zugewinn durch das MPK als besonders vorteilhaft. Es ist leicht vorstellbar, dass in dieser spezifischen, höchst vulnerablen Situation, in der auf engem Raum teilweise rückwärts navigiert werden muss, der unterstützenden Wirkung eines MPK besondere Bedeutung zukommt. Es zeigt sich ferner, dass die Dimensionen, in denen die üblichen Messinstrumente die allgemeinen Mobilitätsvorteile erfassen, ggf. nicht immer alle wesentlichen Lebensbereiche abdecken. Gerade zu den Aspekten der Selbstversorgung und der Bewahrung der Unabhängigkeit in der Körperhygiene und persönlichen Pflege liegen nur wenige Untersuchungsergebnisse bei Prothesenträgern vor.
Die hohe Präferenz für die MPKs scheint die in der Klasse der eingeschränkten Außenbereichsgeher und der Patienten mit vaskulärer Ätiologie umfängliche Erfüllung der persönlichen Bedürfnisse abzubilden. Die Mitteilung von Kaufman et al. zur hohen Anzahl der Patienten, dieeine aus methodischen Gründen geplante Rückversorgung auf ihr NMPK verweigerten, unterstreicht diesen Aspekt in deutlicher Weise.
Kosteneffizienz
Die Bestimmung der Kosteneffizienz wurde in einer aus deutschen Amputationszahlen nach DRG-Report ermittelten Kohorte von Patienten beginnend mit einem Alter von 40 Jahren durchgeführt. Dabei wurden die von Cutti et al. 141 nach Altersklassen stratifizierten Utility-Werte angenommen. Cutti et al. ermittelten gerade in dieser Altersklasse aufgrund des steigenden Einflusses von Depressionen und Angstzuständen eine Reduktion der Kosteneffizienz und einen ICER-Wert von 51.000 Euro pro QALY. Gerade in dieser Altersklasse zeigten sich jedoch die von Kuhlmann et al. 142 berücksichtigten Effekte der Sturzfolgenvermeidung besonders deutlich und führten zu einer erheblichen Steigerung der Kosteneffizienz. Bemerkenswert ist, dass dies auch unter Berücksichtigung der hohen Mortalität insbesondere bei vaskulär betroffenen Patienten der Fall ist. Hier wird das in dieser Population überproportional hohe Verletzungsrisiko kompensiert.
Methodische Aspekte
Zusammenfassend lässt sich feststellen, dass sich die Evidenz zum Nutzen von MPK mit Linearhydraulik bei eingeschränkten Außenbereichsgehern und Amputierten mit vaskulärer Ätiologie sowohl in quantitativer als auch in qualitativer Hinsicht deutlich erweitert hat. Es ist dabei zu bemerken, dass selbst eine Arbeit wie die von Lansade et al. 143 aufgrund der fehlenden Verblindung als methodisch nur „mittel“ eingestuft werden kann. Die Weiterentwicklung adäquater Klassifizierungsmethoden und das Lösen des Verblindungsproblems wird die vorrangige Aufgabe beim Design klinischer Studien zur Bewertung exoprothetischer Komponenten bleiben. Fünf der bewerteten zusätzlichen Arbeiten sind ebenso wie die von Kannenberg et al. 144 145 bewerteten 6 Publikationen über 4 unabhängige Studien prospektiver Natur.
Die Arbeiten von Hahn et al. 146 147Aalysierten retrospektiv die Ergebnisse von Testversorgungen, deren Ergebnis zur Beantragung der Kostenübernahme verwendet wurden. Dies erfordert eine gesonderte Betrachtung unter Würdigung des Einflusses von Verzerrungsfaktoren (Bias).
Beide Kohorten bestanden aus Probanden, für die nach Einschätzung der untersuchenden Orthopädietechniker in einer Testversorgung sehr wahrscheinlich ein klinischer Nutzen des MPK nachweisbar sein würde. Tatsächlich handelt es sich hier aber – entgegen gelegentlich wahrscheinlich unzureichend reflektierten Einwänden – nicht um eine Verzerrung („selection bias“), sondern um ein Ergebnis. Während die detaillierten Vorauswahlkriterien des Orthopädietechnikers unbekannt sein mögen, so stellt die Kohorte in ihrer demografischen Vielfalt, ausgerichtet am Potenzial zur Erfüllung funktionaler Gebrauchsvorteile, das Ergebnis genau dieser Selektion dar. Auch wenn sich daraus eine Generalisierbarkeit der Ergebnisse nicht unmittelbar ableiten lässt, so gilt dennoch genauso, dass die in der Kohorte verbleibenden Parameter (beispielsweise Mobilitätsgrad oder Ätiologie u. v. m.) ihre Qualifikation als Kontraindikation eingebüßt haben. Mit anderen Worten: Das Potenzial von Probanden niedriger Mobilitätsgrade oder beispielsweise vaskulärer Ätiologie, von Gelenken wie „C‑Leg“ oder „Genium“ zu profitieren, ergibt sich allein aus ihrer Repräsentanz in der Kohorte selbst.
Wurdemann et al. 148 haben in einer ähnlichen Analyse den Einfluss des Funktionalen Komorbiditätsindex auf die Mobilität von Probanden mit MPKs ermittelt und kommen zu der gleichen Schlussfolgerung: Ein Einfluss ist zwar erkennbar – eine Vorhersagekraft, wie sie beispielsweise für ein Ausschlusskriterium erforderlich wäre, lasst sich jedoch nicht ableiten. Auch Wurdemann et al. konstatieren, dass Faktoren wie der Body Mass Index (BMI) sich durch das Fehlen jeglicher Sensitivität nicht einmal in den Kreis möglicher Ausschlusskriterien einreihen können.
Kannenberg et al. 149150 wiesen in ihrer Arbeit darauf hin, dass für Probanden mit Gehgeschwindigkeiten unterhalb von 0,5 m/s keine ausreichenden Untersuchungsergebnisse vorlagen.
Kaufman et al. 151[29] nehmen diesen Hinweis auf und legen dar, dass diese Evidenzlücke mit ihrer Arbeit nun geschlossen worden sei. Zusammenfassend darf man angesichts des aktuellen Standes der Literatur feststellen, dass die Hypothese, ein eingeschränkter Mobilitätsgrad oder die Atiologie „vaskuläre Erkrankung“ schlössen eine Versorgung mit MPK aufgrund mangelnder klinischer Vorteile aus, wissenschaftlich nicht haltbar ist. Die Autoren bewerten das Vorenthalten einer medizinisch und gesundheitsökonomisch sinnvollen Technologie auf der Grundlage wissenschaftlich nur schwer begründbarer Einzelparameter ohne nachgewiesene Vorhersagekraft angesichts der für den Einzelnen möglichen schwerwiegenden Folgen als äußerst problematisch.
Limitationen
Der Stand der Literatur und damit die Anzahl der untersuchten Probanden haben sich stark erweitert. Auch finden sich keine Parameter, die systematisch eine Aussage zugunsten von NMPKs erlauben würden. Die identifizierten neuen Studien beinhalten eine Vielzahl von Perspektiven und decken unterschiedliche Untersuchungsszenarien und Aspekte des funktionellen Zugewinns durch MPK ab. Dennoch verhindert das Problem einer effektiven Verblindung die Durchführung klinischer Studien mit einer dem allgemeinen Standard der Medizintechnik entsprechenden formal hohen methodischen Qualität. Auch leiden einige Arbeiten unter einer hohen Rate an Studienabbrechern, und da diese sich überwiegend in der vaskulären Population befinden, ist auch der Einfluss der Progression der Grunderkrankung vor allem bei längeren Beobachtungszeiträumen zu berücksichtigen. Alle Studien berichten von Einzelsituationen, in denen ein Zugewinn klinisch effektiver Wirksamkeit weniger hoch als gewünscht ausfällt. Die untersuchten Patientengruppen sind in hohem Maße komorbid, auch kognitive Fähigkeiten spielen dabei eine Rolle. Daher bleibt auch in diesen Studien die Frage nach der universellen Generalisierbarkeit der Ergebnisse offen. Gleichzeitig gilt umgekehrt, dass einem grundsätzlichen Ausschluss dieser Patienten von der Versorgung mit MPK mit Linearhydraulik jede wissenschaftliche Grundlage fehlt. Im Zweifel bleibt die Empfehlung der individuellen Probeversorgung zur Ermittlung des individuellen Potenzials das Mittel der Wahl. Die weitere Forschung wird sich mit den spezifischen Gegebenheiten und Bedürfnissen dieser Patientengruppe intensiver auseinandersetzen müssen.
Schlussfolgerungen
Die Ergebnisse dieser aktualisierten systematischen Übersichtsarbeit legen nahe, dass eingeschränkte Außenbereichsgeher und Prothesennutzer mit vaskulärer Amputationsätiologie durch die Nutzung mikroprozessorgesteuerter Prothesengelenke ihr Sturzrisiko, ihre Sturzangst und die Zahl ihrer Stürze signifikant reduzieren können. Aktivitäten im Außenbereich, die eigentlich typisch für den Mobilitätsgrad AK/MFCL‑3 sind, können signifikant besser ausgeführt werden. Dies spiegelt sich auch in der Eigenwahrnehmung der Patienten wider. Die speziell auf die Bedürfnisse dieser Patientengruppe abgestimmten Passteile erhöhen dabei die Wahrscheinlichkeit einer erfolgreichen und sicheren Versorgung. Insgesamt stützen die Ergebnisse der vorliegenden Arbeit die Position, die Nutzung von MPKs bei eingeschränkten Außenbereichsgehern mit einseitiger Oberschenkelamputation heute als Standardversorgung zu betrachten. Testversorgungen
können dazu beitragen, Patienten zu identifizieren, die nicht von einem MPK profitieren.
Für die Autoren:
Dr. med. Andreas Kannenberg
Executive Medical Director North America Otto Bock HealthCare LP
11501 Alterra Parkway, Suite 600 Austin, Texas 78758 USA
andreas.kannenberg@ottobock.com
Begutachteter Beitrag/reviewed paper
Hahn A, Kannenberg A. Zum Nutzen mikroprozessorgesteuerter Prothesenkniegelenke bei eingeschränkten Außenbereichsgehern: eine aktualisierte systematische Literaturanalyse. Orthopädie Technik, 2020; 71 (5): 46–57
- Entwicklung eines zum physiologischen Gangbild kongruenten polyzentrischen Knieorthesengelenks – Zwischenstand eines Forschungsprojektes — 10. April 2026
- Mikroprozessorgesteuerte stand- und schwungphasenkontrollierte Ganzbeinorthesen (SSCO): Entwicklung, Systeme und Versorgungsrealität in der orthopädietechnischen Praxis — 9. April 2026
- Gips oder Orthese bei distalen Radiusfrakturen? — 8. April 2026
- Nelson VS, Flood KM, Bryant PR, Huang ME, Pasquina PF, Roberts TL. Limb deficiency and prosthetic management. 1. Decision in making prosthetic prescription and management. Arch Phys Med Rehabil, 2006; 87 (Suppl. 1): S3–S9. PMID:
16500189 - Sawers AB, Hafner BJ. Outcomes associated with the use of microprocessor-controlled prosthetic knees among individuals with unilateral transfemoral limb loss: A systematic review. J Rehab Res Dev, 2013; 50 (3): 273–314. PMID: 23881757
- Blumentritt S, Schmalz T, Jarasch R. The safety of C‑leg: Biomechanical tests. J Prosthet Orthot, 2009; 21 (1): 2–17
- Blumentritt S. Biomechanische Aspekte zur Indikation von Prothesenkniegelenken. Orthopädie Technik, 2004; 55 (6): 508–524
- Berry D, Olson MD, Larntz K. Perceived stability, function, and satisfaction among transfemoral amputees using microprocessor and non-microprocessor controlled prosthetic knees: a multicenter survey. J Prosthet Orthot, 2009; 21 (1): 32–42
- Kaufman KR, Levine JA, Brey RH, Iverson BK, McGrady SK, Padgett DJ, Joyner MJ. Gait and balance of transfemoral amputees using passive mechanical and microprocessor-controlled prosthetic knees. Gait Posture, 2007; 26 (4): 489–493. PMID: 17869114
- Segal AD, Orendurff MS, Klute GK, McDowell ML, Pecoraro JA, Shofer J, Czerniecki JM. Kinematic and kinetic comparisonsof transfemoral amputee gait using C‑Leg and Mauch SNS prosthetic knees. J Rehabil Res Dev, 2006; 43 (7): 857–870. PMID: 17436172
- Kahle JT, Highsmith MJ, Hubbard SL. Comparison of non-microprocessor knee mechanism versus C‑Leg on prosthesisevaluation questionnaire, stumbles, falls, walking tests, stair descent, and knee preference. J Rehabil Res Dev, 2008; 45 (1): 1–14. PMID: 18566922
- Seymour R, Engbretson B, Kott K, Ordway N, Brooks G, Crannell J, Hickernell E, Wheller K. Comparison between the Cleg® microprocessor-controlled prosthetic knee and non-microprocessor control prosthetic knees: A preliminary study of energy expenditure, obstacle course performance, and quality of life survey. Prosthet Orthot Int, 2007; 31 (1): 51–61. PMID: 17365885
- Berry D, Olson MD, Larntz K. Perceived stability, function, and satisfaction among transfemoral amputees using microprocessor
and non-microprocessor controlled prosthetic knees: a multicenter survey. J Prosthet Orthot, 2009; 21 (1): 32–42 - Kaufman KR, Levine JA, Brey RH, Iverson BK, McGrady SK, Padgett DJ, Joyner MJ. Gait and balance of transfemoralamputees using passive mechanical and microprocessor-controlled prosthetic knees. Gait Posture, 2007; 26 (4): 489–493. PMID: 17869114
- Kahle JT, Highsmith MJ, Hubbard SL. Comparison of non-microprocessor knee mechanism versus C‑Leg on prosthesisevaluation questionnaire, stumbles, falls, walking tests, stair descent, and knee preference. J Rehabil Res Dev, 2008; 45 (1): 1–14. PMID: 18566922
- Seymour R, Engbretson B, Kott K, Ordway N, Brooks G, Crannell J, Hickernell E, Wheller K. Comparison between the Cleg® microprocessor-controlled prosthetic knee and non-microprocessor control prosthetic knees: A preliminary study of energy expenditure, obstacle course performance, and quality of life survey. Prosthet Orthot Int, 2007; 31 (1): 51–61. PMID:
17365885 - Berry D, Olson MD, Larntz K. Perceived stability, function, and satisfaction among transfemoral amputees using microprocessorand non-microprocessor controlled prosthetic knees: a multicenter survey. J Prosthet Orthot, 2009; 21 (1): 32–42
- Kahle JT, Highsmith MJ, Hubbard SL. Comparison of non-microprocessor knee mechanism versus C‑Leg on prosthesisevaluation questionnaire, stumbles, falls, walking tests, stair descent, and knee preference. J Rehabil Res Dev, 2008; 45 (1): 1–14. PMID: 18566922
- Highsmith MJ, Kahle JT, Miro RM, Mengelkoch LJ. Ramp descent performance with the C‑leg and interrater reliabilityof the Hill Assessment Index. J Prosthet Orthot, 2013; 37 (5): 362–368
- Hafner BJ, Willingham LL, Buell NC, Allyn KJ, Smith DG. Evaluation of function, performance, and preference as transfemoral amputees transition from mechanical to microprocessor control of the prosthetic knee. Arch Phys Med Rehabil, 2007; 88 (2): 207–217. PMID: 17270519
- Lura, Derek J. Effects of the Genium Microprocessor Knee System on Knee Moment Symmetry During Hill Walking.Technol Innov, 2016; 18 (2):151–157. doi: 10.21300/18.2–3.2016.151
- Blumentritt S, Schmalz T, Jarasch R. The safety of C‑leg: Biomechanical tests. J Prosthet Orthot, 2009; 21 (1): 2–17
- Kahle JT, Highsmith MJ, Hubbard SL. Comparison of non-microprocessor knee mechanism versus C‑Leg on prosthesisevaluation questionnaire, stumbles, falls, walking tests, stair descent, and knee preference. J Rehabil Res Dev, 2008; 45 (1):
1–14. PMID: 18566922 - Highsmith MJ, Klenow TD, Kahle JT, Wernke MM, Carey SL, Miro RM, Lura DJ, Sutton BS. Effects of the Genium kneesystem on functional level, stair ambulation, perceptive and economic outcomes in transfemoral amputees. Technol Innov, 2016; 18: 139–150. doi: 10.21300/18.2–3.2016.139
- Lura DJ, Wernke MW, Carey SL, Kahle JT, Miro RM, Highsmith MJ. Crossover study of amputee stair ascent and descent biomechanics using Genium and C‑Leg prostheses with comparison to non-amputee control. Gait Posture, 2017; 58: 103–107. doi: 10.1016/j.gaitpost.2017.07.114
- Schmalz T, Blumentritt S, Marx B. Biomechanical analysis of stair ambulation in lower limb amputees. Gait Posture,2007; 25 (2): 267–278. PMID: 16725325
- Blumentritt S, Schmalz T, Jarasch R. The safety of C‑leg: Biomechanical tests. J Prosthet Orthot, 2009; 21 (1): 2–17
- Blumentritt S. Biomechanische Aspekte zur Indikation von Prothesenkniegelenken. Orthopädie Technik, 2004; 55 (6):508–524
- Blumentritt S, Schmalz T, Jarasch R. The safety of C‑leg: Biomechanical tests. J Prosthet Orthot, 2009; 21 (1): 2–17
- Berry D, Olson MD, Larntz K. Perceived stability, function, and satisfaction among transfemoral amputees using microprocessorand non-microprocessor controlled prosthetic knees: a multicenter survey. J Prosthet Orthot, 2009; 21 (1): 32–42
- Kahle JT, Highsmith MJ, Hubbard SL. Comparison of non-microprocessor knee mechanism versus C‑Leg on prosthesisevaluation questionnaire, stumbles, falls, walking tests, stair descent, and knee preference. J Rehabil Res Dev, 2008; 45 (1): 1–14. PMID: 18566922
- Hafner BJ, Willingham LL, Buell NC, Allyn KJ, Smith DG. Evaluation of function, performance, and preference astransfemoral amputees transition from mechanical to microprocessor control of the prosthetic knee. Arch Phys Med
Rehabil, 2007; 88 (2): 207–217. PMID: 17270519 - Lura, Derek J. Effects of the Genium Microprocessor Knee System on Knee Moment Symmetry During Hill Walking.Technol Innov, 2016; 18 (2):151–157. doi: 10.21300/18.2–3.2016.151
- Highsmith MJ, Kahle JT, Shepard NT, Kaufman KR. The effect of the C‑Leg knee prosthesis on sensory dependency andfalls during sensory organization testing. Technology and Innovation, 2014; 2013 (15): 343–347
- Highsmith MJ, Kahle JT, Bongiorni DR, Sutton BS, Groer S, Kaufman KR. Safety, energy efficiency, and cost efficacy of the C‑leg for transfemoral amputees. Prosthet Orthot Int, 2010; 34 (4): 362–377. PMID: 20969495
- Chen C, Hanson M, Chaturvedi R, Mattke S, Hillestad R. Economic benefits of microprocessor controlled prostheticknees: a modeling study. J Neuroeng Rehabil, 2018 (25): 62. doi: 10.1186/s12984-018‑0405‑8
- Cutti AG, Lettieri E, Del Maestro M, Radaelli G, Luchetti M, Verni G, Masella C. Stratified cost-utility analysis of C‑Legversus mechanical knees: Findings from an Italian sample of transfemoral amputees. Prosthet Orthot Int, 2017; 41 (3): 227–236. doi: 10.1177/0309364616637955
- Alemayehu B, Warner KE. The lifetime distribution of health care costs. Health Serv Res, 2004; 39 (3): 627–642. PMID:
14159482 - Lubitz J, Riley GF. Trends in Medicare payments in the last year of life. N Engl J Med 1993; 328 (15): 1092–1096. PMID: 8455667
- Hoover D, Crystal S, Kumar R, Sambamoorthi U, Cantor J. Medical expenditures during the last year of life: findingsfrom the 1992–1996 Medicare Current Beneficiary Survey. Health Serv Res, 2002; 37 (6):1625–1642. PMID: 12656289
- The Global Lower Extremity Amputation Study Group. Epidemiology of lower extremity amputation in centres inEurope, North America, and East Asia. Br J Surg, 2000; 87 (3): 328–337. PMID: 10718803
- van Velzen JM, van Bennekom CA, Polomski W, Slootman JT, an der Woude LH, Houdijk H. Physical capacityand walking ability after lower limb amputation: a systematic review. Clin Rehabil, 2006; 20 (11): 999‑1016. PMID: 17065543
- Kannenberg A, Zacharias B, Pröbsting E. Benefits of microprocessor-controlled prosthetic knees to limited communityambulators: Systematic review. J Rehabil Res Dev, 2014; 51 (10): 1469–1496. doi: 10.1682/JRRD.2014.05.0118
- Kannenberg A, Zacharias B, Pröbsting E. Zum Nutzen mikroprozessor-gesteuerter Prothesenkniegelenke bei eingeschränkten Außenbereichsgehern. Eine systematische Analyse der Literatur. Orthopädie Technik, 2015; 66 (2):18–29
- Kannenberg A, Zacharias B, Pröbsting E. Benefits of microprocessor-controlled prosthetic knees to limited community ambulators: Systematic review. J Rehabil Res Dev, 2014; 51 (10): 1469–1496. doi: 10.1682/JRRD.2014.05.0118
- Kannenberg A, Zacharias B, Pröbsting E. Zum Nutzen mikroprozessor-gesteuerter Prothesenkniegelenke bei eingeschränkten Außenbereichsgehern. Eine systematische Analyse der Literatur. Orthopädie Technik, 2015; 66 (2):18–29
- Hofstad CJ, van der Linde H, van Limbeek J, Postema K. Prescription of prosthetic ankle-foot mechanisms after lower limb amputation. Cochrane Database Syst Rev, 2004, (1): Art. No.: CD003978. doi: 10.1002/14651858.CD003978.pub2
- Lansade C, Vicaut E, Paysant J, Ménager D, Cristina MC, Braatz F, Domayer S, Perennou D, Chiesa G. Mobility and satisfaction with a microprocessor-controlled knee in moderately active amputees: A multi-centric randomized crossover trial. Ann Phys Rehabil Med, 2018; (61): 278–285. doi: 10.1016/j.rehab.2018.04.003. PMID: 29753888
- Kaufman KR, Bernhardt KA, Symms K. Functional assessment and satisfaction of transfemoral amputees with mobility (FASTK2): A clinical trial of microprocessor-controlled vs. non-microprocessor-controlled knees. Clin Biomech (Bristol, Avon), 2018; 58: 116–122. doi: 10.1016/j.clinbiomech.2018.07.012
- Wong K, Rheinstein J, Stern MA. Benefits for adults with transfemoral amputation and peripheral artery disease using microprocessor compared with nonmicroprocessor prosthetic knees. Arch Phys Med Rehabil, 2015; 94 (10): 804–810. doi:10.1097/PHM.0000000000000265
- Mileusnic MP, Hahn A, Reiter S. Effects of a Novel Microprocessor-Controlled Knee, Kenevo, on the Safety, Mobility, and Satisfaction of Lower-Activity Patients with Transfemoral Amputation. J Prosthet Orthot, 2017; 29 (4): 198–205
- Hasenoehrl T, Schmalz T, Windhager R, Domayer S, Dana S, Ambrozy C, et al. Safety and function of a prototype microprocessor-controlled knee prosthesis for low active transfemoral amputees switching from a mechanic knee prosthesis: a pilot study. Disabil Rehabil Assist Technol, 2018; 13 (2): 157–165. PMID: 28399722. doi: 10.1080/17483107.2017.1300344
- Hahn A, Lang M. Effects of mobility grade, age, and etiology on functional benefit and safety of subjects evaluated in more than 1200 C‑Leg trial fittings in Germany. J Prosthet Orthot, 2015; 27 (3): 86–95
- Hahn A, Lang M. Corrigendum to [35], J Prosthet Orthot, 2019; 31 (1): 80
- Hahn A, Lang M, Stuckert C. Analysis of clinically important factors on the performance of advanced hydraulic, microprocessor-controlled exo-prosthetic knee joints based on 899 trial fittings. Medicine (Baltimore), 2016; 95 (45): e5386. PMID:27828871
- Wetz HH, Hafkemeyer U, Drerup B. Einfluss des C‑Leg-Kniegelenk-Passteiles der Fa. Otto Bock auf die Versorgungsqualität Oberschenkelamputierter: Eine klinisch-biomechanische Studie zur Eingrenzung von Indikationskriterien. [The influence of the C‑Leg knee shin system of Otto Bock on the care of above-knee amputees: A clinical biomechanical study to define indications.] Orthopäde, 2005; 34 (4): 298–319. PMID: 15812621
- Kuhr K. Multivariate Analyse des funktionellen Zugewinns bei Kniegelenksystemen. Diplomarbeit, TU Dortmund, 2008
- Kuhlmann A, Krüger H, Seidinger S, Hahn A. Cost-effectiveness and budget impact of the microprocessor-controlled knee C‑Leg in transfemoral amputees with and without diabetes mellitus. Eur J Health Econ, 2020. doi: 10.1007/s10198-019–01138‑y [Epub ahead of print]
- Wong K, Rheinstein J, Stern MA. Benefits for adults with transfemoral amputation and peripheral artery disease using microprocessor compared with nonmicroprocessor prosthetic knees. Arch Phys Med Rehabil, 2015; 94 (10): 804–810. doi: 10.1097/PHM.0000000000000265
- Kaufman KR, Bernhardt KA, Symms K. Functional assessment and satisfaction of transfemoral amputees with mobility (FASTK2): A clinical trial of microprocessor-controlled vs. non-microprocessor-controlled knees. Clin Biomech (Bristol, Avon), 2018; 58: 116–122. doi: 10.1016/j.clinbiomech.2018.07.012
- Lansade C, Vicaut E, Paysant J, Ménager D, Cristina MC, Braatz F, Domayer S, Perennou D, Chiesa G. Mobility and satisfaction with a microprocessor-controlled knee in moderately active amputees: A multi-centric randomized crossover trial. Ann Phys Rehabil Med, 2018; (61): 278–285. doi: 10.1016/j.rehab.2018.04.003. PMID: 29753888
- Mileusnic MP, Hahn A, Reiter S. Effects of a Novel Microprocessor-Controlled Knee, Kenevo, on the Safety, Mobility, and Satisfaction of Lower-Activity Patients with Transfemoral Amputation. J Prosthet Orthot, 2017; 29 (4): 198–205
- Hahn A, Lang M, Stuckert C. Analysis of clinically important factors on the performance of advanced hydraulic, microprocessor-controlled exo-prosthetic knee joints based on 899 trial fittings. Medicine (Baltimore), 2016; 95 (45): e5386. PMID:27828871
- Hasenoehrl T, Schmalz T, Windhager R, Domayer S, Dana S, Ambrozy C, et al. Safety and function of a prototype microprocessor-controlled knee prosthesis for low active transfemoral amputees switching from a mechanic knee prosthesis: a pilot study. Disabil Rehabil Assist Technol, 2018; 13 (2): 157–165. PMID: 28399722. doi: 10.1080/17483107.2017.1300344
- Hahn A, Lang M. Effects of mobility grade, age, and etiology on functional benefit and safety of subjects evaluated in more than 1200 C‑Leg trial fittings in Germany. J Prosthet Orthot, 2015; 27 (3): 86–95
- Hahn A, Lang M, Stuckert C. Analysis of clinically important factors on the performance of advanced hydraulic, microprocessor-controlled exo-prosthetic knee joints based on 899 trial fittings. Medicine (Baltimore), 2016; 95 (45): e5386. PMID:27828871
- Hahn A, Lang M, Stuckert C. Analysis of clinically important factors on the performance of advanced hydraulic, microprocessor-controlled exo-prosthetic knee joints based on 899 trial fittings. Medicine (Baltimore), 2016; 95 (45): e5386. PMID:27828871
- Mileusnic MP, Hahn A, Reiter S. Effects of a Novel Microprocessor-Controlled Knee, Kenevo, on the Safety, Mobility, and Satisfaction of Lower-Activity Patients with Transfemoral Amputation. J Prosthet Orthot, 2017; 29 (4): 198–205
- Kaufman KR, Bernhardt KA, Symms K. Functional assessment and satisfaction of transfemoral amputees with mobility (FASTK2): A clinical trial of microprocessor-controlled vs. non-microprocessor-controlled knees. Clin Biomech (Bristol, Avon), 2018; 58: 116–122. doi: 10.1016/j.clinbiomech.2018.07.012
- Hahn A, Lang M. Effects of mobility grade, age, and etiology on functional benefit and safety of subjects evaluated in more than 1200 C‑Leg trial fittings in Germany. J Prosthet Orthot, 2015; 27 (3): 86–95
- Hahn A, Lang M, Stuckert C. Analysis of clinically important factors on the performance of advanced hydraulic, microprocessor-controlled exo-prosthetic knee joints based on 899 trial fittings. Medicine (Baltimore), 2016; 95 (45): e5386. PMID:27828871
- Lansade C, Vicaut E, Paysant J, Ménager D, Cristina MC, Braatz F, Domayer S, Perennou D, Chiesa G. Mobility and satisfaction with a microprocessor-controlled knee in moderately active amputees: A multi-centric randomized crossover trial. Ann Phys Rehabil Med, 2018; (61): 278–285. doi: 10.1016/j.rehab.2018.04.003. PMID: 29753888
- Kaufman KR, Bernhardt KA, Symms K. Functional assessment and satisfaction of transfemoral amputees with mobility (FASTK2): A clinical trial of microprocessor-controlled vs. non-microprocessor-controlled knees. Clin Biomech (Bristol, Avon), 2018; 58: 116–122. doi: 10.1016/j.clinbiomech.2018.07.012
- Wong K, Rheinstein J, Stern MA. Benefits for adults with transfemoral amputation and peripheral artery disease using microprocessor compared with nonmicroprocessor prosthetic knees. Arch Phys Med Rehabil, 2015; 94 (10): 804–810. doi: 10.1097/PHM.0000000000000265
- Hahn A, Lang M. Effects of mobility grade, age, and etiology on functional benefit and safety of subjects evaluated in more than 1200 C‑Leg trial fittings in Germany. J Prosthet Orthot, 2015; 27 (3): 86–95
- Hahn A, Lang M, Stuckert C. Analysis of clinically important factors on the performance of advanced hydraulic, microprocessor-controlled exo-prosthetic knee joints based on 899 trial fittings. Medicine (Baltimore), 2016; 95 (45): e5386. PMID:27828871
- Mileusnic MP, Hahn A, Reiter S. Effects of a Novel Microprocessor-Controlled Knee, Kenevo, on the Safety, Mobility, and Satisfaction of Lower-Activity Patients with Transfemoral Amputation. J Prosthet Orthot, 2017; 29 (4): 198–205
- Mileusnic MP, Hahn A, Reiter S. Effects of a Novel Microprocessor-Controlled Knee, Kenevo, on the Safety, Mobility, and Satisfaction of Lower- Activity Patients with Transfemoral Amputation. J Prosthet Orthot, 2017; 29 (4): 198–205
- Kuhlmann A, Krüger H, Seidinger S, Hahn A. Cost-effectiveness and budget impact of the microprocessor-controlled knee C‑Leg in transfemoral amputees with and without diabetes mellitus. Eur J Health Econ, 2020. doi: 10.1007/s10198- 019–01138‑y [Epub ahead of print]
- Blumentritt S, Schmalz T, Jarasch R. The safety of C‑leg: Biomechanical tests. J Prosthet Orthot, 2009; 21 (1): 2–17
- Blumentritt S. Biomechanische Aspekte zur Indikation von Prothesenkniegelenken. Orthopädie Technik, 2004; 55 (6): 508–524
- Berry D, Olson MD, Larntz K. Perceived stability, function, and satisfaction among transfemoral amputees using microprocessor and non-microprocessor controlled prosthetic knees: a multicenter survey. J Prosthet Orthot, 2009; 21 (1): 32–42
- Kaufman KR, Levine JA, Brey RH, Iverson BK, McGrady SK, Padgett DJ, Joyner MJ. Gait and balance of transfemoral amputees using passive mechanical and microprocessor-controlled prosthetic knees. Gait Posture, 2007; 26 (4): 489–493. PMID: 17869114
- Segal AD, Orendurff MS, Klute GK, McDowell ML, Pecoraro JA, Shofer J, Czerniecki JM. Kinematic and kinetic comparisons of transfemoral amputee gait using C‑Leg and Mauch SNS prosthetic knees. J Rehabil Res Dev, 2006; 43 (7): 857–870. PMID: 17436172
- Kahle JT, Highsmith MJ, Hubbard SL. Comparison of non-microprocessor knee mechanism versus C‑Leg on prosthesis evaluation questionnaire, stumbles, falls, walking tests, stair descent, and knee preference. J Rehabil Res Dev, 2008; 45 (1): 1–14. PMID: 18566922
- Seymour R, Engbretson B, Kott K, Ordway N, Brooks G, Crannell J, Hickernell E, Wheller K. Comparison between the Cleg ® microprocessor-controlled prosthetic knee and non-microprocessor control prosthetic knees: A preliminary study of energy expenditure, obstacle course performance, and quality of life survey. Prosthet Orthot Int, 2007; 31 (1): 51–61. PMID: 17365885
- Highsmith MJ, Kahle JT, Miro RM, Mengelkoch LJ. Ramp descent performance with the C‑leg and interrater reliability of the Hill Assessment Index. J Prosthet Orthot, 2013; 37 (5): 362–368
- Hafner BJ, Willingham LL, Buell NC, Allyn KJ, Smith DG. Evaluation of function, performance, and preference as transfemoral amputees transition from mechanical to microprocessor control of the prosthetic knee. Arch Phys Med Rehabil, 2007; 88 (2): 207–217. PMID: 17270519
- Lura, Derek J. Effects of the Genium Microprocessor Knee System on Knee Moment Symmetry During Hill Walking. Technol Innov, 2016; 18 (2):151–157. doi: 10.21300/18.2–3.2016.151
- Highsmith MJ, Klenow TD, Kahle JT, Wernke MM, Carey SL, Miro RM, Lura DJ, Sutton BS. Effects of the Genium knee system on functional level, stair ambulation, perceptive and economic outcomes in transfemoral amputees. Technol Innov, 2016; 18: 139–150. doi: 10.21300/18.2–3.2016.139
- Lura DJ, Wernke MW, Carey SL, Kahle JT, Miro RM, Highsmith MJ. Crossover study of amputee stair ascent and descent biomechanics using Genium and C‑Leg prostheses with comparison to non-amputee control. Gait Posture, 2017; 58: 103–107. doi: 10.1016/j.gaitpost.2017.07.114
- Schmalz T, Blumentritt S, Marx B. Biomechanical analysis of stair ambulation in lower limb amputees. Gait Posture, 2007; 25 (2): 267–278. PMID: 16725325
- Highsmith MJ, Kahle JT, Shepard NT, Kaufman KR. The effect of the C‑Leg knee prosthesis on sensory dependency and falls during sensory organization testing. Technology and Innovation, 2014; 2013 (15): 343–347
- Highsmith MJ, Kahle JT, Bongiorni DR, Sutton BS, Groer S, Kaufman KR. Safety, energy efficiency, and cost efficacy of the C‑leg for transfemoral amputees. Prosthet Orthot Int, 2010; 34 (4): 362–377. PMID: 20969495
- Lansade C, Vicaut E, Paysant J, Ménager D, Cristina MC, Braatz F, Domayer S, Perennou D, Chiesa G. Mobility and satisfaction with a microprocessor-controlled knee in moderately active amputees: A multi-centric randomized crossover trial. Ann Phys Rehabil Med, 2018; (61): 278–285. doi: 10.1016/j.rehab.2018.04.003. PMID: 29753888
- Wetz HH, Hafkemeyer U, Drerup B. Einfluss des C‑Leg-Kniegelenk-Passteiles der Fa. Otto Bock auf die Versorgungsqualität Oberschenkelamputierter: Eine klinisch-biomechanische Studie zur Eingrenzung von Indikationskriterien. [The influence of the C‑Leg knee shin system of Otto Bock on the care of above-knee amputees: A clinical biomechanical study to define indications.] Orthopäde, 2005; 34 (4): 298–319. PMID: 15812621
- Miller WC, Speechley M, Deathe AB. The prevalence and risk factors of falling and fear of falling among lower extremity amputees. Arch Phys Med Rehabil, 2001; 82 (8): 1031–1037. PMID: 11494181
- Tinetti ME. Clinical practice. Preventing falls in elderly persons. N Engl J Med, 2003; 348 (1): 42–49. PMID: 12510042
- Kannenberg A, Zacharias B, Pröbsting E. Benefits of microprocessor-controlled prosthetic knees to limited community ambulators: Systematic review. J Rehabil Res Dev, 2014; 51 (10): 1469–1496. doi: 10.1682/JRRD.2014.05.0118
- Kannenberg A, Zacharias B, Pröbsting E. Zum Nutzen mikroprozessor-gesteuerter Prothesenkniegelenke bei eingeschränkten Außenbereichsgehern. Eine systematische Analyse der Literatur. Orthopädie Technik, 2015; 66 (2):18–29
- Kahle JT, Highsmith MJ, Hubbard SL. Comparison of non-microprocessor knee mechanism versus C‑Leg on prosthesis evaluation questionnaire, stumbles, falls, walking tests, stair descent, and knee preference. J Rehabil Res Dev, 2008; 45 (1): 1–14. PMID: 18566922
- Hafner BJ, Smith DG. Differences in function and safety between Medicare Functional Classification Level‑2 and ‑3 transfemoral amputees and influence of prosthetic knee joint control. J Rehabil Res Dev, 2009; 46 (3): 417–434. PMID: 19675993
- Wong K, Rheinstein J, Stern MA. Benefits for adults with transfemoral amputation and peripheral artery disease using microprocessor compared with nonmicroprocessor prosthetic knees. Arch Phys Med Rehabil, 2015; 94 (10): 804–810. doi: 10.1097/PHM.0000000000000265
- Kaufman KR, Bernhardt KA, Symms K. Functional assessment and satisfaction of transfemoral amputees with mobility(FASTK2): A clinical trial of microprocessor-controlled vs. non-microprocessor-controlled knees. Clin Biomech (Bristol, Avon), 2018; 58: 116–122. doi: 10.1016/j.clinbiomech.2018.07.012
- Lansade C, Vicaut E, Paysant J, Ménager D, Cristina MC, Braatz F, Domayer S, Perennou D, Chiesa G. Mobility and satisfaction with a microprocessor-controlled knee in moderately active amputees: A multi-centric randomized crossover trial. Ann Phys Rehabil Med, 2018; (61): 278–285. doi: 10.1016/j.rehab.2018.04.003. PMID: 29753888
- Hahn A, Lang M. Effects of mobility grade, age, and etiology on functional benefit and safety of subjects evaluated in more than 1200 C‑Leg trial fittings in Germany. J Prosthet Orthot, 2015; 27 (3): 86–95
- Hahn A, Lang M, Stuckert C. Analysis of clinically important factors on the performance of advanced hydraulic, microprocessor-controlled exo-prosthetic knee joints based on 899 trial fittings. Medicine (Baltimore), 2016; 95 (45): e5386. PMID:27828871
- Mileusnic MP, Hahn A, Reiter S. Effects of a Novel Microprocessor-Controlled Knee, Kenevo, on the Safety, Mobility, and Satisfaction of Lower-Activity Patients with Transfemoral Amputation. J Prosthet Orthot, 2017; 29 (4): 198–205
- Burnfield JM, Eberly VJ, Gronely JK, Perry J, Yule WJ, Mulroy SJ. Impact of stance phase microprocessor-controlled knee prosthesis on ramp negotiation and community walking function in K2 level transfemoral amputees. Prosthet Orthot Int, 2012; 36 (1): 95–104
- Resnik L, Borgia M. Reliability of outcome measures for people with lower-limb amputations: Distinguishing true change from statistical error. Phys Ther, 2011; 91 (4): 555–565. PMID: 21310896. doi: 10.2522/ptj.20100287
- Dite W, Connor HJ, Curtis HC. Clinical identification of multiple fall risk early after unilateral transtibial amputation. Arch Phys Med Rehabil, 2007; 88 (1): 109–114. PMID: 17207685
- Hasenoehrl T, Schmalz T, Windhager R, Domayer S, Dana S, Ambrozy C, et al. Safety and function of a prototype microprocessor-controlled knee prosthesis for low active transfemoral amputees switching from a mechanic knee prosthesis: a pilot study. Disabil Rehabil Assist Technol, 2018; 13 (2): 157–165. PMID: 28399722. doi: 10.1080/17483107.2017.1300344
- Hahn A, Lang M. Effects of mobility grade, age, and etiology on functional benefit and safety of subjects evaluated in more than 1200 C‑Leg trial fittings in Germany. J Prosthet Orthot, 2015; 27 (3): 86–95
- Hahn A, Lang M, Stuckert C. Analysis of clinically important factors on the performance of advanced hydraulic, microprocessor-controlled exo-prosthetic knee joints based on 899 trial fittings. Medicine (Baltimore), 2016; 95 (45): e5386. PMID:27828871
- Hahn A, Lang M, Stuckert C. Analysis of clinically important factors on the performance of advanced hydraulic, microprocessor-controlled exo-prosthetic knee joints based on 899 trial fittings. Medicine (Baltimore), 2016; 95 (45): e5386. PMID:27828871
- Blumentritt S. Biomechanische Aspekte zur Indikation von Prothesenkniegelenken. Orthopädie Technik, 2004; 55 (6): 508–524
- Kannenberg A, Zacharias B, Pröbsting E. Benefits of microprocessor-controlled prosthetic knees to limited community ambulators: Systematic review. J Rehabil Res Dev, 2014; 51 (10): 1469–1496. doi: 10.1682/JRRD.2014.05.0118
- Kannenberg A, Zacharias B, Pröbsting E. Zum Nutzen mikroprozessor-gesteuerter Prothesenkniegelenke bei eingeschränkten Außenbereichsgehern. Eine systematische Analyse der Literatur. Orthopädie Technik, 2015; 66 (2):18–29
- Thiele J, Schöllig C, Bellmann M, Kraft M. Designs and performance of three new microprocessor-controlled knee joints. Biomed Tech (Berl), 2019; 64 (1):119–126. doi: 10.1515/bmt-2017–0053
- Bellmann M, Köhler TM, Schmalz T. Comparative biomechanical evaluation of two technologically different microprocessor-controlled prosthetic knee joints in safety-relevant daily-life situations. Biomed Tech (Berl), 2019; 64 (4): 407–420. doi: 10.1515/bmt-2018–0026
- Bellmann M, Schmalz T, Blumentritt S. Comparative biomechanical analysis of current microprocessor-controlled prosthetic knee joints. Arch Phys Med Rehabil, 2010; 91 (4): 644–652. PMID: 20382300
- Prinsen EC, Nederhand MJ, Olsman J, Rietman JS. Influence of a user-adaptive prosthetic knee on quality of life, balance confidence, and measures of mobility: a randomised cross-over trial. Clin Rehabil, 2015; 29 (6): 581–591. doi: 10.1177/0269215514552033
- Hafner BJ, Askew RL. Physical performance and self-report outcomes associated with use of passive, adaptive, and active prosthetic knees in persons with unilateral, transfemoral amputation: Randomized crossover trial. J Rehabil Res Dev 2015; 52 (6): 677–700
- Kuhlmann A, Krüger H, Seidinger S, Hahn A. Cost-effectiveness and budget impact of the microprocessor-controlled knee C‑Leg in transfemoral amputees with and without diabetes mellitus. Eur J Health Econ, 2020. doi: 10.1007/s10198-019–01138‑y [Epub ahead of print]
- Kannenberg A, Zacharias B, Pröbsting E. Benefits of microprocessor-controlled prosthetic knees to limited community ambulators: Systematic review. J Rehabil Res Dev, 2014; 51 (10): 1469–1496. doi: 10.1682/JRRD.2014.05.0118
- Kannenberg A, Zacharias B, Pröbsting E. Zum Nutzen mikroprozessor-gesteuerter Prothesenkniegelenke bei eingeschränkten Außenbereichsgehern. Eine systematische Analyse der Literatur. Orthopädie Technik, 2015; 66 (2):18–29
- Hahn A, Lang M. Effects of mobility grade, age, and etiology on functional benefit and safety of subjects evaluated in more than 1200 C‑Leg trial fittings in Germany. J Prosthet Orthot, 2015; 27 (3): 86–95
- Hahn A, Lang M, Stuckert C. Analysis of clinically important factors on the performance of advanced hydraulic, microprocessor-controlled exo-prosthetic knee joints based on 899 trial fittings. Medicine (Baltimore), 2016; 95 (45): e5386. PMID:27828871
- Kahle JT, Highsmith MJ, Hubbard SL. Comparison of non-microprocessor knee mechanism versus C‑Leg on prosthesis evaluation questionnaire, stumbles, falls, walking tests, stair descent, and knee preference. J Rehabil Res Dev, 2008; 45 (1): 1–14. PMID: 18566922
- Hafner BJ, Smith DG. Differences in function and safety between Medicare Functional Classification Level‑2 and ‑3 transfemoral amputees and influence of prosthetic knee joint control. J Rehabil Res Dev, 2009; 46 (3): 417–434. PMID: 19675993
- Kaufman KR, Bernhardt KA, Symms K. Functional assessment and satisfaction of transfemoral amputees with mobility (FASTK2): A clinical trial of microprocessor-controlled vs. non-microprocessor-controlled knees. Clin Biomech (Bristol, Avon), 2018; 58: 116–122. doi: 10.1016/j.clinbiomech.2018.07.012
- Mileusnic MP, Hahn A, Reiter S. Effects of a Novel Microprocessor-Controlled Knee, Kenevo, on the Safety, Mobility, and Satisfaction of Lower-Activity Patients with Transfemoral Amputation. J Prosthet Orthot, 2017; 29 (4): 198–205
- Hahn A, Lang M. Effects of mobility grade, age, and etiology on functional benefit and safety of subjects evaluated in more than 1200 C‑Leg trial fittings in Germany. J Prosthet Orthot, 2015; 27 (3): 86–95
- Hahn A, Lang M, Stuckert C. Analysis of clinically important factors on the performance of advanced hydraulic, microprocessor-controlled exo-prosthetic knee joints based on 899 trial fittings. Medicine (Baltimore), 2016; 95 (45): e5386. PMID:27828871
- Hahn A, Lang M, Stuckert C. Analysis of clinically important factors on the performance of advanced hydraulic, microprocessor-controlled exo-prosthetic knee joints based on 899 trial fittings. Medicine (Baltimore), 2016; 95 (45): e5386. PMID:27828871
- Hasenoehrl T, Schmalz T, Windhager R, Domayer S, Dana S, Ambrozy C, et al. Safety and function of a prototype microprocessor-controlled knee prosthesis for low active transfemoral amputees switching from a mechanic knee prosthesis: a pilot study. Disabil Rehabil Assist Technol, 2018; 13 (2): 157–165. PMID: 28399722. doi: 10.1080/17483107.2017.1300344
- Hahn A, Lang M. Effects of mobility grade, age, and etiology on functional benefit and safety of subjects evaluated in more than 1200 C‑Leg trial fittings in Germany. J Prosthet Orthot, 2015; 27 (3): 86–95
- Kannenberg A, Zacharias B, Pröbsting E. Benefits of microprocessor-controlled prosthetic knees to limited community ambulators: Systematic review. J Rehabil Res Dev, 2014; 51 (10): 1469–1496. doi: 10.1682/JRRD.2014.05.0118
- Kannenberg A, Zacharias B, Pröbsting E. Zum Nutzen mikroprozessor-gesteuerter Prothesenkniegelenke bei eingeschränkten Außenbereichsgehern. Eine systematische Analyse der Literatur. Orthopädie Technik, 2015; 66 (2):18–29
- Lansade C, Vicaut E, Paysant J, Ménager D, Cristina MC, Braatz F, Domayer S, Perennou D, Chiesa G. Mobility and satisfaction with a microprocessor-controlled knee in moderately active amputees: A multi-centric randomized crossover trial. Ann Phys Rehabil Med, 2018; (61): 278–285. doi: 10.1016/j.rehab.2018.04.003. PMID: 29753888
- Kaufman KR, Bernhardt KA, Symms K. Functional assessment and satisfaction of transfemoral amputees with mobility (FASTK2): A clinical trial of microprocessor-controlled vs. non-microprocessor-controlled knees. Clin Biomech (Bristol, Avon), 2018; 58: 116–122. doi: 10.1016/j.clinbiomech.2018.07.012
- Kaufman KR, Bernhardt KA, Symms K. Functional assessment and satisfaction of transfemoral amputees with mobility (FASTK2): A clinical trial of microprocessor-controlled vs. non-microprocessor-controlled knees. Clin Biomech (Bristol, Avon), 2018; 58: 116–122. doi: 10.1016/j.clinbiomech.2018.07.012
- Mileusnic MP, Hahn A, Reiter S. Effects of a Novel Microprocessor-Controlled Knee, Kenevo, on the Safety, Mobility, and Satisfaction of Lower-Activity Patients with Transfemoral Amputation. J Prosthet Orthot, 2017; 29 (4): 198–205
- Cutti AG, Lettieri E, Del Maestro M, Radaelli G, Luchetti M, Verni G, Masella C. Stratified cost-utility analysis of C‑Leg versus mechanical knees: Findings from an Italian sample of transfemoral amputees. Prosthet Orthot Int, 2017; 41 (3): 227–236. doi: 10.1177/0309364616637955
- Kuhlmann A, Krüger H, Seidinger S, Hahn A. Cost-effectiveness and budget impact of the microprocessor-controlled knee C‑Leg in transfemoral amputees with and without diabetes mellitus. Eur J Health Econ, 2020. doi: 10.1007/s10198- 019–01138‑y [Epub ahead of print]
- Lansade C, Vicaut E, Paysant J, Ménager D, Cristina MC, Braatz F, Domayer S, Perennou D, Chiesa G. Mobility and satisfaction with a microprocessor-controlled knee in moderately active amputees: A multi-centric randomized crossover trial. Ann Phys Rehabil Med, 2018; (61): 278–285. doi: 10.1016/j.rehab.2018.04.003. PMID: 29753888
- Kannenberg A, Zacharias B, Pröbsting E. Benefits of microprocessor-controlled prosthetic knees to limited community ambulators: Systematic review. J Rehabil Res Dev, 2014; 51 (10): 1469–1496. doi: 10.1682/JRRD.2014.05.0118
- Kannenberg A, Zacharias B, Pröbsting E. Zum Nutzen mikroprozessor-gesteuerter Prothesenkniegelenke bei eingeschränkten Außenbereichsgehern. Eine systematische Analyse der Literatur. Orthopädie Technik, 2015; 66 (2):18–29
- Hahn A, Lang M. Effects of mobility grade, age, and etiology on functional benefit and safety of subjects evaluated in more than 1200 C‑Leg trial fittings in Germany. J Prosthet Orthot, 2015; 27 (3): 86–95
- Hahn A, Lang M, Stuckert C. Analysis of clinically important factors on the performance of advanced hydraulic, microprocessor-controlled exo-prosthetic knee joints based on 899 trial fittings. Medicine (Baltimore), 2016; 95 (45): e5386. PMID:27828871
- Wurdeman SR, Stevens PM, Campbell JH. Mobility Analysis of AmpuTees II: Comorbidities and Mobility in Lower Limb Prosthesis Users. Am J Phys Med Rehabil, 2018; 97 (11): 782–788. doi: 10.1097/PHM.0000000000000967
- Kannenberg A, Zacharias B, Pröbsting E. Benefits of microprocessor-controlled prosthetic knees to limited community ambulators: Systematic review. J Rehabil Res Dev, 2014; 51 (10): 1469–1496. doi: 10.1682/JRRD.2014.05.0118
- Kannenberg A, Zacharias B, Pröbsting E. Zum Nutzen mikroprozessor-gesteuerter Prothesenkniegelenke bei eingeschränkten Außenbereichsgehern. Eine systematische Analyse der Literatur. Orthopädie Technik, 2015; 66 (2):18–29
- Kaufman KR, Bernhardt KA, Symms K. Functional assessment and satisfaction of transfemoral amputees with mobility (FASTK2): A clinical trial of microprocessor-controlled vs. non-microprocessor-controlled knees. Clin Biomech (Bristol, Avon), 2018; 58: 116–122. doi: 10.1016/j.clinbiomech.2018.07.012