Einleitung
Die größte Sorge der Patienten in der Phase vor einer anstehenden Operation ist die Angst vor den Schmerzen, die mit dem bevorstehenden Eingriff verbunden sein werden. Weiterhin ist eine suffiziente Analgesie essentiell, um die Gelenkbeweglichkeit und andere Outcome-Parameter zu optimieren. Dies war wohl auch einer der Gründe für die Aktion „Das schmerzfreie Krankenhaus“, die vor einigen Jahren initiiert wurde, wenngleich jedem klinisch Tätigen bewusst war, dass damit unerfüllbare Erwartungen geschürt wurden. Dennoch war es zweifellos wichtig, dass Ärzte sich intensiver mit diesen Sorgen der Patienten befassen, wie es etwa die Arbeit von Maier aus dem Jahr 2010 im Deutschen Ärzteblatt überaus deutlich zeigte 1. Die perioperative Schmerztherapie ist hierbei die ureigene Aufgabe der operierendenden Ortho-päden oder Unfallchirurgen; sie kann keinesfalls völlig den anderen Disziplinen alleine überlassen werden 2.
Gerade im Bereich der Gelenkchirurgie gibt es Maßnahmen wie den Fußblock 3 oder den Suprascapularisblock 4, die hervorragend vom Operateur eingesetzt werden können. Lange Zeit galt als optimale Form der postoperativen Schmerztherapie die Epiduralanästhesie oder periphere Nervenblockadeverfahren wie beispielsweise die Blockade des N. femoralis, des N. ischiadicus sowie des N. saphenus. Hiermit ist zwar das Ziel der Schmerzreduktion zu erreichen, dies geht jedoch einher mit einem sensomotorischen Kontrollverlust, was eine Mobilisation des Patienten deutlich erschwert. Im ungünstigsten Fall kommt es sogar zu Verletzungen aufgrund von Stürzen des Patienten bei fehlender motorischer Kontrolle der betroffenen Extremität.
Die lokale Infiltrationsanästhesie (LIA)
In diesem Umfeld hat sich die lokale Infiltrationsanästhesie (LIA) insbesondere im Bereich des Kniegelenkes etabliert. Diese Form der intraoperativen Schmerztherapie wird auch an der Schulter und am Hüftgelenk verwendet. Das Verfahren ist sicher, preisgünstig und erfordert einen deutlich geringeren technischen Aufwand und weniger Fertigkeiten als die oben genannten Verfahren.
In ihrer ursprünglichen Form 5 wurde die LIA als Wund- und Gelenkinfiltration mit Lokalanästhetikum und Adjuvantien beschrieben, wodurch die motorische Funktion der Extremität und damit die Mobilisationsfähigkeit des Patienten nicht beeinträchtigt werden sollte. Die Autoren stellten hierbei eine Multiinjektionstechnik sowie die Verwendung eines in das Kniegelenk perioperativ eingelegten Katheters vor, der postoperativ zu einer zusätzlichen Analgesie führen soll. Im Laufe der Zeit wurden die Technik sowie die verwendeten Substanzen von unterschiedlichen Autoren modifiziert. Bei den heute geläufigen Techniken werden weiterhin hochvolumige und zum Teil hochdosierte und langwirksame Lokalanästhetika in Kombination mit NSAR sowie Vasokonstriktoren verwendet. Gelegentlich werden auch Opioide oder Cortison mit hinzugegeben. Die Katheter werden intraartikulär oder auch nur als Wundkatheter angewendet.
Die ersten klinischen Studien hierzu zeigten sehr vielversprechende Ergebnisse 6 7. Die lokale Infiltrationsanästhesie erfolgt durch den Operateur selbst. Dieser infiltriert sukzessive verschiedene Bereiche (dorsale Kapsel, Seitenbänder, Ligamentum patellae und Subkutangewebe) in drei verschiedenen Portionen. Ein Katheter wird intraartikulär positioniert, der am Abend und am nächsten Tag mit einer weiteren Gabe des oben genannten Schmerzcocktails bestückt wird. Nach der morgendlichen Gabe wird der Katheter entfernt. Ein Kompressionsverband mit großflächiger Kühlung mit Kühlelementen für vier bis sechs Stunden verlängert die Analgesiedauer.
Ziel ist es, den Patienten früh zu mobilisieren. Nicht immer gelingt dies – wie in der Literatur dargestellt – schon nach drei bis fünf Stunden. In der Klinik des Verfassers wird das Verfahren seit 2015 angewendet. Die Erfahrungen zeigen, dass die Mobilisation durchaus zügiger erfolgen kann als mit anderen Formen der Anästhesie. Die Motorik ist nicht beeinträchtigt, sodass der Patient auch rasch das Knie aktiv belasten kann. In anderen Ländern erfolgt auch eine sehr frühzeitige Entlassung, teilweise schon am 2. postoperativen Tag 8. Dies ist innerhalb des deutschen Versorgungssystems jedoch nicht umsetzbar.
Durchführung einer LIA
Ablauf
Folgende Schritte werden bei einer LIA vollzogen:
- Es findet eine Infiltration von dorsaler Kapsel, Seitenbändern, Ligamentum patellae und des Subkutangewebes in drei verschiedenen Portionen statt.
- Ein Katheter wird intraartikulär positioniert, der am Abend und am nächsten Tag bestückt wird.
- Nach der morgendlichen Gabe wird der Katheter entfernt.
- Ein Kompressionsverband mit großflächiger Kühlung mit Kühlelementen für vier bis sechs Stunden verlängert die Analgesie-Dauer.
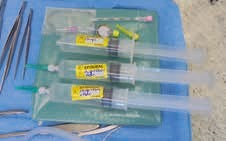
Infiltrierte Medikamente (Abb. 1)
Spritze 1 und 2 jeweils:
- 50 ml Ropivacain (Naropin) 2 mg/ml
- 0,25 ml Adrenalin 1 mg/ml
- 1 ml Parecoxib (Dynastat) 20 mg/ml
Spritze 3:
- 50 ml Ropivacain (Naropin) 2 mg/ml
- Einbringen des PDA-Katheters vor Wundverschluss in das Kniegelenk
Zeitpunkte der Infiltrationen
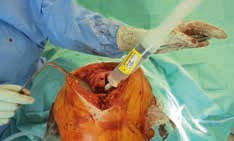
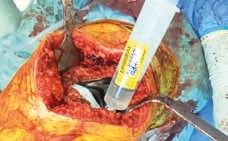
Spritze 1 (Abb. 2a u. b) vor Implantation der Prothese:
- Infiltration der hinteren Gelenkkapsel
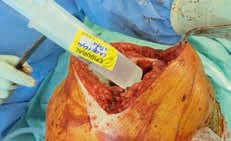
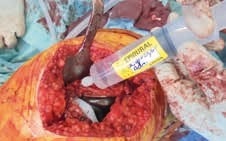
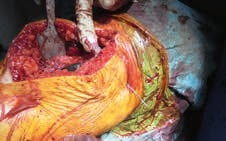
Spritze 2 (Abb. 3, 4) nach Implantation der Prothese:
- Infiltration der ventralen Kapsel, des Seitenbandapparates und des Streckapparates
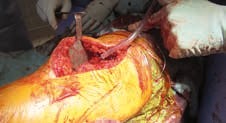
- Einbringen des Katheters (Abb. 5, 6)
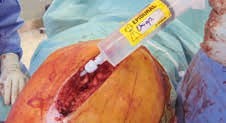
Spritze 3 (Abb. 7) vor Subkutannaht:
- Infiltration des Subkutangewebes
Am Morgen des 1. postoperativen Tages: 50 ml Ropivacain (Naropin) 2 mg/ml; anschließend wird der Katheter gezogen.
Studienlage
In nahezu allen Studien konnte gezeigt werden, dass die LIA gegenüber Placebo- oder Sham-Techniken überlegen ist. Eine Überlegenheit oder Gleichwertigkeit gegenüber den klassischen zentralen oder peripheren Nervenblockaden konnte bisher jedoch nicht belegt werden. Aufgrund der Inhomogenität der Studienbedingungen konnte bislang keine abschließende wissenschaftliche Bewertung abgegeben werden 9. Bezüglich der frühen postoperativen Mobilität (OP-Tag und erster postoperativer Tag) zeigen die meisten Erhebungen jedoch einen Vorteil der LIA bezüglich Kraft und Gehstrecke.
Für die Knieendoprothetik gibt es bereits eine umfangreiche Studienlage. Darunter finden sich mehrere prospektive epidemiologische Erhebungen 10 11 12. Daneben sind auch verschiedene randomisierte kontrollierte Studien publiziert; hierzu zählen fünf Studien im Vergleich zu einer Kontrollgruppe mit systemischer Analgesie 13 14 15 16 17, drei Studienvergleiche zu einer Nervus-femoralis-Blockade 18 19 20 sowie zwei Studienvergleiche zu einer Epiduralanalgesie 21 22. Die LIA zeigt in allen Studien eine signifikant verbesserte Analgesiequalität, die sich in einer höheren Patientenzufriedenheit und insbesondere in einer besseren Funktionalität des Gelenks auswirkt. Dieser Effekt ist in den ersten Tagen bis hin zu etwa drei Monaten nachweisbar. Nach sechs Monaten findet sich jedoch kein Unterschied zwischen den Gruppen mehr. In den Studien, in denen die Liegedauer ein besonderes Qualitätsmerkmal darstellt, scheint die LIA die Liegedauer zu verkürzen. Wundheilungsstörungen oder systemische Toxizität bzw. potenziell toxische Plasmakonzentration, bedingt durch die hohe Dosierung von Lokalanästhetika, wurden in keinem Fall beobachtet.
Die Studien, die die LIA mit der Femoralisblockade vergleichen, zeigen, dass die LIA sowohl die Schmerzen als auch die Rescue-Medikation und die Funktionalität in den ersten Tagen deutlich verbessert 23 24. Der Vergleich von LIA und Epiduralanästhesie 25 26 zeigt bessere Schmerzscores, eine bessere Rescue-Medikation und eine kürzere Krankenhausliegedauer in der LIA-Gruppe. Auch Teng et al. (2014) zeigten, dass die multimodale Medikamenteninjektion in der Knieendoprothetik sehr effektiv ist 27. Weiterhin ist es durchaus sinnvoll, eine LIA mit einer epiduralen Anästhesie zu kombinieren 28.
Fazit
Aufgrund der Frühmobilisation bei der LIA können Patienten prinzipiell früher entlassen werden. Ibrahim et al. (2013) ermittelten nach großen Knieeingriffen eine frühere Entlassung von bis zu 69 Stunden 29. Dies hat jedoch im deutschen System der DRGs (Diagnosis Related Groups) mit hoher Wahrscheinlichkeit keinen Effekt.
Der Autor:
Prof. Dr. med. Dr. h. c. Jörg Jerosch
Chefarzt der Klinik für Orthopädie,
Unfallchirurgie und Sportmedizin
Johanna-Etienne-Krankenhaus gGmbH
Am Hasenberg 46
41462 Neuss
j.jerosch@ak-neuss.de
Begutachteter Beitrag/reviewed paper
Jerosch J. Lokale Infiltrationsanästhesie (LIA). Orthopädie Technik, 2018; 69 (2): 50–52
- Entwicklung eines zum physiologischen Gangbild kongruenten polyzentrischen Knieorthesengelenks – Zwischenstand eines Forschungsprojektes — 10. April 2026
- Mikroprozessorgesteuerte stand- und schwungphasenkontrollierte Ganzbeinorthesen (SSCO): Entwicklung, Systeme und Versorgungsrealität in der orthopädietechnischen Praxis — 9. April 2026
- Gips oder Orthese bei distalen Radiusfrakturen? — 8. April 2026
- Maier C, Nestler N, Richter H, Hardinghaus W, Pogatzki-Zahn E, Zenz M, Osterbrink J. The quality of pain management in German hospitals. Dtsch Arztebl Int, 2010; 107 (36): 607–614. doi: 10.3238/ arztebl.2010.0607
- Jerosch J, Linke C. Patientenzentrierte Medizin in Orthopädie und Unfallchirurgie. Berlin/Heidelberg: Springer Verlag, 2016
- Jerosch,J, Heisel J. Operative Therapie von Fuß und Sprunggelenk. Köln: Deutscher Ärzteverlag, 2008
- Jerosch J, Saad M, Greig M, Filler T. Suprascapular nerve block as a method of preventive pain control in shoulder surgery. Knee Surg Sports Traumatol Arthrosc, 2008; 16: 602–607
- Kerr DR, Kohan L. Local infiltration analgesia: a technique for the control of acute postoperative pain following knee and hip surgery: a case study of 325 patients. Acta Orthop, 2008; 79 (2): 174–183. doi: 10.1080/17453670710014950
- Vendittoli PA, Makinen P, Drolet P, Lavigne M, Fallaha M, Guertin MC, Varin F. A multimodal analgesia protocol for total knee arthroplasty. A randomized, controlled study. J Bone Joint Surg Am, 2006; 88 (2): 282–289
- Busch CA, Shore BJ, Bhandari R, Ganapathy S, MacDonald SJ, Bourne RB, Rorabeck CH, McCalden RW. Efficacy of periarticular multimodal drug injection in total knee arthroplasty. A randomized trial. J Bone Joint Surg Am, 2006; 88 (5): 959–963
- Röstlund T, Kehlet H. High-dose local infiltration analgesia after hip and knee replacement – what is it, why does it work, and what are the future challenges? Acta Orthop, 2007; 78 (2): 159–161
- Andersen LØ, Kehlet H. Analgesic efficacy of local infiltration analgesia in hip and knee arthroplasty: a systematic review. Br J Anaesth, 2014; 113 (3): 360–374. doi: 10.1093/bja/aeu155
- Kerr DR, Kohan L. Local infiltration analgesia: a technique for the control of acute postoperative pain following knee and hip surgery: a case study of 325 patients. Acta Orthop, 2008; 79 (2): 174–183. doi: 10.1080/17453670710014950
- Peters CL, Shirley B, Erickson J. The effect of a new multimodal perioperative anesthetic regimen on postoperative pain, side effects, rehabilitation, and length of hospital stay after total joint arthroplasty. J Arthroplasty, 2006; 21 (6 Suppl 2): 132–138
- Andersen LØ, Gaarn-Larsen L, Kristensen BB, Husted H, Otte KS, Kehlet H. Subacute pain and function after fast-track hip and knee arthroplasty. Anaesthesia, 2009; 64 (5): 508–513. doi: 10.1111/j.1365– 2044.2008.05831.x.165
- Vendittoli PA, Makinen P, Drolet P, Lavigne M, Fallaha M, Guertin MC, Varin F. A multimodal analgesia protocol for total knee arthroplasty. A randomized, controlled study. J Bone Joint Surg Am, 2006; 88 (2): 282–289
- Busch CA, Shore BJ, Bhandari R, Ganapathy S, MacDonald SJ, Bourne RB, Rorabeck CH, McCalden RW. Efficacy of periarticular multimodal drug injection in total knee arthroplasty. A randomized trial. J Bone Joint Surg Am, 2006; 88 (5): 959–963
- Andersen LØ, Husted H, Otte KS, Kristensen BB, Kehlet H. High-volume infiltration analgesia in total knee arthroplasty: a randomized, double-blind, placebo-controlled trial. Acta Anaesthesiol Scand, 2008; 52 (10): 1331–1335. doi: 10.1111/j.1399–6576.2008.01777.x
- Essving P, Axelsson K, Kjellberg J, Wallgren O, Gupta A, Lundin A. Reduced morphine consumption and pain intensity with local infiltration analgesia (LIA) following total knee arthroplasty. Acta Orthop, 2010; 81 (3): 354–360. doi: 10.3109/17453674.2010.487241
- Essving P, Axelsson K, Kjellberg J, Wallgren O, Gupta A, Lundin A. Reduced hospital stay, morphine consumption, and pain intensity with local infiltration analgesia after unicompartmental knee arthroplasty. Acta Orthop, 2009; 80 (2): 213–219. doi: 10.3109/17453670902930008
- Parvataneni HK, Shah VP, Howard H, Cole N, Ranawat AS, Ranawat CS. Controlling pain after total hip and knee arthroplasty using a multimodal protocol with local periarticular injections: a prospective randomized study. J Arthroplasty, 2007; 22 (6 Suppl 2): 33–38
- Toftdahl K, Nikolajsen L, Haraldsted V, Madsen F, Tønnesen EK, Søballe K. Comparison of peri- and intraarticular analgesia with femoral nerve block after total knee arthroplasty: a randomized clinical trial. Acta Orthop, 2007; 78 (2): 172–179
- Carli F, Clemente A, Asenjo JF, Kim DJ, Mistraletti G, Gomarasca M, Morabito A, Tanzer M. Analgesia and functional outcome after total knee arthroplasty: periarticular infiltration vs continuous femoral nerve block. Br J Anaesth, 2010; 105 (2): 185–195. doi: 10.1093/bja/aeq112
- Andersen KV, Bak M, Christensen BV, Harazuk J, Pedersen NA, Søballe K. A randomized, controlled trial comparing local infiltration analgesia with epidural infusion for total knee arthroplasty. Acta Orthop, 2010; 81 (5): 606–610. doi: 10.3109/17453674.2010.519
- Spreng UJ, Dahl V, Hjall A, Fagerland MW, Ræder J. High-volume local infiltration analgesia combined with intravenous or local ketorolac+morphine compared with epidural analgesia after total knee arthroplasty. Br J Anaesth, 2010; 105 (5): 675–682. doi: 10.1093/bja/ aeq232
- Parvataneni HK, Shah VP, Howard H, Cole N, Ranawat AS, Ranawat CS. Controlling pain after total hip and knee arthroplasty using a multimodal protocol with local periarticular injections: a prospective randomized study. J Arthroplasty, 2007; 22 (6 Suppl 2): 33–38
- Toftdahl K, Nikolajsen L, Haraldsted V, Madsen F, Tønnesen EK, Søballe K. Comparison of peri- and intraarticular analgesia with femoral nerve block after total knee arthroplasty: a randomized clinical trial. Acta Orthop, 2007; 78 (2): 172–179
- Andersen KV, Bak M, Christensen BV, Harazuk J, Pedersen NA, Søballe K. A randomized, controlled trial comparing local infiltration analgesia with epidural infusion for total knee arthroplasty. Acta Orthop, 2010; 81 (5): 606–610. doi: 10.3109/17453674.2010.519
- Spreng UJ, Dahl V, Hjall A, Fagerland MW, Ræder J. High-volume local infiltration analgesia combined with intravenous or local ketorolac+morphine compared with epidural analgesia after total knee arthroplasty. Br J Anaesth, 2010; 105 (5): 675–682. doi: 10.1093/bja/ aeq232
- Teng Y, Jiang J, Chen S, Zhao L, Cui Z, Khan MS, Du W, Gao X, Wang J, Xia Y. Periarticular multimodal drug injection in total knee arthroplasty. Knee Surg Sports Traumatol Arthrosc, 2014; 22 (8): 1949–1957. doi: 10.1007/s00167-013‑2566‑0
- Tsukada S, Wakui M, Hoshino A. Postoperative epidural analgesia compared with intraoperative periarticular injection for pain control following total knee arthroplasty under spinal anesthesia: a randomized controlled trial. J Bone Joint Surg Am, 2014; 96 (17): 1433–1438. doi: 10.2106/JBJS.M.01098
- Ibrahim MS, Alazzawi S, Nizam I, Haddad FS. An evidence-based review of enhanced recovery interventions in knee replacement surgery. Ann R Coll Surg Engl, 2013; 95 (6): 386–389. doi: 10.1308/003588413X 13629960046435