Einleitung
Die infantile Zerebralparese (IZP) ist mit einer Prävalenz von etwa 2–3 Fällen pro 1000 Lebendgeburten die häufigste motorische Störung im Kindesalter1. Bei 85 % der Betroffenen treten spastische Lähmungen auf, die durch erhöhten Muskeltonus und gesteigerte Reflexaktivität charakterisiert sind2. Diese neurologischen Beeinträchtigungen wirken sich auf das muskuloskelettale System aus und führen zu Bewegungseinschränkungen, häufig distal betonter Muskelschwäche sowie ineffizienter motorischer Kontrolle3. Die unzureichende Muskeldehnung in den physiologischen Bereich begünstigt die Verkürzung der Muskulatur und die Entstehung von Kontrakturen, was die Mobilität zusätzlich einschränkt4.
Ein typisches Merkmal der IZP ist der Spitzfuß, der durch einen erhöhten Tonus der Plantarflexoren entsteht5. Dieser erhöhte Tonus führt zu einer frühzeitigen Aktivierung der Plantarflexoren in der terminalen Schwungphase sowie zu Beginn der Standphase6. In der Folge erfolgt der Initialkontakt mit dem Vorfuß, und eine Belastung der Ferse bleibt im weiteren Verlauf der Standphase aus. Durch die verkleinerte Unterstützungsfläche verringert sich die Stabilität beim Gehen. Zudem verläuft der Bodenkraftvektor unter dem Vorfuß und vor dem Kniegelenk, was zu einer Tendenz zur Überstreckung der Kniegelenke führt7. Die betonte Vorfußbelastung beim Gehen bewirkt sekundär eine übermäßige Biegebelastung des Mittelfußes8. Gibt der Fuß in der Sagittalebene nach, spricht man von einem „Durchbrechen“ des Fußes9. Spastische Faszikel arbeiten bei verkürzter Länge und werden dadurch möglicherweise vermehrt im aufsteigenden Abschnitt der Kraft-Längen-Kurve eingesetzt. In diesem Bereich ist die Fähigkeit zur aktiven Kraftentwicklung typischerweise reduziert10.
Konservative Therapiemethoden wie Unterschenkelorthesen zielen darauf ab, den Muskeltonus zu reduzieren und den Bewegungsumfang zu verbessern, indem die Plantarflexoren passiv gedehnt werden. Eine gängige Behandlungsmethode ist die vorübergehende Ruhigstellung der gestreckten Wade mithilfe von Gipsverbänden oder Orthesen11. Das Halten der Gelenke nahe der maximalen Streckstellung über mehrere Stunden täglich über einen Zeitraum von mehreren Wochen kann das Fortschreiten von Kontrakturen verhindern und das Gangbild verbessern12. Darüber hinaus wird angenommen, dass passives Dehnen eine Verringerung der Spastizität bewirken kann13. Orthesen begrenzen die Plantarflexion und besitzen eine dorsale Auflage. Zusätzlich kann eine Feder, die über Nacht eingesetzt wird, die Dehnungswirkung verstärken (Abb. 1). Ein entscheidender Aspekt ist, dass die Ferse gut in der Orthese gefasst wird, beispielsweise durch eine ringförmige Fußfassung, um ein Abheben der Ferse zu vermeiden. Andernfalls würde statt der Wade der Mittelfußbereich gedehnt. Durch sukzessive Korrektur und konsequente Tragezeiten von über 6 Stunden pro Tag sowie eine Gesamtdauer von mehr als 3 Monaten kann der Sohlenwinkel bei Barfußbelastung verbessert und ein normaler Fersenkontakt beim Initialkontakt erreicht werden14 15.
Darüber hinaus können passives Dehnen und längere Tragezeiten morphologische Anpassungen fördern, wie die Verlängerung der Achillessehne, die Anpassung des Muskelbauches sowie die Verlängerung der Faszikellänge, ohne die Muskulatur zu schwächen16. Der Einfluss auf die Tonusregulation während des Gehens wurde bislang unseres Wissens nach noch nicht untersucht.
Ziel dieser Studie ist es daher, die Effekte einer langfristigen orthesenbasierten Dehnung der Plantarflexoren auf deren Aktivitätsprofil zu analysieren. Es wird angenommen, dass bei ausreichender Tragedauer von mindestens 6 Stunden täglich über einen Zeitraum von 3 Monaten die Dehnreize durch Orthesen die pathologisch erhöhte Aktivität der Plantarflexoren in der terminalen Schwungphase und zu Beginn der Standphase reduzieren können.
Methodik
Patienten: Kinder im Alter von 5 bis 14 Jahren mit CP, GMFCS I–II und Spitzfußdeformität wurden nacheinander in die Studie einbezogen, wenn sie mindestens 3 Monate lang mit einer Unterschenkelorthese versorgt wurden (Abb. 1). Die Patienten und ihre Eltern wurden über die Studie informiert und gaben ihr schriftliches Einverständnis, wie von der Ethikkommission der Technischen Universität München genehmigt (4/18S).
Orthesenversorgung: Eine individuell angefertigte Unterschenkelorthese mit 2 modularen Komponenten nach dem Design von Baise und Pohlig17 wurde zur Behandlung der Spitzfußdeformität eingesetzt (Abb. 1). Die Unterschenkelschale mit Kondylenstütze wird durch einen vorderen Klettverschluss gesichert. Die zirkuläre Fußschale, die über ein Gelenk (F1734; Ottobock GmbH & Co. KG, Duderstadt, Deutschland) mit der Unterschenkelschale verbunden ist, reponiert das Subtalargelenk bei Knick- oder Klumpfuß in die Neutralstellung und verhindert ein Abrutschen des Rückfußes. Die Plantarflexion wurde eingeschränkt, während die Beweglichkeit in Dorsalflexion auf 5–10° begrenzt wurde.
Die Teilnehmer wurden angehalten, die Orthese gemäß Tardieu et al. 18 während des Schlafens mindestens 6 Stunden pro Nacht zu tragen. Bei einer passiven Dorsalflexion von weniger als 5° gegenüber der Neutralstellung wurde zusätzlich eine verlängerte Nutzung tagsüber empfohlen, sodass die Tragedauer auf bis zu 23 Stunden pro Tag ausgeweitet werden konnte. Einlagen und Fußorthesen sorgten tagsüber für die korrekte Ausrichtung des Subtalargelenks. Kinder mit einem positiven Silfverskjöld-Test trugen eine zusätzliche Oberschenkelschale während des Schlafens, um die Kniestreckung sicherzustellen und den M. gastrocnemius zu dehnen. Die tatsächliche Tragedauer wurde mittels eines Temperatursensors (Orthotimer, Rollerwerk-Medical, Balingen, Deutschland) über 3 Monate mit einer Aufnahmefrequenz von 15 Minuten gemessen. Dabei zeigte sich, dass nur 47 % der Kinder die empfohlene Tragezeit einhielten. Es wurde eine signifikante Korrelation zwischen der Tragedauer und der Dorsalextension beim Gehen festgestellt: Erst ab einer Tragezeit von über 6 Stunden pro Tag konnte eine statistisch signifikante Verbesserung der Dorsalextension um 2,3° ± 3,1° erreicht werden19.
Messungen: Vor und nach dem 3‑monatigen Behandlungszeitraum wurde eine instrumentierte 3D-Ganganalyse mit einem 8‑Kamera-System (200 Hz, Vicon Motion Systems Ltd., Oxford, UK) mit 2 Kraftmessplatten (1000 Hz, AMTI, Watertown/MA, USA), auf einer 13 Meter langen Gehstrecke durchgeführt. Reflektierende Marker wurden entsprechend einem modifizierten Plug-in-Gait-Modell20 und dem Oxford Foot Model21 an spezifischen anatomischen Landmarken platziert. Die Oberflächen-EMG-Messung des medialen M. gastrocnemius und des M. soleus erfolgte gemäß den Seniam-Richtlinien22 mithilfe eines DTS-Systems (Noraxon Inc., Scottsdale, USA). Die Kinder gingen barfuß in ihrer bevorzugten Geschwindigkeit. Es wurden 5 gültige Gehversuche aufgezeichnet, bei denen der Fußkontakt auf den Kraftmessplatten erfolgreich erfasst wurde. Zusätzlich wurde die Kraft der Plantarflexoren im Sitzen mit gestrecktem Knie während einer maximalen willkürlichen Kontraktion (MVC) mithilfe eines handgehaltenen Dynamometers (Mobie, SAKAImed, Tokyo, Japan) gemessen. Der Ablauf und die Inhalte der Messungen sind in Abbildung 2 dargestellt.
Datenauswertung und Statistik: Die Markertrajektorien wurde mithilfe eines quintischen Spline-Algorithmus (Woltring) mit einer mittleren quadratischen Fehlergrenze von 12 gefiltert. Die Rohdaten des EMG wurden mit einer Abtastrate von 1000 Hz erfasst und anschließend mit einem Butterworth-Bandpassfilter 4. Ordnung (20–400 Hz) zur Entfernung von Bewegungsartefakten und hochfrequentem Rauschen verarbeitet. Die gefilterten Signale wurden anschließend vollwellengleichgerichtet und mit einem Tiefpassfilter mit einer Grenzfrequenz von 10 Hz geglättet, um die lineare Hüllkurve zu erzeugen. Die EMG-Amplituden wurden auf die maximale willkürliche isometrische Kontraktion (MVC) normiert. Das integrierte EMG (IEMG) wurde über die einzelnen Gangphasen hinweg berechnet.
Um den Einfluss der tatsächlichen Tragedauer bei der Auswertung zu berücksichtigen, wurden die Teilnehmer in 2 Gruppen eingeteilt: eine Interventionsgruppe mit einer Tragedauer von 6 oder mehr Stunden und eine Kontrollgruppe mit einer Tragedauer von weniger als 6 Stunden pro Tag, wobei beide Gruppen die gleiche Indikation und identische Einschlusskriterien erfüllten. Die statistische Analyse wurde mittels zweifaktorieller ANOVA mit wiederholten Messungen über die Zeit durchgeführt.
Ergebnisse
Es wurden 41 Kinder in die Studie aufgenommen. Die Gründe für den Abbruch nach der ersten Messung waren zusätzlicher Behandlungsbedarf (n = 1), Nichtverfügbarkeit für die abschließende Messung (n = 5), Defekte des Temperatursensors (n = 3) sowie unbrauchbare EMG-Signale (n = 5). Somit lagen vollständige Daten zu Gang, klinischen Parametern, Temperatur und EMG für 27 Teilnehmer zu beiden Messzeitpunkten vor. Das Durchschnittsalter der Teilnehmer bei der ersten Messung betrug 10,7 Jahre (SD = 2,9).
15 Probanden hielten die empfohlene Tragedauer von mehr als 6 Stunden pro Tag ein und werden daher als konforme Gruppe (CPK) bezeichnet. 13 Probanden trugen die Orthesen weniger als 6 Stunden pro Tag und werden als nicht-konforme Gruppe (CPNK) bezeichnet. Die Eigenschaften beider Gruppen sind in Tabelle 1 dargestellt. Weitere Details zur Verteilung der Tragedauer zwischen Tag und Nacht finden sich bei Oestreich et al. 23.
Die Daten der klinischen Messungen zu Bewegungsausmaß, Kraft und Spastizität sind in Tabelle 2 aufgeführt. Das passive Bewegungsausmaß verbesserte sich signifikant um 2,7° ± 5,1° in der CPK-Gruppe und um 2,3° ± 4,2° in der CPNK-Gruppe (p = 0,049). Auch die maximale isometrische Kraft nahm signifikant zu (p = 0,036). Die Spastizität verringerte sich in beiden Gruppen leicht, jedoch nicht signifikant.
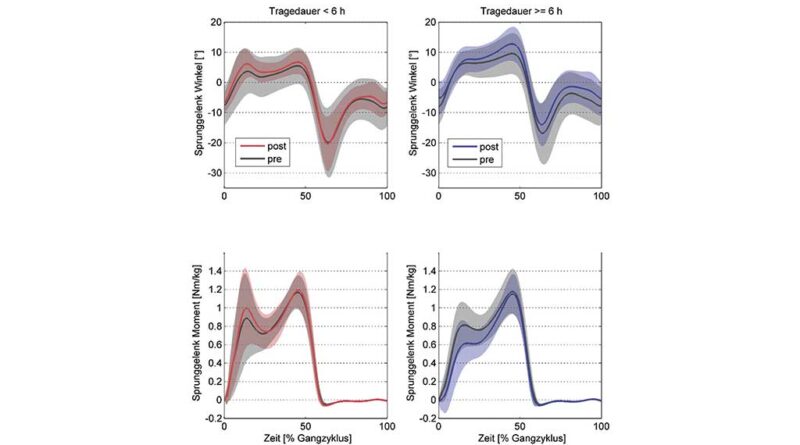
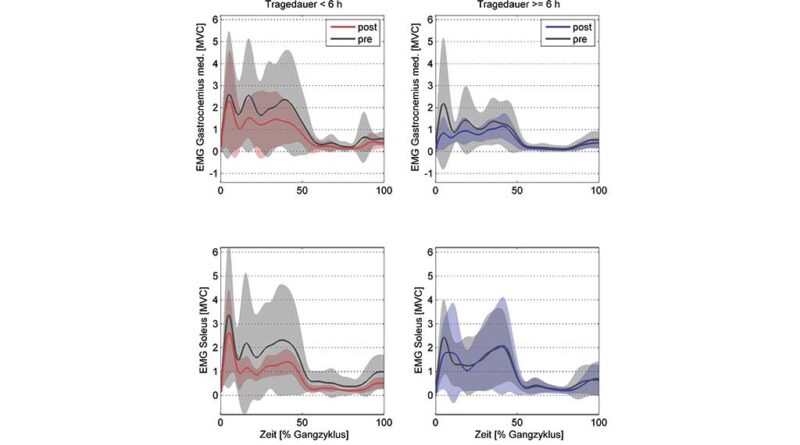
Die Daten der Ganganalyse sind in Tabelle 3 dargestellt, und die entsprechenden Kurven für den Gangzyklus sind in Abbildung 3 (Sprunggelenkswinkel und Momente) sowie Abbildung 4 (EMG) zu finden. Bei den Weg-Zeit-Parametern wurden keine signifikanten Unterschiede zwischen den Gruppen oder durch die Therapie festgestellt. Hinsichtlich der Dorsalextension im Sprunggelenk zeigte lediglich die CPK-Gruppe, die die Orthese mehr als 6 Stunden pro Tag trug, eine signifikante Verbesserung der maximalen Dorsalextension beim Initialkontakt und in der Schwungphase nach der Behandlung sowie eine signifikante Reduktion des Sprunggelenksmoments bei der Lastübernahme, wie der signifikante Interaktionseffekt zeigt. Das Maximum in der Standphase wurde in beiden Gruppen signifikant verbessert, jedoch ohne signifikanten Interaktionseffekt. Der Effekt in der CPK-Gruppe war mit einer Verbesserung von 3,0° ± 4,9° im Durchschnitt deutlich größer als der in der CPNK-Gruppe (0,5° ± 4,4°).
In beiden Gruppen zeigte das über die Schwungphase integrierte EMG eine signifikante Reduktion der Aktivität des M. gastrocnemius medialis (p = 0,048).
Diskussion
Wie erwartet verbesserte das Tragen von Orthesen über mehr als 6 Stunden die aktive Dorsalextension beim Gehen und reduzierte die EMG-Aktivität während der Schwungphase. Allerdings war das IEMG nur für den M. gastrocnemius in der terminalen Schwungphase reduziert und nicht für den M. soleus und nicht zu Beginn der Standphase. Zudem zeigte die Kontrollgruppe CPNK mit einer geringeren Tragedauer als 6 Stunden ebenfalls eine Reduktion der Aktivität des M. gastrocnemius in der Schwungphase.
Die beobachteten Effekte in der Kontrollgruppe, wie die Verbesserungen der passiven Dorsalextension, der maximalen isometrischen Kraft und des integrierten EMG (IEMG), sind bemerkenswert, auch wenn sie sich weniger stark auf das Gangbild auswirkten als in der CPK-Gruppe. Ein möglicher Grund für diese positiven Veränderungen könnte die durchschnittliche Tragedauer der Orthesen von 3,9 ± 1,6 Stunden pro Tag in der Kontrollgruppe sein, die offenbar ausreichte, um Fortschritte in klinischen Messungen und im EMG zu erzielen. Allerdings traten signifikante Anpassungen im Gangbild, insbesondere eine Verminderung des Plantarflexionsmomentes zu Beginn der Standphase, erst bei längeren Tragezeiten von mehr als 6 Stunden auf.
In beiden Gruppen verbesserten sich das passive Bewegungsausmaß der Dorsalextension, die maximale isometrische Kraft sowie die maximale Dorsalextension während des Gehens. Auffällig war jedoch, dass nur in der CPK-Gruppe die muskuläre und gelenkbezogene Steifigkeit spürbar abnahm, was zu einem geringeren Plantarflexionsmoment während der Standphase führte (Abb. 3). Die CPNK-Gruppe hingegen zeigte nach der Therapie keinen vergleichbaren Effekt auf die Steifigkeit, was durch das nahezu unveränderte oder sogar leicht erhöhte Gelenkmoment während der Belastungsreaktion erkennbar wurde. Diese tiefgreifenderen Anpassungen in der CPK-Gruppe lassen sich wahrscheinlich auf die längere und konsistentere Dehnungsdauer zurückführen. Die Ergebnisse deuten darauf hin, dass eine nachhaltige Reduzierung der Muskelsteifigkeit, ein zentraler Faktor bei der Behandlung von Spastizität, eine kontinuierliche und ausreichend lange Intervention erfordert.
Die Ergebnisse zeigten eine reduzierte Aktivität des M. gastrocnemius in der terminalen Schwungphase, während beim M. soleus keine vergleichbare Veränderung beobachtet wurde. Ein möglicher Grund dafür könnte sein, dass Patienten mit IZP größere Schwierigkeiten bei der Kontrolle biartikulärer Muskeln haben als bei monoartikulären Muskeln24, da biartikuläre Muskeln häufiger von Spastizität betroffen sind25. Biartikuläre Muskeln wie der M. gastrocnemius, die an Bewegungen mehrerer Gelenke beteiligt sind, spielen eine zentrale Rolle bei grundlegenden motorischen Funktionen wie Stehen, Gehen und Laufen und passen sich stark an die veränderten Gangmuster bei CP an. Dehnen mittels Orthesen kann die Flexibilität über die von diesen Muskeln überspannten Gelenke hinweg verbessern und so zu einer Reduzierung der muskulären Hyperaktivität führen. Im Gegensatz dazu sind monoartikuläre Muskeln wie der M. soleus, die nur an einem Gelenk wirken und an einfacheren Bewegungsabläufen beteiligt sind, weniger stark von Spastizität betroffen. Dadurch ist auch das Potenzial für funktionelle Verbesserungen durch Dehnen in diesen Muskeln geringer.
Wie könnte der Mechanismus einer Tonussenkung aussehen? Chronisches Halten in verlängerter Position, wie es bei neuroorthopädischen Einlagen beschrieben wird, könnte über die Regulation von Muskelspindeln und Golgi-Sehnenorganen eine Tonussenkung bewirken26. Muskelspindeln reagieren auf Dehnung mit afferenten Signalen, die reflektorisch eine Kontraktion auslösen, um den Muskel zu schützen. Bei längerer Dehnung kann ihre Empfindlichkeit jedoch sinken, was zu einer reduzierten Reflexaktivität und somit zu einem geringeren Tonus führt. Golgi-Sehnenorgane reagieren auf erhöhte Spannung, indem sie hemmende Signale aussenden, die die Kontraktion des Muskels dämpfen. Eine dauerhafte Dehnung durch Fußorthesen könnte so über eine Anpassung der Muskelspindelsensitivität und der Reflexaktivität eine langfristige Tonussenkung bewirken.
Trotz der Immobilisierung durch die Orthesen und der damit verbundenen Muskelatrophie27 wurde eine Verbesserung der Kraft der Plantarflexoren gemessen. Ein möglicher Grund dafür könnte sein, dass die meisten Patienten in der Studie die Orthese hauptsächlich nachts trugen, während sie tagsüber ihre Muskeln beim Gehen aktiv nutzten und trainierten28. Der Kraftzuwachs könnte durch eine vermehrte Dorsalextension und eine verbesserte Kraft-Längen-Relation bedingt sein. Dies würde zu einem Kraftzuwachs bei gleicher Muskelaktivität führen, was die Normalisierung des EMG in Bezug auf das Maximalkraftpotenzial MVC beeinflussen könnte. Die Normierung auf das MVC ist unerlässlich, um EMG-Signale bei Wiederholungsmessungen zu vergleichen, da bei einer erneuten Verklebung Elektrodenposition und Hautwiderstand variieren können. Eine größere Kraft bei angenommen gleicher EMG-Aktivierung würde zu einer Normalisierung führen, die ein niedrigeres EMG-Signal zur Folge hätte. Dieser Mechanismus könnte den Kraftzuwachs durch die größere Muskeldehnung erklären, was auch zu einem niedrigeren EMG-Signal führte und in beiden Gruppen beobachtet wurde.
Die klinische Relevanz dieser Studie liegt in der Bestätigung der Wirksamkeit einer langfristigen orthesenbasierten Dehnung der Plantarflexoren bei Kindern mit IZP. Die Ergebnisse zeigen, dass eine konsequente Anwendung von Orthesen mit einer Tragedauer von mindestens 6 Stunden täglich signifikante Verbesserungen in der Gangmechanik, insbesondere in der Dorsalextension des Sprunggelenks und der Reduktion des Plantarflexionsmoments während der Standphase, bewirken kann. Dies könnte zu einer besseren Mobilität und funktionellen Unabhängigkeit für die betroffenen Kinder führen.
Limitierungen der Studie: Zwar wurde im Mittel eine Reduktion der Spastizität in der klinischen Messung beobachtet, diese war jedoch nicht signifikant. Im Gegensatz zu den instrumentellen Messungen der Kraft und der passiven Dorsalextension mittels Goniometer könnte die Einschätzung der Spastizität durch den Beobachter zu subjektiv gewesen sein, um die Effekte der Spitzfußbehandlung mit Orthesen zuverlässig nachzuweisen. Instrumentelle Spastizitätsmessungen hätten hier möglicherweise genauere Ergebnisse liefern können29. Zudem zeigte die EMG-Messung aufgrund der Dynamik und der Bewegungen des Muskelbauchs beim Impakt zu Beginn der Standphase eine hohe Variabilität zwischen den Probanden, während in der Schwungphase geringere Schwankungen auftraten (Abb. 4). Daher konnten zu Beginn der Behandlung keine signifikanten Änderungen nachgewiesen werden.
Fazit
Das EMG in der Schwungphase zeigte eine Reduktion bei den Patienten mit gastrocnemius-bedingtem Spitzfuß. Diese Verbesserung war sowohl auf die passive Dehnung als auch auf den Kraftzuwachs in beiden Gruppen zurückzuführen. Allerdings zeigte sich eine signifikante Verbesserung der Steifigkeit erst bei längeren Tragezeiten. Eine längere Tragedauer ermöglichte es, den Muskel während der Bewegung in der Schwungphase leichter zu dorsalextendieren, was zu einer deutlicheren Verbesserung des Gangbildes, insbesondere beim Initialkontakt und in der nachfolgenden Standphase, führte. Dieser Effekt war bei kürzerer Tragedauer weniger ausgeprägt.
Für die Autoren:
Prof. Dr. Harald Böhm
Behandlungszentrum Aschau GmbH
Bernauer Str. 18
83229 Aschau im Chiemgau
HAWK – Hochschule für angewandte Wissenschaft und Kunst Hildesheim/Holzminden/Göttingen
Fakultät Ingenieurwissenschaften und Gesundheit, Gesundheitscampus Göttingen
Hermann-Rein-Str. 2A
37075 Göttingen
harald.boehm@hawk.de
Begutachteter Beitrag/reviewed paper
Böhm H, Schönherr F, Oestreich C. Effekte einer orthetischen Langzeitbehandlung auf die Tonusregulation bei Kindern mit spastischem Spitzfuß. Orthopädie Technik, 2025; 76 (4): 46–53
Tab. 1 Probandeneigenschaften beider Gruppen mit unterschiedlicher Tragedauer (Td) pro Tag zum Zeitpunkt der ersten Messung vor der Intervention.
| Tragedauer (Td) | Td unter 6 h | Td ≥ 6 h |
|---|---|---|
| Anzahl (27) | 12 | 15 |
| Tragedauer (h) | 3,9 (1,6) | 8,6 (3,9) |
| Geschlecht (m/w) | 6/6 | 12/3 |
| Alter (Jahre) | 11,3 (3,1) | 10,3 (2,7) |
| GMFCS (I/II) | 7/5 | 9/6 |
| Uni/Bilateral | 6/6 | 7/8 |
| BMI (kg/m2) | 19,4 (3,9) | 18,5 (3,9) |
Tab. 2 Klinische Messungen in den Gruppen mit unterschiedlicher Tragedauer (Td) pro Tag; signifikante Unterschiede (p < 0,05) sind fett hervorgehoben.
| Tragedauer | Td unter 6 h | Td ≥ 6 h | ANOVA p‑Werte | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| pre | post | pre | post | Gruppe | Zeit | Interaktion | |||||||||
| Passive Dorsalextension (°) | -1,4 (6,7) | 0,9 (4.9) | 1,0 (3.9) | 3,7 (5.5) | 0,149 | 0,049 | 0,870 | ||||||||
| Maximale isometrische Kraft (N/kg) | 4,9 (1,1) | 5,5 (1,2) | 4,7 (1,2) | 5,0 (1,1) | 0,658 | 0,036 | 0,919 | ||||||||
| Spastik M. gastrocnemius (MAS) | 1,5 (0.5) | 1,3 (0,6) | 1,2 (0,6) | 1,1 (0.5) | 0,107 | 0,160 | 0,623 | ||||||||
| Spastik M. soleus (Knie 90°) (MAS) | 1,6 (0,6) | 1,2 (0,7) | 1,2 (0,7) | 1,1 (0,5) | 0,178 | 0,130 | 0,290 |
Tab. 3 Weg-Zeit-Parameter, Kinematik, Kinetik und integriertes EMG (IEMG) vor und nach Orthesenbehandlung in den beiden Gruppen mit unterschiedlicher Tragedauer (Td) pro Tag; signifikante Unterschiede (p < 0,05) sind fett hervorgehoben.
| Tragedauer | Td unter 6 h | Td ≥ 6 h | ANOVA p‑Werte | ||||
|---|---|---|---|---|---|---|---|
| pre | post | pre | post | Gruppe | Zeit | Interaktion | |
| Dimensionslose Geschwindigkeit | 0.40 (0,05) | 0,42 (0,04) | 0,43 (0,06) | 0,45 (0,04) | 0,082 | 0,060 | 0,704 |
| Dimensionslose Schrittlänge | 67,9 (8,6) | 70,1 (6,4) | 73,2 (5,3) | 73,8 (5,9) | 0,075 | 0,157 | 0,425 |
| Dimensionslose Kadenz | 0,58 (0,04) | 0,59 (0,03) | 0,58 (0,04) | 0,59 (0,03) | 0,917 | 0,153 | 0,730 |
| Sprunggelenk DF Initialkontakt (°) | -3,1 (3,9) | -3,1 (4,3) | -7,0 (5,1) | -3,5 (6,0) | 0,254 | 0,047 | 0,042 |
| Sprunggelenk DF max. Standphase (°) | 9,2 (5,0) | 9,7 (4,0) | 9,7 (4,1) | 12,7 (4,9) | 0,323 | 0,016 | 0,077 |
| Sprunggelenk DF max. Schwungphase (°) | -0,9 (4,7) | -1,1 (5,3) | -2,1 (5,4) | 1,8 (5,0) | 0,655 | 0,029 | 0,020 |
| Sprunggelenk Moment Lastübernahme (Nmm/kg) | 375 (298) | 400 (258) | 290 (172) | 159 (209) | 0,073 | 0,049 | 0,014 |
| IEMG soleus Lastübernahme | 86,2 (78,2) | 77,2 (46,2) | 73,9 (44,5) | 59,7 (52,7) | 0,420 | 0,364 | 0,838 |
| IEMG soleus terminale Schwungphase | 32,7 (29,0) | 19,0 (9,0) | 25,2 (26,2) | 24,9 (23,5) | 0,915 | 0,249 | 0,269 |
| IEMG gastroc. med. Lastübernahme | 79,8 (81,3) | 71,5 (71,7) | 63,9 (80,5) | 26,9 (20,0) | 0,138 | 0,212 | 0,426 |
| IEMG gastroc. med. terminale Schwungphase | 22,9 (14,6) | 17,0 (13,2) | 19,8 (14,4) | 14,9 (8,0) | 0,544 | 0,048 | 0,869 |
Quellenverzeichnis
- Entwicklung eines zum physiologischen Gangbild kongruenten polyzentrischen Knieorthesengelenks – Zwischenstand eines Forschungsprojektes — 10. April 2026
- Mikroprozessorgesteuerte stand- und schwungphasenkontrollierte Ganzbeinorthesen (SSCO): Entwicklung, Systeme und Versorgungsrealität in der orthopädietechnischen Praxis — 9. April 2026
- Gips oder Orthese bei distalen Radiusfrakturen? — 8. April 2026
- Oskoui M et al. An update on the prevalence of cerebral palsy: a systematic review and meta-analysis. Developmental Medicine and Child Neurology, 2013; 55 (6): 509–519. https://doi.org/10.1111/dmcn.12080
- Surveillance of cerebral palsy in Europe: a collaboration of cerebral palsy surveys and registers. Developmental Medicine and Child Neurology, 2001; 42 (12): 816–824. https://doi.org/10.1111/j.1469–8749.2000.tb00695.x
- Shortland A. Muscle deficits in cerebral palsy and early loss of mobility: can we learn something from our elders? Developmental Medicine and Child Neurology, 2009; 51 (4): 59–63. https://doi.org/10.1111/j.1469–8749.2009.03434.x
- Goldstein M, Harper DC. Management of cerebral palsy: equinus gait. Developmental Medicine and Child Neurology, 2001; 43 (8): 563–569. https://doi.org/10.1111/j.1469–8749.2001.tb00762.x
- Ross SA, Engsberg JR. Relation between spasticity and strength in individuals with spastic diplegic cerebral palsy. Developmental Medicine and Child Neurology, 2002; 44 (3): 148–157. https://doi.org/10.1111/j.1469–8749.2002.tb00778.x
- Lam WK et al. Biomechanical and electromyographic evaluation of ankle foot orthosis and dynamic ankle foot orthosis in spastic cerebral palsy. Gait & Posture, 2005; 22 (3): 189–197. https://doi.org/10.1016/j.gaitpost.2004.09.011
- Armand S, Decoulon G, Bonnefoy-Mazure A. Gait analysis in children with cerebral palsy. EFORT Open Reviews, 2016; 1 (12): 448–460. https://doi.org/10.1302/2058–5241.1.000052
- Dixon PC, Böhm B, Döderlein L. Ankle and midfoot kinetics during normal gait: A multi-segment approach. Journal of Biomechanics, 2012; 45 (6): 1011–1016 https://doi.org/10.1016/j.jbiomech.2012.01.001
- Maurer JD et al. A kinematic description of dynamic midfoot break in children using a multi-segment foot model. Gait & Posture, 2013; 38 (2): 287–292. https://doi.org/10.1016/j.gaitpost.2012.12.002
- Hösl M, Böhm H, Arampatzis A, Döderlein L. Effects of ankle–foot braces on medial gastrocnemius morphometrics and gait in children with cerebral palsy. Journal of Children’s Orthopaedics, 2015; 9 (3): 209–219. https://doi.org/10.1007/s11832-015‑0664‑x
- Hösl M, Böhm H, Arampatzis A, Döderlein L. Effects of ankle–foot braces on medial gastrocnemius morphometrics and gait in children with cerebral palsy. Journal of Children’s Orthopaedics, 2015; 9 (3): 209–219. https://doi.org/10.1007/s11832-015‑0664‑x
- Hösl M, Böhm H, Arampatzis A, Döderlein L. Effects of ankle–foot braces on medial gastrocnemius morphometrics and gait in children with cerebral palsy. Journal of Children’s Orthopaedics, 2015; 9 (3): 209–219. https://doi.org/10.1007/s11832-015‑0664‑x
- Pin T, Dyke P, Chan M. The effectiveness of passive stretching in children with cerebral palsy. Developmental Medicine and Child Neurology, 2006; 48 (10): 855–862. https://doi.org/10.1017/S0012162206001836
- Hösl M, Böhm H, Arampatzis A, Döderlein L. Effects of ankle–foot braces on medial gastrocnemius morphometrics and gait in children with cerebral palsy. Journal of Children’s Orthopaedics, 2015; 9 (3): 209–219. https://doi.org/10.1007/s11832-015‑0664‑x
- Pin T, Dyke P, Chan M. The effectiveness of passive stretching in children with cerebral palsy. Developmental Medicine and Child Neurology, 2006; 48 (10): 855–862. https://doi.org/10.1017/S0012162206001836
- Hösl M, Böhm H, Arampatzis A, Döderlein L. Effects of ankle–foot braces on medial gastrocnemius morphometrics and gait in children with cerebral palsy. Journal of Children’s Orthopaedics, 2015; 9 (3): 209–219. https://doi.org/10.1007/s11832-015‑0664‑x
- Baise MPK. Behandlung des reversiblen dynamischen Spitzfußes mittels Unterschenkelorthesen mit ringförmiger Fußfassung. Medizinisch-Orthopädische Technik, 2005; 3: 1–19
- Tardieu C, Lespargot A, Tabary C, Bret MD. For how long must the soleus muscle be stretched each day to prevent contracture? Developmental Medicine and Child Neurology, 1988; 30 (1): 3–10. https://doi.org/10.1111/j.1469–8749.1988.tb04720.x
- Oestreich C et al. Orthotic bracing to treat equinus in children with spastic cerebral palsy: recorded compliance and impact of wearing time. Gait & Posture, 2025; 118: 75–84. https://doi.org/10.1016/j.gaitpost.2025.01.034
- Stief F et al. Reliability and accuracy in three-dimensional gait analysis: a comparison of two lower body protocols. Journal of Applied Biomechanics, 2013; 29 (1): 105–111. https://doi.org/10.1123/jab.29.1.105
- Stebbins J et al. Repeatability of a model for measuring multi-segment foot kinematics in children, Gait & Posture, 2006; 23 (4): 401–410. https://doi.org/10.1016/j.gaitpost.2005.03.002
- Hermens HJ, Freriks B, Disselhorst-Klug C, Rau G. Development of recommendations for SEMG sensors and sensor placement procedures. Journal of Electromyography and Kinesiology, 2000; 10 (5): 361–374. https://doi.org/10.1016/S1050-6411(00)00027–4
- Oestreich C et al. Orthotic bracing to treat equinus in children with spastic cerebral palsy: recorded compliance and impact of wearing time. Gait & Posture, 2025; 118: 75–84. https://doi.org/10.1016/j.gaitpost.2025.01.034
- Prilutsky BI. Coordination of Two- and One-Joint Muscles: Functional Consequences and implications for Motor Control. Motor Control, 2000; 4 (1): 1–44. https://doi.org/10.1123/mcj.4.1.1
- Lampe R et al. MRT-measurements of muscle volumes of the lower extremities of youths with spastic hemiplegia caused by cerebral palsy, Brain and Development, 2006; 28 (8): 500–506. https://doi.org/10.1016/j.braindev.2006.02.009
- Sousa ASP, Silva A, Tavares JMRS. Biomechanical and neurophysiological mechanisms related to postural control and efficiency of movement: A review. Somatosensory and Motor Research, 2012; 29 (4): 131–143. https://doi.org/10.3109/08990220.2012.725680
- Hösl M, Böhm H, Arampatzis A, Döderlein L. Effects of ankle–foot braces on medial gastrocnemius morphometrics and gait in children with cerebral palsy. Journal of Children’s Orthopaedics, 2015; 9 (3): 209–219. https://doi.org/10.1007/s11832-015‑0664‑x
- Oestreich C et al. Orthotic bracing to treat equinus in children with spastic cerebral palsy: recorded compliance and impact of wearing time. Gait & Posture, 2025; 118: 75–84. https://doi.org/10.1016/j.gaitpost.2025.01.034
- Bar-On L et al. A clinical measurement to quantify spasticity in children with cerebral palsy by integration of multidimensional signals, Gait & Posture, 2013; 38 (1): 141–147. https://doi.org/10.1016/j.gaitpost.2012.11.003