Guter Schlaf ist ein hohes Gut für das psychische und physische Wohlbefinden. Je älter wir werden, desto störanfälliger wird unser circadianes System. Krankheiten, Beschwerden und Medikamente bringen zusätzliche Veränderungen. Umso verwunderlicher, dass die Schlafhygiene ein noch vernachlässigtes Pflegequalitätsmerkmal ist. Gerade in der geriatrischen und gerontopsychiatrischen Pflege spielt die Förderung vorhandener Ressourcen eine salutogenetische Rolle.
Einleitung
2,6 Mio. Menschen mit steigender Tendenz sind in Deutschland pflegebedürftig (Stand: 31.12.2013). Etwa 1,86 Mio. (71 %) davon leben in ihrer Häuslichkeit, ca. 764.000 (29 %) in stationären Pflegeeinrichtungen. Zwischen 2011 und 2013 erhöhte sich die Zahl der pflegebedürftigen Menschen um 5 %, für die folgenden Jahre 1 ist mit einem noch höheren Zuwachs zu rechnen.
Die Pflegequalität in Deutschland regeln die Richtlinien des GKV-Spitzenverbandes zur Begutachtung von Pflegebedürftigkeit nach dem XI. Buch des Sozialgesetzbuches und die Qualitätsprüfungen des Medizinischen Dienstes der Krankenkassen (MDK) für ambulante und stationäre Pflegeanbieter. Kriterien zur systematischen Erfassung der Nachtaktivitäten und Schlussfolgerungen bezüglich des Schlafverhaltens sind in den Begutachtungselementen bisher nicht integriert 2 3. Dieser Artikel möchte auf ein vernachlässigtes Analysefenster in der Pflege – die Nacht – aufmerksam machen und zeigen, dass technischer Fortschritt in der Pflege die menschliche Qualifikation der ganzheitlichen Interpretation von Beobachtungen ergänzen und verbessern kann.
Guter Schlaf gehört zu den wichtigsten Lebenselixieren, damit Körper und Seele sich erholen können. Dazu ist jedoch eine ausgewogene Nachtruhe erforderlich, die bei Menschen im höheren Lebensalter aufgrund eines veränderten Schlafbedürfnisses bzw. aufgrund kognitiver Veränderungen verloren gehen kann. Daher ist eine Fremdeinschätzung der Nachtruhe in Form technischer Unterstützung ein sinnvolles Assessmentinstrument.
Im Folgenden werden anhand von sechs Praxisbeispielen aus zwei stationären Pflegeeinrichtungen in Mittelfranken Interventionen eines technisch erweiterten Risikomanagements hinsichtlich Sturz, Dekubitus und Schlaf skizziert. Erstmals werden dabei die besonderen Sicherheits- und Schlafbedürfnisse von Menschen mit sehr hohem Unterstützungs- bzw. Pflegebedarf anhand objektiver Merkmale dargestellt, was entsprechende Schlussfolgerungen hinsichtlich der Förderung eines bedürfnisorientierten Versorgungssettings in der letzten Lebensphase erlaubt.
Der Schlaf im höheren Lebensalter
Schlaf wird als Zustand äußerer Ruhe bei Menschen bezeichnet. Während des Schlafs sind Vitalzeichen wie zum Beispiel Atmung, Puls oder Blutdruck zeitweise herabgesetzt und unterscheiden sich somit von den Werten im Wachzustand.
Beim Schlaf werden zwei übergeordnete Phasen unterschieden: der NonRapid-Eye-Movement-(NREM-)Schlaf, bei dem der Schlafende keine Bewegungen der Augen zeigt, und der Rapid-Eye-Movement-(REM-)Schlaf mit zum Teil lebhaften Augenbewegungen. Der NREM-Schlaf wird zudem in vier Stadien eingeteilt:
- Stadium 1: leichter Schlaf kurz nach dem Einschlafen. Die Muskelspannung wird reduziert, und das bewusste Wahrnehmen der Umgebung entschwindet langsam.
- Stadium 2: leichter Schlaf; dieses Schlafstadium wird im Laufe des Schlafs zunehmend länger. Die Augen sind in diesem Stadium ruhig und die Augenlider geschlossen. Der Muskeltonus hat sich gegenüber dem Wachsein deutlich verringert.
- Stadium 3: Übergang in den Tiefschlaf.
- Stadium 4: Tiefschlaf, die tiefste Schlafphase. Entsprechend desorientiert und verschlafen wirken Schläfer, die jetzt geweckt werden. Die Schlafstadien 3 und 4 werden auch zusammen als Tiefschlaf bezeichnet. Die Augen sind ganz ruhig, der Muskeltonus signalisiert tiefe Entspannung, der Blutdruck fällt ab, Atmung und Herzschlag werden langsamer.
In der Regel wird der NREM-Schlaf bei einem Schlafvorgang mehrmals von REM-Schlaf abgelöst. Der REM-Schlaf wird auch als Traumschlaf bezeichnet. Wird ein Schlafender aus diesem Stadium geweckt, berichtet er in 80 % der Fälle, geträumt zu haben. Schlafwandeln tritt dagegen nicht während des REM-Schlafes, sondern während der Tiefschlafphasen auf.
Während dem Tiefschlaf weitgehend die Aufgabe der physischen Regeneration zugeschrieben wird, scheint es so, dass der REM-Schlaf für die psychische Erholung notwendig ist. Viele Ergebnisse bestätigen Zusammenhänge zwischen REM-Schlaf, Gedächtnisfestigung und Stimmung. Der erwachsene Mensch verbringt ungefähr 20 % seiner Schlafzeit in diesem Stadium.
Schlafstörungen
Die jeweilige altersbedingt normale Schlafarchitektur kann durch unterschiedliche Ursachen gestört sein. Dazu gehören körperliche und psychische Erkrankungen, Umwelteinflüsse, Medikamente, Drogen, Alkohol, psychische Belastungen und genetisch bedingte Einflüsse. Typische Erkrankungen, die zu Schlafstörungen führen können, sind unter anderem Schilddrüsenkrankheiten, hormonelle Störungen, Herz-Kreislauf-Störungen, Nierenerkrankungen, Magen-Darm-Erkrankungen, Rheuma, Krebs, Hirnschäden, Epilepsie, Atemwegserkrankungen und Schmerzen unterschiedlicher Genese.
Etwa 70 bis 80 % der psychiatrisch erkrankten Patienten klagen über erhebliche Schlafstörungen. Zu den psychischen Krankheitsbildern, die häufig mit Schlafstörungen auftreten, gehören Depressionen, Schizophrenien, Angststörungen, Essstörungen, Stress und Demenzen. Umgekehrt entwickeln sich im Laufe einer körperlich bedingten Schlafstörung auch schwere depressive Verstimmungen, sodass es schwerfällt zu entscheiden, was Ursache und was Folge einer Schlafstörung ist 4 5 6.
Behandlung von Schlafstörungen bei Demenzkranken
Schlafstörungen bei Demenzkranken lassen sich nicht alleine mit Medikamenten behandeln. Medikamentöse schlafverbessernde Maßnahmen müssen mit einer Therapie der Demenz, mit einer Behandlung körperlicher oder psychischer Begleitkrankheiten und mit nichtmedikamentösen Verfahren verbunden werden. Folgende Therapieansätze haben sich dabei bewährt:
- Die Patienten werden am Tage aktiviert; der Schlaf tagsüber wird vermindert. Höchstens eine halbe Stunde Mittagschlaf ist erlaubt. Der Schlafdruck am Abend nimmt auf diese Weise zu, und der Nachtschlaf wird verbessert.
- Organische und psychische Begleiterkrankungen werden konsequent behandelt, um Störungen des Schlafes so weit wie möglich zu vermeiden.
- Schlafgestörte Patienten mit Demenz erhalten mit einem Licht-Therapie-Gerät tagsüber eine Bestrahlung mit hellem, weißem Licht. Diese Lichttherapie wirkt als Zeitgeber auf die innere Uhr und normalisiert die Schlaf-Wach-Funktion. Eine vergleichbar gute Wirkung haben regelmäßige Spaziergänge an der Sonne, bevorzugt nachmittags oder am frühen Abend. Sie vermindern frühabendliche Verwirrtheitszustände und ein zu frühes Zubettgehen.
- Zur Behandlung von Schlafstörungen bei älteren dementen Patienten sind von den klassischen Schlafmitteln vor allem Benzodiazepin bzw. Rezeptoragonisten geeignet. Sie wirken kurz und verhindern so einen unnötigen Schlafanstoß am Tage nach der abendlichen Einnahme. Bei Schlafstörungen, Unruhe und Erregungszuständen Demenzkranker haben auch niedrig dosiert verabreichte Neuroleptika einen hohen Stellenwert 7 8 9 10.
Eine besondere Lebensumwelt und Schlaf von Menschen mit schwerer Demenz
Seit 2006 wird in Deutschland über eine segregativ-spezialisierte Versorgungsform diskutiert. In einer sogenannten Pflegeoase leben 4 bis 8 Menschen mit schwerer Demenz und hohem Pflege- und Unterstützungsbedarf in einem Mehrpersonenraum zusammen. Eine Besonderheit ist die ständige Anwesenheit einer Pflegeperson innerhalb des Raumes und längere Liegezeiten der Pflegeoasenbewohner. Die Pflegenden können durch die ständige Präsenz auf Bedürfnisse nicht nur zeitnah, sondern auch personenindividuell reagieren. Wissenschaftliche Studien und eine „Expertengruppe Pflegeoase“ haben sich mit einer bestmöglichen Lebensqualität in der letzten Lebensphase beschäftigt, die von hoher Vulnerabilität, hohem Schutz- bzw. Sicherheitsbedürfnis und vollständiger Hilfsbedürftigkeit gekennzeichnet ist. Je weiter eine Demenzerkrankung voranschreitet, desto wichtiger wird der Einfluss einer an die individuellen Bedürfnisse, Ressourcen und Einschränkungen angepassten Umwelt für die Erhaltung von Kompetenzen und Lebensqualität der Betroffenen 11 12 13 14.
Etwa 40 % der an einer Alzheimer-Demenz erkrankten Menschen haben laut Städt 15 eine Schlafstörung. Bei einer ausgeprägten Schlafstörung kann es zu schweren Störungen des circadianen Rhythmus mit Tag-Nacht-Umkehr kommen. Kuhn und Rutenkröger 16 kommen in ihrer wissenschaftlich bedeutsamen ersten Beobachtung des Schlafverhaltens bei Menschen mit schwerster Demenz zu dem Ergebnis, dass viele Schlafstörungen und insgesamt extrem lange Ruhe- bzw. Schlafphasen aufgrund des „Verschwindens des Tag-Nacht-Rhythmus“ bis hin zu einer kompletten Fragmentierung des Schlafs mit zum Teil häufigen extrem kurzen Schläfchen und extrem kurzen Wachphasen für diese Personengruppe kennzeichnend ist.
Eine sogenannte qualitätsgeleitete Pflegeoase gibt es auch in einer der beiden untersuchten Praxiseinrichtungen, sodass die Untersuchung des Schlafes gerade bei dieser Personengruppe mit höchstem Hilfeanspruch und fehlender Kommunikation interessant war.
Pflegeunterstützende und technikbasierte Assessmentmethode
Es wird immer einfacher, körperliche Aktivitäten und Schlaf mit Hilfe technischer Geräte zu erfassen. Beim präventiven Gesundheitsmanagement und beim Sport werden die Analysemöglichkeiten der „Wearable-Technologien“ jüngerer Generationen gern genutzt, um das individuelle Trainings- und Fitnessprogramm zu überwachen. Schlaf, Aktivität und Vitalwerte sind die wichtigsten Indikatoren der täglichen Analyse. Im Hinblick auf Pflegerisiken und die Einhaltung des Medizinproduktegesetzes sind diese Geräte jedoch ungeeignet. Das technische System, das im Praxistest im Einsatz war – der Mobility Monitor des Herstellers Compliant Concept – hat folgende Funktionen:
- Eine Mobilitätsanalyse ermöglicht ein effizientes Assessment und eine gezieltere Planung der Pflegemaßnahmen, z. B. eine Verbesserung des Schlafverhaltens (Mobilitätsdaten).
- Hinzu kommt eine Dekubitusprophylaxe mit Immobilitätswarnung bei Ausbleiben hautentlastender Eigenbewegungen des Bewohners bzw. des Patienten (Immobilitätswarnung).
- Es erfolgt eine Sturzprophylaxe bei 360 Grad Bettausstiegswarnung (Bettausstiegsmodul).
Der Mobility Monitor
Der Mobility Monitor der Schweizer Medizintechnikfirma Compliant Concept ist ein elektronisches Analyse- und Informationssystem für das pflegerischmedizinische Management von dekubitus- und/oder sturzgefährdeten Personen im Krankenhaus oder im Pflege- bzw. Altenheim.
Es besteht aus einer Sensoreinheit und einem Bedienmodul (Abb. 1). Die Sensoreinheit wird unter der Matratze mittig auf dem Krankenhaus- oder Pflegebett platziert und per Kabel mit dem Bedienmodul verbunden. Das Bedienmodul wird über ein Netzteil mit Strom versorgt. Es kann an standardmäßige Lichtrufanlagen angeschlossen werden. Es kann Daten erfassen und speichern sowie auf einem USB-Stick abspeichern oder – in der „Wireless“-Version – auch kabellos an einen Computer übertragen. Das System wird bei jedem Personen- oder Bettenwechsel neu kalibriert. Einmal pro Jahr muss das System einer funktionstechnischen Kontrolle durch den Hersteller unterzogen werden.
In der Sensoreinheit befinden sich Sensoren, die Bewegungen einer im Bett befindlichen Person und die damit verbundenen Druckveränderungen erfassen und in elektronische Informationen umwandeln können. Diese Signale werden an das Bedienmodul weitergeleitet. Im Bedienmodul befindet sich eine elektronische Einheit, deren spezieller Software-Algorithmus Druckveränderungen permanent klassifiziert und diese in digital verwertbare Daten umwandelt und speichert. Dabei kann die Sensitivität der Erfassung für einen definierten Zeitraum (2‑, 4- oder 6‑stündlich) voreingestellt werden. Gleichzeitig kann das System Drucksteigerungen an den Betträndern erkennen, die typisch für Personen sind, die das Bett verlassen. Ist das System an die Lichtrufanlage angeschlossen, erfolgt – je nach Alarmeinstellung – bei Vorliegen von Bewegungsmangel oder beim Verlassen des Bettes ein entsprechender Alarm. Eine erfolgte Alarmierung kann vom Fachpersonal am Bedienmodul per Tastendruck quittiert werden; dies wird im System entsprechend gespeichert.
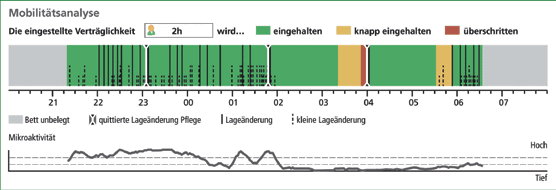
Sind die vom Bedienmodul erfassten Daten auf einen Computer übertragen worden, lassen sich diese mit einer speziellen Software – dem Mobility & Care Manager – darstellen, ausdrucken und später auswerten: die sogenannte Mobilitätsanalyse (Abb. 2). In ihr wird pro Person individuell dargestellt, ob und welche Bewegungen eine Person pro Zeitraum (z. B. im Laufe einer Nacht) ausgeführt hat. Dazu gehören hautentlastende Lageänderungen ebenso wie Mikroaktivität. Die Mobilitätsanalyse zeigt auch die vom Fachpersonal quittierten Alarme des Systems.
Einsatzmöglichkeiten in der Pflege
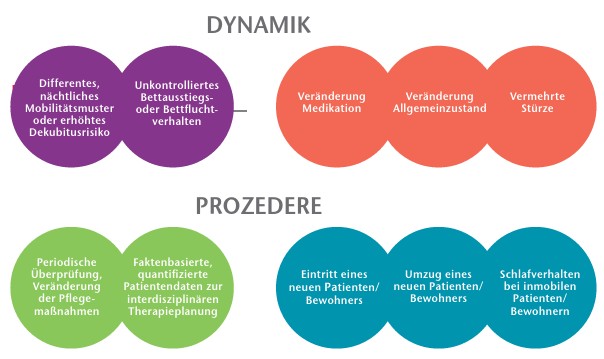
Der Mobility Monitor eignet sich als gezieltes periodisches und evaluierendes Beobachtungsinstrument, um die Lebensqualität des Bewohners bzw. des Patienten zu erhalten und dessen Pflegequalität zu sichern (Abb. 3). Steuerung, Koordination und Auswertung der technischen Daten übernahm im beschriebenen Beobachtungszeitraum die Pflegedienstleitung. Diese Aufgaben sind jedoch im regelmäßigen Einsatz vom Pflegeteam zu leisten.
Dynamische Prozesse:
- differentes nächtliches Mobilitätsmuster oder erhöhtes Dekubitusrisiko
- unkontrolliertes Bettausstiegs- und Bettfluchtverhalten
- Veränderung der Medikation
- Veränderung des Allgemeinzustandes
- vermehrte Stürze
Qualitätsgeleitete Prozesse:
- periodische Überprüfung und Veränderung von Pflegemaßnahmen
- faktenbasierte, quantifizierte Patientendaten zur interdisziplinären Therapieplanung
- Eintritt/Umzug eines neuen Bewohners/Patienten
- Schlafverhalten bei immobilen Bewohnern/Patienten
- Schlafverhalten bei Menschen mit schwerer Demenz/letzte Lebensphase
Praxisbeobachtungen und Fallbeispiele
Fall 1: Hildegard – Schmerzen unklarer Genese
Geboren 1949, Pflegestufe 1; Diagnose: Schizophrenie, normale Alterserscheinungen
Besonderheit: Die Bewohnerin wohnt aufgrund ihrer chronischen psychischen Erkrankung und fehlender Eigenfürsorge schon lange in einem Pflegeheim. In ihrem persönlichen Wahnsystem treten in der Anamnese immer wieder Schübe mit Schmerzsymptomatik unklarer Genese auf. Die Stimmung ist meist melancholisch.
Auffälligkeit: Seit einigen Wochen klagt die Bewohnerin über Schmerzen in der Hand und im Arm, kann den Schmerz aber nicht richtig benennen. Sie selbst sagt aus, dass sie schlecht schlafe, da die Schmerzen nachts stärker seien. Die Nachtschicht bestätigt eine vermehrte nächtliche Unruhe. Der zuständige Hausarzt und der hinzugezogene Neurologe erkennen keine Behandlungsoption und verweisen auf psychische Ursachen und die Anamnese.
Hypothese/fachliche Einschätzung der Pflegedienstleitung: Überprüfung der Nachtaktivität und Klärung des tatsächlichen Schlafverhaltens (1 Woche)
Analyse der Monitordaten: Die Bewohnerin kommt nicht in ausreichende Schlafphasen, sie zeigt eine hohe Mobilität (Drehen, Bewegen), es gibt keine Entspannungsphasen, sie wandert nachts.
Intervention: Besprechung mit dem Hausarzt, Ansetzen eines Schmerzmittels zur Nacht zur Probe
Dynamik: Nach einer Woche Testanalyse kommt es zu einer sichtbaren Verbesserung der Entspannungsphasen; die Bewohnerin berichtet über Entlastung und weniger Schmerzen. Darauf aufbauend erfolgen eine fachärztliche Abklärung der Schmerzen und eine Diagnosefeststellung der Arthrose. Eine medikamentöse und nichtmedikamentöse Therapie wird eingeleitet. Durch die objektive Beurteilung der technischen Daten wird die somatische Ursache differenzierbar.
Fall 2: Paula – vermehrte Stürze
Geboren 1932, Pflegestufe 2; Diagnose: Persönlichkeitsstörung, Diabetes mellitus, Epilepsie
Besonderheit: Die Bewohnerin ist seit Jahren unauffällig in ihrer psychischen Erkrankung, ihre Körperphysionomie hat sich verändert, sie hat ohne krankheitsbedingtem Hintergrund abgenommen.
Auffälligkeit: Es kommt zu häufigen Stürzen, beobachtet meist zwischen 17 und 18 Uhr. Seit einigen Monaten besteht ein physischer Abbauprozess, es kommt zu mehrfachen Krankenhausaufenthalten wegen Sturz und zur somatischen Ursachenuntersuchung ohne Befund, eine Vorstellung beim Neurologen ergibt keine weiteren Erkenntnisse.
Hypothese/fachliche Einschätzung der Pflegedienstleitung: Überprüfung der Mobilitätsdaten und des Schlafverhaltens, Veränderung der Medikation
Analyse der Monitordaten: Das Schlaf- und Mobilitätsverhalten zeigt große Unterschiede: Die Bewohnerin fällt am frühen Abend schnell in einen (zu) tiefen Schlaf, erkennbar an zu wenig Eigenbewegungen in der ersten Nachthälfte (18.30–24 Uhr); erst nach einer Erholungsphase von 3 bis 4 Stunden sind Eigenbewegungen wieder nachweislich sichtbar.
Intervention: Besprechung der Schlaf und Mobilitätsanalyse mit dem Neurologen mit Reduzierung/Adaption an verändertes Körpergewicht der Bedarfsmedikation (Seroquel) am Abend, Angebot des Mittagsschlafes für eine Erholungsphase am Tag (Verbesserung der Schlafhygiene)
Dynamik: Nach 5 Wochen und wiederholtem Einsatz der technischen Überwachung sind die Schlafphasen und das Mobilitätsmuster der Bewohnerin ausgewogener geworden. Aufgrund des körperlichen Abbaus war eine Medikationsanpassung am Abend notwendig, und auch der Mittagsschlaf wirkt sich förderlich auf die Allgemeinkonstitution aus. Die Bewohnerin verteilt ihre Ressourcen gleichmäßiger, die unkonzentrierte und sturzgefährdete Phase am Abend wurde abgewendet.
Fall 3: Anneliese – Medikamente, Sturz
Geboren 1929, Pflegestufe 3; Diagnose: fortgeschrittene Alzheimererkrankung, Hypertonie
Besonderheit: Die Bewohnerin ist neu in der Einrichtung, sie hat vorher zweimal die Pflegeeinrichtung gewechselt, weil eine fortlaufende Unruhe und herausforderndes Verhalten schnell zu Problemen führten. Sie ist sehr mobil, läuft viel hin und her, sucht die Nähe zu Mitbewohnern ohne natürliches Distanzverhalten. Sie ist in einem permanenten Erregungszustand mit wenig Entspannungsmomenten.
Auffälligkeit: Die hochdosierte Medikation (bis 8 mg Tavor, zusätzlich Quentiax) und eine zusätzliche Bedarfsmedikation zeigen keine unmittelbare Wirkung, d. h., je mehr Mittel gegeben wurden, desto unruhiger war die Bewohnerin. Es kommt zu Stürzen durch fehlende Konzentration und Unruhe.
Hypothese/fachliche Einschätzung der Pflegedienstleitung: Mobilitätsdaten und Schlafverhalten werden überprüft. Der Vorschlag der Pflegedienstleitung, die Medikation zur Beobachtung zu reduzieren, wird vom Pflegepersonal und vom Arzt abgelehnt.
Analyse der Monitordaten: Anhand der technischen Auswertung zeigt sich, dass die Bewohnerin extrem schlecht schläft, häufig wach und unruhig ist und das Bett kurzzeitig und oft verlässt. Die Einschlafphase nach der Abendmedikation ist sehr schwierig; die Bewohnerin gelangt in keine Durchschlafphase; damit fehlt dem Körper Erholung bzw. eine Muskelrelaxation.
Intervention: Schlaf- und Mobilitätsanalyse werden mit dem Neurologen und dem Pflegeteam besprochen. Es erfolgt eine gemeinsame Entscheidung für eine langsame Medikamentenreduktion (von 8 mg Tavor auf 3 mg, Senkung von Quentiax), eine Senkung der Bedarfsmedikation, die Planung einer ressourcenorientierten Tagesstruktur durch das sozialtherapeutische Team (nichtmedikamentöse Intervention) sowie die Einbeziehung in persönliche Einzelangebote durch Betreuungsassistenz, um die Schlafhygiene zu verbessern und den circadianen Rhythmus zu stärken.
Dynamik: Es kommt zu einem längeren Einsatz des Mobility Monitor. Anfangs gibt es nur wenig Verbesserung; das Pflegeteam befürchtet eine Verschlimmerung und benötigt immer wieder Motivation zur Geduld für die Medikamentenreduktion. Das feste Tagesangebot zeigt nach 3 Wochen Wirkung, die Bewohnerin reagiert besser, wacher und konzentrierter auf Ansprache bzw. Einbindung. Zugleich verändert sich auch das Schlafverhalten: Die Bewohnerin steht nachts fast nicht mehr auf (verringerte Nachtaktivität, verringerte Sturzgefahr). Die Einschlafphase wird gleichmäßig und die Durchschlafphase länger. Der Allgemeinzustand verbesserte sich spürbar. Die Angebote (Morgen- und Abendangebote) für den circadianen Schlaf-Wach-Rhythmus zeigten Wirkung für eine bessere Schlafhygiene.
Fall 4: Frieda – Dekubitusgefährdung und Mobilität
Geboren 1921, Pflegestufe 2; Diagnose: KHK, Arthrose, Presbyakusis, Demenz, Herzschrittmacher, Hypothyrose
Besonderheit: Die Bewohnerin sitzt aufgrund einer Arthrose im Rollstuhl.
Auffälligkeit: Die Braden-Skala zeigt 17 von 19 Punkten, demnach besteht für die Bewohnerin nur eine geringe Dekubitusgefährdung. Tatsächlich neigt sie jedoch zu Druckstellen. Es entsteht eine Fachkraftdiskussion über das eingesetzte Assessment und die daraus abzuleitenden Maßnahmen.
Hypothese/fachliche Einschätzung der Pflegedienstleitung: Es wird der Einsatz einer technischen Überwachung beschlossen, um mehr Informationen über das Mobilitäts- und Aktivitätsverhalten (Mikrobewegungen) der Bewohnerin im Bett zu erhalten.
Analyse der Monitordaten: Trotz vorhandener Bewegungsressourcen finden keine druckentlastenden Lagerungen über Mikroaktivitäten statt. Es fehlt die notwendige Eigenbewegung und damit auch eine von außen durchgeführte Lagerung, um das differente nächtliche Dekubitusrisiko zu vermeiden (Abb. 4).
Intervention: Aufnahme von Lagerungsintervallen (4 Stunden) durch Pflegende in die Pflegeplanung und Überprüfung durch den Mobility Monitor.
Dynamik: Laut Braden-Skala war die Bewohnerin nicht dekubitusgefährdet; durch die technische Aktivitätsanalyse wurde jedoch schnell deutlich, dass die Braden-Skala kein genaues Messmittel ist. Die fehlenden Eigenbewegungen waren für das Dekubitusrisiko verantwortlich. Nach bereits einer Woche konnte dank technischer Überwachung und veränderter Interventionsmaßnahme die Pflegequalität verbessert werden. Eine solche Überprüfung wäre mit menschlicher Beobachtung nicht möglich gewesen.
Fall 5:
a) Gerhard – Nachtaktivität, Dekubitus und Schlaf
Geboren 1927, Pflegestufe 3; Diagnose: Demenz, Hypertonie, massive Adipositas, Hirninfarkt – letzte Phase der Demenz
b) Horst – Nachtaktivität, Dekubitus und Schlaf
Geboren 1952, Pflegestufe 3; Diagnose: Alzheimer mit frühem Beginn, letzte Phase der Demenz
Besonderheit: Beide Bewohner leben in einer segregativ-spezialisierten Wohnform, der „Pflegeoase“, in einem Mehrpersonenraum, zusammen mit insgesamt 6 Bewohnern mit homogenen Kriterien. Es besteht Dauerpräsenz mindestens einer Pflegeperson im Raum zwischen 7 und 20 Uhr, ab 20 Uhr erfolgt die Betreuung durch die hausübergreifende Nachtschicht. In der Pflegeoase werden keine Bedarfsmedikamente zur Nacht gegeben.
Auffälligkeit: Beide Bewohner sind zu 100 % hilfebedürftig; aufgrund der fortgeschrittenen Demenzerkrankung verbringen sie viele Stunden im Bett, dabei besteht eine Störanfälligkeit des Tag-Nacht-Rhythmus. Sie sind schwer mobilisierbar, es ist keine eigene Aussage zur Befindlichkeit möglich.
Hypothese/fachliche Einschätzung der Pflegedienstleitung: Die Nachtschicht wurde in Bezug auf die Einhaltung der Pflegequalität, die Lagerungsintervalle und die Rundgänge überprüft. Die Nacht ist eine sogenannte Black Box bei dieser besonders vulnerablen Personengruppe. Die Möglichkeit der Information durch technische Überwachung vermittelt Einblick in Nachtruhephasen und Eigenbewegungen.
Analyse der Daten des Mobility Monitor: Es zeigt sich über viele Tage hintereinander, dass beide Männer genügend Eigenbewegungen und Mikroaktivitäten nachts aufbringen. Die Lagerungsintervalle durch das Pflegepersonal und damit die zusätzliche Störung des Schlafs sind deshalb nicht notwendig. Auffällig bei beiden Männern sind unruhige Zeiten zwischen 20 und 1 Uhr und zwischen 4 und 7 Uhr mit viel Eigenbewegung, leichten Schlafphasen und wenig Durchschlafphasen. Längere Tiefschlafphasen finden sich vermehrt am Tage.
Intervention: Die Lagerungsintervalle können über den Mobility Monitor aktiviert werden, d. h., das Immobilitätsmodul zeigt aktuell die Notwendigkeit einer Lagerung von außen an. Bei ausreichenden Eigenbewegungen muss der Bewohner nicht mehr im Schlaf gestört werden.
Dynamik: Gerade bei dieser besonderen Personengruppe ist mehr Wissen über den Schlaf und die Eigenbewegungen sinnvoll, um wirksame Pflegemaßnahmen am Tage einzuleiten und ggf. adäquat auf den Nachtverlauf zu reagieren.
Interessant ist bei der Beobachtung der beschriebenen Pflegeoasenbewohner die technische Aufzeichnung unruhiger Phasen bei Abwesenheit der Pflegeperson. Es ist zu vermuten, dass die Dauerpräsenz der Pflegeperson für Entspannung und Sicherheit bei dieser Personengruppe sorgt und deshalb zu tieferen Schlafphasen führt. Aus dieser Beobachtung eine weiterführende Untersuchung mit Hilfe technischer Assistenz zu Schlaf und Eigenbewegung von Menschen mit schwerer Demenz in unterschiedlichen Versorgungssettings anzustreben, würde die Arbeit von Berner, Kuhn und Rutenkröger aus dem Jahr (2011) 17 ergänzen. Kann eine bedürfnisorientierte Lebensumwelt mit Gemeinschaft, Nähe und Sicherheit zu verbesserten Schlafergebnissen bei Menschen mit Demenz und in ihrer letzten Lebensphase führen?
Fazit
„Ich habe die ganze Nacht kein Auge zugetan“ muss keine geläufige Floskel für Menschen im höheren Lebensalter sein. Vielmehr kann technische Unterstützung zur Fremdeinschätzung der Nachtruhe und Nachtaktivität in sinnvoller Weise die Pflegequalität ergänzen. Die Beobachtungen tragen zu einer verbesserten und ganzheitlichen Analyse bei. Die bisher fehlenden Informationen erlauben neue Interventionen und Pflegemaßnahmen und sind – wie in den dargestellten Fällen – immer geprägt von mehr Qualität für den Bewohner (weniger Medikation, weniger Störungen, Vermeidung von Risiken, gezielte Therapieplanung).
Nichtmedikamentöse Interventionen sind zu favorisieren; gerade die Black Box „Nacht“ kann durch Schlafentzug, Schlafstörungen, ungesunde Schlafphasen und den dadurch veränderten körperlichen und geistigen Gesamtzustand zu einer falschen Interpretation des Gesundheitszustands führen. Therapeutische Maßnahmen zur Stärkung des Tag-Nacht-Rhythmus und der Aktiv-/Passiv-Tagesstruktur, interdisziplinäre Gespräche über Krankheiten, Medikation und Wechselwirkungen können viel zu einer verbesserten Schlafhygiene und zur Erhöhung der Pflegequalität beitragen. Ökonomischer Vorteil technischer Unterstützung ist die Vermeidung einer Über- bzw. Unterversorgung; durch den Einsatz technischer Assistenz können Folgekosten von Komplikationen reduziert werden. Unsere menschlichen Ressourcen sind für die Überwachung des Schlafs nicht geeignet, sodass hier Technologien sinnvoll unterstützen und somit die Lebensqualität steigern können.
Für die Autorinnen:
Sabine L. Distler
Dipl.-Psychogerontologin, Dipl.-Sozialpädagogin (FH)
Curatorium Altern gestalten e. V.,
ALWO Unternehmensgruppe
Mühlenweg 5, 91235 Rupprechtstegen
Sabine.Distler@alterngestalten.de
Begutachteter Beitrag/reviewed paper
Distler S, Weiß C. Chancen technischer Assistenz beim Assessment von Sturz, Dekubitus und Schlaf im höheren Alter und bei Pflegebedürftigkeit — Ein Praxisbericht. Orthopädie Technik, 2016; 67 (9): 26–31
- Die orthopädietechnische Versorgung mit einer dynamischen Fingerstreckorthese als eigenständige Therapie bei der Dupuytren’schen Kontraktur — 26. März 2026
- Vergleichende Prüfung konventioneller und additiv gefertigter Prothesenschäfte in Anlehnung an DIN EN ISO 10328:2016 — 10. März 2026
- Easypreg – ein Faserverbundwerkstoff zum Tiefziehen — 9. März 2026
- Statistisches Bundesamt DESTATIS. Pflegestatistik 2013. Pflege im Rahmen der Pflegeversicherung. Deutschlandergebnisse. https://www.destatis.de/DE/Publikationen/Thematisch/Gesundheit/Pflege/PflegeDeutschlandergebnisse5224001139004.pdf?__blob=publicationFile (Zugriff am 17.07.2016)
- Bundesministerium für Gesundheit. Soziale Pflegeversicherung. Leistungsempfänger nach Leistungsarten und Pflegestufen im Jahresdurchschnitt 2014. http://www.bmg.bund.de/fileadmin/dateien/Downloads/Statistiken/Pflegeversicherung/Leistungsemfaenger_Art_Pflegestufen/Leistungsempfaengernach-Leistungsarten-und-Pflegestufen.pdf (Zugriff am 17.07.2016)
- Statistisches Bundesamt DESTATIS. Pflegestatistik 2013. Pflege im Rahmen der Pflegeversicherung. Deutschlandergebnisse. https://www.destatis.de/DE/Publikationen/Thematisch/Gesundheit/Pflege/PflegeDeutschlandergebnisse5224001139004.pdf?__blob=publicationFile (Zugriff am 17.07.2016)
- National Sleep Foundation. How much sleep do we really need? https://sleepfoundation.org/how-sleep-works/how-much-sleep-do-we-really-need (Zugriff am 17.07.2016)
- Müller T. Schlafgestoert.de. Ein Informationsangebot für alle, die mit Schlafstörungen/Schlafmedizin zutun haben. http://www.schlafgestoert.de/site‑1.html (Zugriff am 17.07.2016)
- Vaghela P, Sutin AR. Discrimination and sleep quality among older US adults: the mediating role of psychological distress. Sleep Health, 2016; 2 (2): 100–108
- Hajak G, Zulley J. Schlafstörungen bei Demenz: Ursachen und Behandlungsmöglichkeiten. Alzheimer-Info, 2001; 2: [o. S.]. https://www.deutsche-alzheimer.de/unser-service/archiv-alzheimer-info/schlafstoerungen.html (Zugriff am 17.07.2016)
- Figueiro MG, et al. Tailored lighting intervention for persons with dementia and caregivers living at homeSleep Health, 2015; 1 (4): 322–330
- Deutsche Gesellschaft für Schlafforschung und Schlafmedizin (DGSM), AG Geriatrie. Patientenratgeber Schlaf im Alter. 2011. http://www.dgsm. de/downloads/patienteninformationen/ratgeber/ DGSM%20Ratgeber%202015/Schlaf%20im%20 Alter%20DIN%20A4%20-%20PFADE.pdf (Zugriff am 17.07.2016). Schwalmstadt-Treysa
- Deutsche Gesellschaft für Schlafforschung und Schlafmedizin (DGSM). S3- Leitlinie Nicht erholsamer Schlaf /Schlafstörungen. Somnologie, 2009; 13: 4–160. http://www.dgsm.de/downloads/akkreditierung_ ergebnisqualitaet/S3-Leitlinie_Nicht_erholsamer_ Schlaf-Schlafstoerungen.pdf (Zugriff am 17.07.2016)
- Distler S, Schorr B. Pflegerefugium Vis-à-Vis. Pflegeethik in der Schwerstpflege anhand des Modellprojekts Vis-à-Vis. Zeitschrift für Gerontologie und Ethik, 2012; (3): 59–71
- Distler S. Wohnkonzepte für Menschen mit schwerer Demenz. In: Böning A et al. Praxisleitfaden für die stationäre Altenpflege. Checklisten, Formblätter, Textbausteine (Loseblattsammlung). 35. Ergänzungslieferung. Remagen: AOK Verlag, 2015: Anhang 1–16
- Städtler-Mach B, Worofka I. Wissenschaftliche Evaluation der Pflegeoase Vis-à-Vis im Senioren- und Pflegezentrum Rupprechtstegen. Abschlussbericht. Nürnberg: Evangelische Hochschule Nürnberg, 2012. http://www.evhn.de/index.php?binobj=file&cmd=passthru&oid=3797 (Zugriff am 17.07.2016)
- Berner R, Kuhn C, Rutenkröger A. Evaluation des Schlafverhaltens in einer Pflegeoase im Vergleich zum Doppel- und Einzelzimmer. Evaluationsmodul im Rahmen der wissenschaftlichen Begleitstudie in der Pflegeoase Altenzentrum St. Elisabeth Eislingen. Stuttgart: Demenz Support gGmbH, 2011. http://www.demenz-support.de/Repository/Evaluation_Schlafverhalten_01062012.pdf (Zugriff am 17.07.2016)
- Staedt J. Schlaf im Alter. In: Teising M, Drah LM, Gutzmann H et al. (Hrsg.). Alt und psychisch krank: Diagnostik, Therapie und Versorgungsstrukturen im Spannungsfeld von Ethik und Ressourcen. Stuttgart: Kohlhammer, 2007: 293–308
- Rutenkröger A, Kuhn C. Qualitätskriterien und Handlungsempfehlungen zur Implementierung einer Pflegeoase. In: Brandenburg H, Adam-Paffrath R (Hrsg.). Pflegeoasen in Deutschland, Forschungs- und handlungsrelevante Perspektiven zu einem Wohn- und Pflegekonzept für Menschen mit schwerer Demenz. Hannover: Schlütersche, 2013: 304–316
- Berner R, Kuhn C, Rutenkröger A. Evaluation des Schlafverhaltens in einer Pflegeoase im Vergleich zum Doppel- und Einzelzimmer. Evaluationsmodul im Rahmen der wissenschaftlichen Begleitstudie in der Pflegeoase Altenzentrum St. Elisabeth Eislingen. Stuttgart: Demenz Support gGmbH, 2011. http://www.demenz-support.de/Repository/Evaluation_Schlafverhalten_01062012.pdf (Zugriff am 17.07.2016)