Einleitung
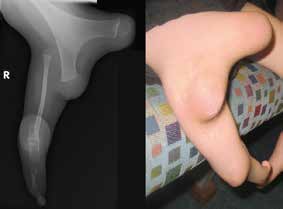
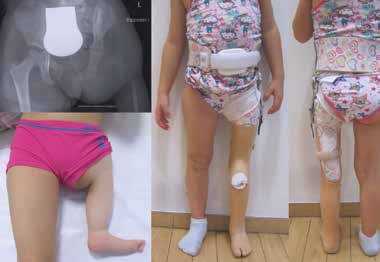
Unter angeborenen Gliedmaßendefekten sind unterschiedlich ausgeprägte Fehlanlagen der oberen und unteren Extremitäten zu verstehen, die sich bereits in der Embryonalentwicklung manifestieren und letztendlich in Abhängigkeit vom Schweregrad zu kosmetischen und funktionellen Beeinträchtigungen der Extremitäten führen können 1. Das Ausmaß einer angeborenen Fehlbildung beschränkt sich nicht immer auf eine Extremität bzw. einen Extremitätenabschnitt: Kombinierte Fehlbildungsformen wie z. B. das Femur-Fibula-Ulna-(FFU-)Syndrom oder das Tibia-Aplasie-Ektrodaktylie-Syndrom breiten sich gleichzeitig über mehrere Extremitätenabschnitte aus. Auch ein beidseitiges Auftreten sowie eine Vielzahl kombinierter syndromaler Erscheinungsformen der angeborenen Fehlbildung wie z. B. das Gollop-Wolfgang-Syndrom mit einhergehender klinisch auffälliger Bifurkation des Femurs (Abb. 1) und Ektrodaktylie an Hand oder Fuß erschweren das systematische Vorgehen in der Hilfsmittelversorgung. Assoziierte Anomalien treten sehr häufig auf und können vor allem bei den schwereren Fehlbildungsformen der unteren Extremitäten wie z. B. der Tibiaaplasie in über 70 Prozent der Fälle festgestellt werden 2. Die Prävalenz der angeborenen Gliedmaßenfehlbildungen ist mit 1,4/1.000 Fälle gering.
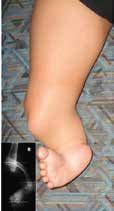
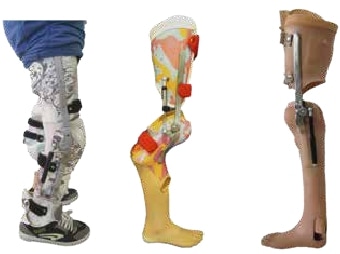
Während bei den Gliedmaßenfehlbildungen an den oberen Extremitäten transversale Defekte überwiegen, dominieren an den unteren Extremitäten longitudinale Fehlbildungen (Abb. 2). Bei den hochgradigen longitudinalen Fehlbildungen zeigt sich der Fibuladefekt am häufigsten (1,6 % aller Gliedmaßenfehlbildungen), gefolgt vom proximalen fokalen Femurdefekt (1,2 %) und von der Tibiaaplasie (1,0 %) 3. Während transversale Gliedmaßenfehlbildungen im klinischen Bild einer Amputation gleichen und daher – entsprechend den damit verbundenen Prinzipien – mit Prothesen behandelt werden 4, gestaltet sich die Versorgung longitudinaler Gliedmaßenfehlbildungen deutlich variantenreicher. Zum Einsatz kommen dabei bevorzugt Orthoprothesen, also ein Hilfsmittel, das sowohl orthetische als auch prothetische Konstruktionsmerkmale umfasst und einen Prothesenfuß sowie ggf. auch ein prothetisches Kniegelenk oder gar eine schaftähnliche Bettung aufweist. Begrifflich wurde die „Orthoprothese“ von Prof. Dr. Ernst Marquardt 5 6 in den späten 60er Jahren in die Hilfsmittelwelt eingeführt.
Das eindeutigste Abgrenzungsmerkmal zwischen Prothese und Orthoprothese besteht aus orthopädietechnischer Sicht darin, dass in eine orthoprothetische Konstruktion kein Stumpf (also auch kein angeborener Stumpf), sondern eine Gliedmaße aufgenommen wird. Wenngleich diese Gliedmaße auch in Länge und Volumen stark dezimiert sein kann oder Funktionseinheiten wie z. B. Hüftgelenk, Kniegelenk oder Sprunggelenke nicht regelhaft angelegt sein müssen, so sind doch fast immer Zehen‑, Fuß, Unterschenkel- und/oder Oberschenkelpartien an der fehlgebildeten Extremität vorhanden. Im Unterschied zu einem Prothesenschaft wird dabei also stets eine unterentwickelte longitudinale Extremität in die Orthoprothesenkonstruktion eingebettet.
Ziele der orthopädietechnischen Versorgung
Longitudinale Fehlbildungen an den unteren Extremitäten gehen mit den unterschiedlichsten Defiziten einher: Neben funktionalen Einschränkungen wie Bewegungseinschränkung in den Gelenken kommen disproportionale Entwicklungen, Malrotationen, deutliche Beinlängendifferenzen, eine reduzierte Kraftentfaltung und nicht zuletzt kompensatorische dynamische Effekte beim Gehen, z. B. das positive Trendelenburg- oder Duchenne-Zeichen, zum Ausdruck 7.
Die Versorgungsziele einer orthoprothetischen wie prothetischen Versorgung der fehlgebildeten unteren Extremität können wie folgt definiert werden:
- Erreichen, Erhaltung und Verbesserung der Steh- und Gehfähigkeit
- Stabilisierung der Extremität in bestmöglicher funktioneller und achsengerechter Position
- Verbesserung der Gelenkbeweglichkeit
- Erhaltung und Förderung maximaler Bewegungsumfänge
- Vermeidung progredienter Fehlstellungen
- Wiederherstellung des Körperbildes
- Förderung der Teilhabe am Alltagsleben sowie altersgerechte Entwicklung
Anforderungen an die Orthoprothesenversorgung, Aufbaukriterien, Passteile
Die Gestaltung der Orthoprothese hängt in entscheidendem Maße von der Höhe des Defektes sowie von den funktionalen klinischen Bedingungen und Möglichkeiten ab. Vor jeder Orthoprothesenversorgung müssen die klinischen Bedingungen wie Bewegungsumfänge, Muskelstatus, dreidimensionale Zuordnung der Extremität im Raum sowie mögliche Belastungssituationen angrenzender Gelenke und Muskeln abgeklärt werden. Neben den funktionellen Kriterien stellt vor allem die exakte Ermittlung der Längenverhältnisse zwischen der fehlgebildeten Extremität und der kontralateralen Beinseite eine wichtige Basis für die Auswahl der geeigneten Funktions- und Strukturteile dar 8 9. Die Konstruktion der Orthoprothese erfolgt vom Körper zum Boden, d. h., die spezifischen klinischen Besonderheiten und Möglichkeiten müssen beim Aufbau der Gesamtkonstruktion berücksichtigt werden. Selbstverständlich können im Orthoprothesenschaft Funktionalitäten wie Traktion und Achskorrekturen berücksichtigt werden. Diese sind jedoch im dreidimensionalen Aufbau der Versorgung nur dann erfolgreich umzusetzen, wenn sie nicht über das Ziel einer akzeptablen körperlichen Beeinflussung hinausschießen. Zu ehrgeizige Korrekturen der fehlgebildeten Extremität, die passiv unter Krafteinwirkung durchaus möglich sind, führen unweigerlich zum Versagen der Funktionalität.
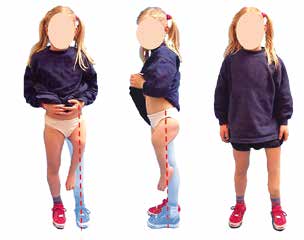
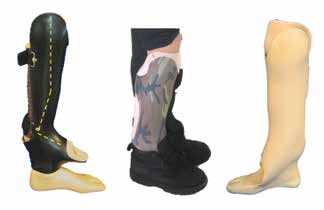
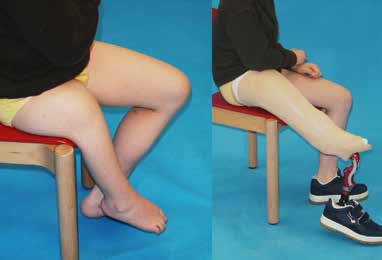
Für den Orthopädie-Techniker ist es daher bereits vor der Durchführung jeglicher Formabnahmen der fehlgebildeten Extremität wichtig zu wissen, in welcher Stellung das Bein bestmöglich mit dem funktionalen Aufbau der Orthoprothese korreliert (Abb. 3). Beim dreidimensionalen Aufbau einer Orthoprothese sind die biomechanischen Aufbaukriterien aus dem Prothesenbau anzuwenden und etwaige körperliche Abweichungen oder Dysfunktionalitäten angemessen zu berücksichtigen.
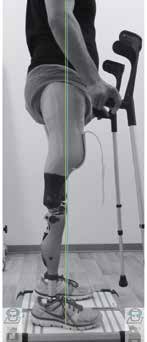
Neben dem dreidimensionalen Lotaufbau und der Messung der vertikalen Kraftlinien können im sensorisch deutlich komplexeren und erweiterten 3D L.A.S.A.R. Posture nun auch wertvolle Informationen über die auftretenden Horizontalkräfte und Torsionsmomente in die Betrachtungen einfließen 10. Gerade bei den komplexen Fehlstellungen der angeborenen Gliedmaßendefekte liefern die synchrone Messung und Darstellung des dreidimensionalen Kraftverlaufes sowie die Foto: ottobock Möglichkeit der visuellen Darstellung von Aufbaubezugslinien wertvolle Informationen zum Aufbau der Orthoprothesenversorgung (Abb. 4).
Die ausgewählten Passteile werden nach den Richtlinien und Vorgaben der Hersteller in den Aufbau eingeordnet und entsprechend berücksichtigt. Bei der Auswahl der an die Aktivität des Nutzers angepassten Passteile bewegt man sich bei den Orthoprothesen häufig in den Grenzbereichen des Möglichen. So scheiden oftmals hochfunktionale Passteile für entsprechende Anwender aufgrund zu geringer Aufbauhöhen oder mangelnder Adaptionsmöglichkeiten bei der Auswahl aus. Da Anwender mit angeborenen Fehlbildungen stellenweise über deutlich günstigere Hebelverhältnisse als Amputierte verfügen, kann es vorkommen, dass die für die Passteilauswahl notwendigen Herstellerangaben über das Anwendergewicht und den Aktivitätsgrad alleine nicht ausreichend sind. So können jugendliche Anwender mit angeborenen Femurdefekten Funktionsteile wie Kniegelenke und Prothesenfüße überfordern oder sogar zerstören, obwohl das für die Einstufung notwendige Aktivitätsprofil korrekt gewählt und das zugelassene Körpergewicht deutlich unterschritten wurde. Vor allem bei den oberschenkellangen Orthoprothesenversorgungen des Femurdefektes ist darauf zu achten, dass die Konstruktion im gebeugten Zustand keine Beschädigungen an den Funktionseinheiten der Passteile verursacht.
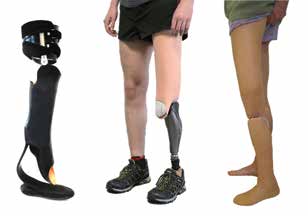
Für aktive Anwender sind energierückgebende Carbonfeder-Prothesenfüße und mikroprozessorgesteuerte Kniesysteme in besonderem Maße gefragt. Von entsprechenden Anwendern wird zumeist auch ein zweiteiliges Kosmetiksystem gefordert, da so jegliche Beeinträchtigung der Kosmetik auf die Funktionalität des Kniesystems ausgeschlossen werden kann (Abb. 5). Es empfiehlt sich in jedem Fall, den Funktionszugewinn derartiger Systeme mit dem Verordner und den Anwendern zu eruieren, die Funktionalitäten zu erproben und nach erfolgreicher Austestung gemeinsam mit dem Kostenträger adäquate Möglichkeiten der Kostenerstattung zu erörtern. Die kosmetische Gestaltung von Orthoprothesen nimmt für viele Betroffene einen wichtigen Stellenwert ein. Hierbei kommen neben dem Wunsch nach einem natürlichen Aussehen 11 oftmals auch funktionale Aspekte wie Wasserfestigkeit, das Tragen von offenem Schuhwerk oder gar von Flip-Flops u. v. m. zum Tragen.
Orthoprothetische Versorgung bei angeborenem Fibuladefekt
Der Fibuladefekt, auch „fibulärer Längsdefekt“ oder „Fibulahemimelie“ genannt, beschreibt das angeborene Fehlen von Teilen der Fibula bis hin zum kompletten Fehlen der Fibula, auch Fibulaaplasie genannt. Die gebräuchlichste Klassifikation wurde von Achterman und Kalamchi 12 im Jahre 1979 veröffentlicht. Sie unterscheidet drei Typen:
- Typ Ia: Hypoplasie der proximalen Fibula, beide Wachstumsfugen vorhanden, jedoch hypoplastisch, intakte Malleolengabel
- Typ Ib: Hypoplasie der Fibula mit dysplastischer oder fehlender Malleolengabel
- Typ II: komplettes Fehlen der Fibula (Fibulaaplasie)
Bei angeborenen Fibuladefekten können die folgenden klinischen Auffälligkeiten auftreten 13 14:
- Syndaktylien
- Minderstrahligkeit des Fußes, Fehlen der lateralen Strahlen
- talocalcaneare Synostosen
- Verkürzung der Tibia
- Beinlängendifferenz
- Antekurvation der Tibia
- Dimple-Bildung im Bereich der Antekurvation
- Innenrotation des Unterschenkels
- Instabilität der Kreuzbänder
- Knie: Achsabweichung im Valgussinne
- Hypoplasie der lateralen Femurkondyle
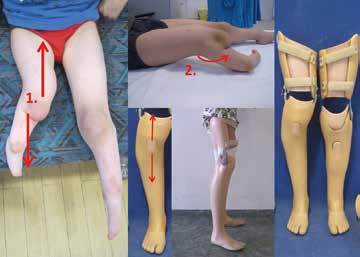
Die orthoprothetische Versorgung muss diesen klinischen Auffälligkeiten gerecht werden und wachstumslenkend jeglichen Verschlechterungen entgegenwirken. Für die Wahl der Orthoprothesenart und die dazugehörige Einbettung der Gliedmaße ist der weitere ärztliche Behandlungsplan entscheidend: Wie groß ist die zu erwartende Beinlängendifferenz zum Wachstumsabschluss? Kann die bestehende Beinlänge ausgeglichen werden? Wie stabil ist das Kniegelenk? Sind sonstige operative Maßnahmen angezeigt?
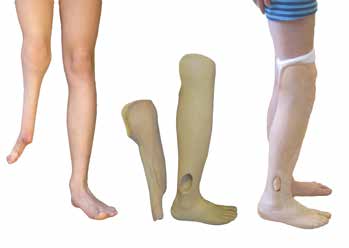
Wird ein Ausgleich der Beinlänge angestrebt – z. B. durch den Einsatz beinverlängernder Maßnahmen –, sollte der Fuß in der Orthoprothese in achsengerechter Position plantigrad eingestellt werden. Die in Verbindung mit dem untergebauten Prothesenfuß entstehende „Doppeldecker“-Orthoprothese (Abb. 6) kann ab einer Beinlängendifferenz von ca. 6 cm realisiert werden. Geringere Beinlängendifferenzen bis ca. 6 cm Längenausgleich werden durch Orthoprothesen in Spitzfußbettung mit begleitender Nachtlagerungs-Orthoprothese in plantigrader Fußeinstellung versorgt. Da Fibulaaplasien häufig mit einer Antecurvation in der Tibia einhergehen, ist darauf zu achten, dass die plantigrade 90°-Position im OSG zum distalen Anteil der Tibia eingestellt wird, da im Rahmen etwaiger operativer Verlängerungen in der Regel auch Korrekturen der Antekurvation erfolgen.
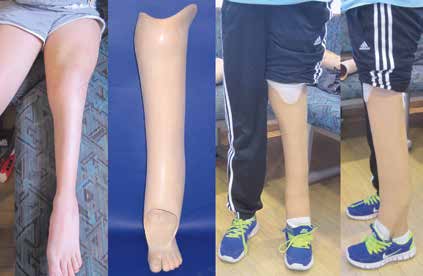
Haben operative Beinverlängerungen zum Wachstumsabschluss zu einer Angleichung der Beinlänge geführt, kann eine abschließende Definitivversorgung mit einer Silikon-Vorfußprothese erfolgen. Diese gleicht die fehlende Fußlänge und das fehlende Fußvolumen des zumeist minderstrahligen Fußes sowie ggf. noch bestehende Beinverkürzungen von bis zu 1,5 bis 2 cm aus und ermöglicht durch die elastische Vollkontaktbettung ein weitgehend physiologisches Abrollverhalten im Alltag. Das Tragen normaler Konfektionsschuhe muss hierbei als erstrebenswertes Therapieziel angesehen werden 15.
Fibuladefekte mit ausgeprägten Fehlformen und hohen Beinlängendefiziten werden bereits zu Beginn der Versorgung in einer kosmetisch ansprechenden Achsenposition der fehlgebildeten Gliedmaße eingebettet. Die Ausbildung einer Tibia-Antekurvation mit sichtbarem „Dimple“ („Grübchen“, Hauteinziehung) kann bei den hohen Fibuladefekten wie z. B. der Fibulaaplasie häufig beobachtet werden 16 17. Zur Vorbeugung progredienter Entwicklungen sollte die Einbettung des bereits antekurvierten Unterschenkels daher unbedingt eine zirkuläre formschlüssige Vollkontaktbettung mit integrierter Stabilisierung der antekurvierten Tibia aufweisen. Wird dies in der orthoprothetischen Versorgung nicht berücksichtigt, kann sich die Antekurvation im Zuge des Wachstums verstärken.
In Abhängigkeit von der oftmals beobachteten Valgus-Tendenz bzw. ‑Deformität im Kniegelenk muss bei der unterschenkellangen Orthoprothesenkonstruktion auch eine hohe Kondylenbettung der lateralen Femurkondyle in Erwägung gezogen werden. Der noch vorhandene und zumeist minderstrahlige Fuß der fehlgebildeten Gliedmaße sollte in der Konstruktion der Tibia in bestmöglicher achsengerechter Position unterstellt werden. Die kosmetische Gestaltung der Orthoprothese sollte stets die Beinform der kontralateralen Beinseite zum Ziel haben (Abb. 7). Etwaige aufgrund der Formabweichungen bestehende Inkongruenzen der Außenform sollten bei dieser Versorgungsart nicht ausgeglichen werden, da dies zu einem „plumpen“ äußeren Erscheinungsbild führt 18. Auch hier sollten stets konfektionierte normale Schuhe getragen werden können. Liegen abweichende Achsendeformitäten (Valgusfehlstellung) oder Instabilitäten im Kniegelenk (Kreuzbänder) vor, muss an eine begleitende Führung des Oberschenkels gedacht werden.
Die Orthoprothese wird dann oberschenkellang ausgeführt, wodurch einer progredienten Entwicklung Einhalt geboten wird. Bei grenzwertigen Versorgungsfällen kann die Oberhülse wahlweise adaptiv gestaltet werden und so z. B. beim Sport und bei anderen starken Beanspruchungen temporär getragen werden. Ergänzt werden diese Versorgungsvarianten oftmals durch korrigierende Nachtlagerungsorthesen mit dynamischen Korrektursystemen.
Orthoprothetische Versorgung bei angeborenem Tibiadefekt
Der Tibiadefekt zählt zu den selteneren angeborenen Fehlbildungsformen und wird in einer bundesweiten Studie mit einem Kollektiv von > 1 Mio. Geburten mit einer Prävalenz von ca. 0,21/10.000 angegeben. Innerhalb aller dort gemeldeten Gliedmaßenfehlbildungen kommt der Tibiadefekt mit einer Häufigkeit von ca. 1 % vor 19. Auch hier treten unterschiedliche Ausprägungen und Schweregrade auf. In internationalen Publikationen wird häufig noch die aus dem Jahre 1978 stammende 4‑Typen-Klassifikation nach Jones 20 angewendet. In unserem Sprachraum hat sich hingegen die Klassifikation nach Kalamchi und Dawe 21 durchgesetzt, welche die distale Femurepiphyse in der Betrachtung nicht mit einem gesonderten Typ einbezieht und sich im Wesentlichen an den Ausprägungen der fehlgebildeten oder nicht vorhandenen Tibia orientiert. Unterschieden werden drei Typen 22:
- Typ I: Tibiaaplasie – vollständiges Fehlen der Tibia
- Typ II: Tibia-Hypoplasie mit Fehlen der distalen Hälfte
- Typ III: Dysplasie der distalen Tibia mit Diastase der tibiofibulären Syndesmose
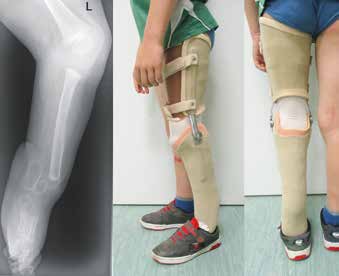
Bei Typ I und II ist klinisch auffällig, dass das Kniegelenk nicht dem Zustand eines normalen physiologischen Kniegelenkes entspricht, womit mehr oder minder starke Bewegungseinschränkungen einhergehen (Abb. 8).
Bei Fehlbildungen oder beim kompletten Fehlen (Aplasie) der Tibia können folgende für die Orthoprothesenversorgung wichtigen klinischen Auffälligkeiten beobachtet werden:
- Hypoplasie der Großzehe
- Polydaktylie
- invertierte Fußposition
- prominenter Malleolus lateralis
- dorsokraniale Dislokation der Fibula
- eingeschränkte ROM
- Beinlängendifferenz
- Hyperplasie der Fibula
- Schwäche des M. quadriceps femoris
Die orthoprothetische Versorgung des Tibiadefektes gestaltet sich typabhängig und berücksichtigt neben den Instabilitäten auch die jeweiligen Funktionsdefizite.
Bei komplettem Fehlen der Tibia ist die dorsokraniale Dislokation der Fibula kaum aufzuhalten. Das Problem dabei ist, dass sich diese Verlagerung limitierend auf die Kniebeugung auswirken kann. Eine frühzeitige Orthoprothesen-Versorgung für den Typ I sollte daher stets oberschenkellang angefertigt werden und über den Weichwandinnenschaft am Unterschenkel und die CAT-Fassung am Oberschenkel ein distrahierendes Moment auf die Fibula ausüben. Mit unterstützenden dynamischen Gasdruckfeder-Einheiten kann die Kniestreckung positiv beeinflusst werden. Problem ist dabei zumeist die fehlende Kraft der knieführenden Muskulatur, insbesondere des M. quadriceps femoris (Abb. 9). Aufgrund des kompletten Fehlens der Tibia wird das Knie nie eine annähernd stabile Situation erreichen können, bei der z. B. auf die Oberhülse in der Konstruktion verzichtet werden könnte.
Die oberschenkellange Orthoprothese stabilisiert das Bein beim Gehen und erhält den Bewegungsumfang im „Pseudo-Kniegelenk“ bestmöglich. In den angloamerikanischen Ländern wird dieser Typ häufig und bereits in den ersten Lebensjahren im Sinne einer Knieexartikulation amputiert – dies vor dem Hintergrund, dass die neue Körpersituation sich frühestmöglich kortikal etabliert.
Fibulofemorale Unterstellungsoperationen konnten bei Typ-I-Tibiadefekten nur mit fragwürdigen Ergebnissen durchgeführt werden. In einer Studie von Epps et al. 23 entwickelten alle Unterstellungen eine Flexionsdeformität. Die Hälfte der Patienten wurde kurze Zeit nach der Unterstellung knieexartikuliert. Deutlich bessere Ergebnisse zeigen sich nach Unterstellung der Fibula beim Typ II: Dort ist der proximale Anteil der Tibia noch vorhanden. Liegen die klinischen Voraussetzungen zur Unterstellung der Fibula — z. B. nach Brown 24 – vor, dann haben die Betroffenen Aussicht auf eine Reduktion der Versorgungshöhe, deshalb auf eine unterschenkellange Versorgung und dadurch eine deutlich verbesserte Prognose für die Nutzung der Orthoprothese im Lebensalltag (Abb. 10). Ohne Unterstellung erfolgt in der Regel eine oberschenkellange Versorgung. Auch hier ist eine Instabilität im Kniegelenk zu beobachten, die zumindest in der frontalen und sagittalen Ebene gut geführt sein muss.
Tibiadefekte Typ III kommen selten vor. Das Kniegelenk ist dabei weitestgehend stabil und benötigt maximal eine seitliche Führung durch eine Kondylenbettung. Instabilitäten treten hingegen im Rückfuß auf. Dem Talus mangelt es an bilateraler Führung der Knöchelgabel, und der Malleolus lateralis neigt dazu, prominent hervorzutreten. Eine entsprechende Hilfsmittelversorgung kann dabei sowohl orthetisch als auch orthoprothetisch erfolgen. Unabhängig von der Konstruktion ist bei dieser Versorgung wichtig, dass der Rückfuß eine stabilisierende zirkuläre Führung erhält.
Orthoprothetische Versorgung bei angeborenem Femurdefekt
Der Femurdefekt tritt fast ausschließlich im Bereich des proximalen Femurs auf, weswegen sich die erste Klassifikation von Aitken tatsächlich auch mit der radiologischen Eingrenzung des proximalen Femuranteils sowie der Hüfte befasste 25. Sie besteht aus vier der Schwere nach ansteigenden Typen A bis D des proximalen fokalen Femurdefektes und liefert relevante Aussagen für die Hilfsmittelversorgung. In den 80er Jahren stellte Pappas 26 eine erweiterte Klassifikation mit neun Typen auf, die der Vollständigkeit halber neben der Femuraplasie auch noch den seltenen distalen Femurtyp sowie hypoplastische Formen des Femurs beschrieb. Erweiterte bildgebende Verfahren wie z. B. Sonographie und MRT sowie die Einbeziehung der vorhandenen Funktionalitäten wie z. B. des Bewegungsumfangs des Hüft- und Kniegelenkes führten zur heute gängigen Klassifikation nach Dror Paley 27. Im Vergleich zu den älteren Klassifikationen beinhaltet die Paley-Klassifikation in ihren acht Klassen auch Hinweise auf mögliche Behandlungsstrategien – zumeist operative wie z. B. seine sogenannten Superhip- und Superknee-Rekonstruktionen.
Für den Orthopädie-Techniker ist es wichtig, die Klassifikationen und ihre Besonderheiten zu kennen. Bereits im Vorfeld einer orthoprothetischen Versorgung werden Informationen zu Stabilität, Belastbarkeit und Beweglichkeit von Hüfte und Knie benötigt 28 29. Unterschieden werden muss auch, ob die Orthoprothesenversorgung nach etwaigen operativen Eingriffen durchgeführt wird oder ob ein bestehender Femurdefekt konservativ versorgt wird. Die orthoprothetische Versorgung des Femurdefektes findet zumeist in einer oberschenkellangen Versorgungstechnik statt. Lediglich bei den Klassifikationstypen mit stabiler Hüft- und Kniesituation ohne wesentliche Flexionskontrakturen kann an eine Versorgung mit einer unterschenkellangen Orthoprothese gedacht werden (Abb. 11). Grundsätzliche Charakteristika, die der Orthopädie-Techniker bei der Versorgung des Femurdefektes berücksichtigen sollte, sind:
- Verkürzung des Beines an OS und US
- Insuffizienz und Pathologie der proximalen Muskulatur (u. a. resultiert hieraus auch die vermehrte Abduktion)
- Hüft- und Knieflexionsfehlstellung bis hin zur Kontraktur mit Gefahr der Progredienz
- Malrotation des Beines (häufig Außenrotation)
- pelvifemorale Instabilität
- assoziierte Fehlbildungen wie z. B. die Fibulaaplasie
Häufig gibt es in der Versorgungspraxis Hilfsmittel, die ihren ausschließlichen Fokus auf den Ersatz der fehlenden Beinlänge richten. Dies ist für eine derartige komplexe Deformität nicht ausreichend und fördert unter Umständen bereits bestehende Pathologien. Der Femurdefekt tritt oft mit assoziierten Anomalien wie z. B. einer Fibulaaplasie auf, wodurch der Anspruch bezüglich der Gestaltung des geeigneten Hilfsmittels deutlich zunimmt. Auch der Zeitpunkt der Versorgung beeinflusst die Behandlungsstrategie der konservativen Hilfsmittelversorgung entscheidend. So macht es einen deutlichen Unterschied, ob ein Kind oder ein Erwachsener mit Femurdefekt versorgt wird. Die meisten Femurdefekte zeichnen sich im proximalen Femurbereich ab. Das Femur ist stark verkürzt und wirkt gedrungen; die Muskulatur weicht deutlich von der normtypischen Interaktion von Spieler/Gegenspieler ab. Dadurch unterliegt der zu kurze Oberschenkel der Gefahr einer zunehmenden Fehlstellung in die Flexion, Abduktion und Außenrotation. Infolgedessen ist auch das Knie im kompensatorischen Sinne betroffen und neigt vor allem in den ersten Jahren zur Abweichung in die vermehrte unphysiologische Flexionsstellung.
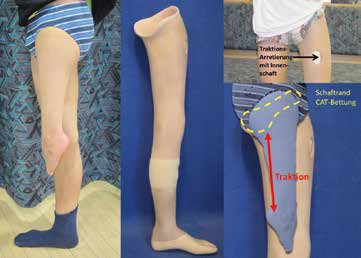
In den ersten beiden Lebensjahren sollte daher die Anbringung frei beweglicher Gelenke im Kniebereich der Orthoprothese als obsolet angesehen werden. Sehr wichtig ist, dass das Lernen des Aufrichtens, Stehens und Gehens mit einer bestmöglichen Extension dieser Gelenke in der orthoprothetischen Konstruktion erfolgt. Oftmals geht mit dieser Flexionsfehlstellung eine nicht zu unterschätzende Instabilität in Hüfte und Knie einher. Die Orthoprothese sollte daher mit einem sitzbeinintegrierenden („CAT-Bettung“) Containerschaft versehen werden. Im Bereich des Fußes und Unterschenkels empfiehlt sich zum Aufbau einer Traktionswirkung die zirkuläre Einbettung mit einem Weichwandinnenschaft mit frontalem Verriegelungskeil zum Außencontainer der Orthoprothese 30. Als Gegenlager zum Aufbau der extendierenden Längstraktion dient hierzu die zuvor erwähnte CAT-Bettung, bei der das Femur in eine bestmögliche Adduktionsstellung zu bringen ist (Abb. 12). Bei der späteren Umstellung auf eine Freigabe der Beweglichkeit des Kniegelenks sollte wegen der zunehmenden Gefahr erneuter Flexionsdeformitäten an zusätzliche Lagerungsorthesen für die Nacht mit dynamischen Streckquengelungen gedacht werden.
Beinlängendefizite von Patienten mit Femurdefekten sind vermehrt im Bereich des Oberschenkels angesiedelt. Bei assoziierten Anomalien wie z. B. dem Fibuladefekt, die bei weit über 50 Prozent der Femurdefekte vorkommen, kann man auch am Unterschenkel Längendifferenzen feststellen. Für die orthoprothetische Versorgung ist es sehr wichtig, dass man beim Aufbau der Orthoprothese möglichst seitengleiche Längenverhältnisse der Beine schafft. Dies hat wichtige Auswirkungen, die man sowohl beim Sitzen als auch bei der Ansteuerung der Orthoprothese in der Dynamik erkennen kann. So können während des Heranwachsens Disproportionen mit Drehpunktverlagerungen entstehen, die das normale Sitzen z. B. in der Schule oder in öffentlichen Verkehrsmitteln beeinträchtigen (Abb. 13). Ein operativer Wachstumsstopp der distalen Epiphysenfuge kann bei hohen Defekten für die dauerhafte Funktionalität – auch nach Wachstumsabschluss – sehr wertvoll sein. Oftmals müssen bereits bei der Formabnahme zur Orthoprothesenversorgung etwaige Längenverhältnisse und Stellungen des noch vorhandenen Fußes berücksichtigt werden, damit später ein entsprechendes Kniesystem in achsengerechter Position an der orthoprothetischen Konstruktion angebracht werden kann. In Einzelfällen müssen durch individuelle Zurichtungen niedrigste Verbindungselemente geschaffen werden, damit der Einsatz eines adäquaten Funktions-Passteils überhaupt erst erfolgen kann.
Beckenübergreifende Versorgungen kommen glücklicherweise nur selten vor. Sie sind meistens auf instabile Hüftsituationen, Streckdefizite in der Hüfte und Femuraplasien zurückzuführen und sollen den Kindern und Jugendlichen überhaupt erst eine ausreichende Rumpfstabilität für das Erlernen der Fortbewegung ermöglichen (Abb. 14).
Fazit
Die orthopädietechnische Versorgung angeborener longitudinaler Gliedmaßendefekte der unteren Extremität stellt sich als äußerst variantenreich dar und fordert selbst spezialisierte Orthopädie-Techniker regelmäßig auf, erfahrenes Handeln zu hinterfragen. Keine Versorgung vergeht, ohne dass etablierte Vorgehensweisen modifiziert oder gar verworfen werden müssen. Zusätzliche Informationen aus der bildgebenden Diagnostik ermöglichen einen transparenteren Blick auf die Klassifikationen der Deformitäten. Dieser Umstand lässt die orthoprothetische Versorgung in einem höchst spannenden und zugleich auch technisch sehr anspruchsvollen Umfeld erscheinen. Auch die zunehmende Komplexität, die bei der Integration hochentwickelter und anspruchsvoller mikroprozessorgesteuerter Prothesenpassteile zum Einsatz kommt, erfordert umso mehr eine enge interdisziplinäre Abstimmung mit den behandelnden Ärzten und Therapeuten. Letztendlich müssen alle Bestrebungen dem Betroffenen zugutekommen und dessen Teilhabe am Lebensalltag bestmöglich unterstützen.
Für die Autoren:
Michael Schäfer, GF
Diplom-Orthopädietechnik-Meister
Pohlig GmbH
Grabenstätter Str. 1
83278 Traunstein
m.schaefer@pohlig.net
Begutachteter Beitrag/reviewed paper
Schäfer M, Fleps H, Baumeister T, Wiedmann S. Orthoprothetische Versorgung longitudinaler Gliedmaßenfehlbildungen an den unteren Extremitäten von Kindern und Jugendlichen. Orthopädie Technik, 2018; 69 (1): 40–47
- Vergleichende Prüfung konventioneller und additiv gefertigter Prothesenschäfte in Anlehnung an DIN EN ISO 10328:2016 — 10. März 2026
- Easypreg – ein Faserverbundwerkstoff zum Tiefziehen — 9. März 2026
- Konservative Versorgung einer adulten Skoliose mit einem modularen Bausatz – ein Versorgungsbeispiel — 6. März 2026
- Döderlein L, Schäfer M. Rehabilitation von Kindern und Jugendlichen mit angeborenen Fehlbildungen. Kinder- und Jugendmedizin, 2010; 10 (7): 395–402
- Schoenecker PL, Capelli AM, Millar EA, Sheen MR, Haher T, Aiona MD, Meyer LC. Congenital longitudinal deficiency of the tibia. J Bone Joint Surg Am, 1989; 71 (2): 278–287
- Weber M, Schröder S, Berdel P, Niethard F. Register zur bundesweiten Erfassung angeborener Gliedmaßenfehlbildungen. Zeitschrift für Orthopädie und Unfallchirurgie, 2005; 143 (5): 534–538
- Greitemann B, Brückner L, Schäfer M, Baumgartner R. Amputation und Prothesenversorgung. Indikationsstellung – operative Technik – Nachbehandlung – Funktionstraining. 4., vollständig überarbeitete Auflage. Stuttgart, New York: Thieme Verlag, 2016: 504–531
- Marquardt E. The multiple limb deficient child. In: Bowker JH, Michael JW (eds). Atlas of limb prosthetics. 2nd edition. St. Louis: Mosby, 1992: 839–884
- Marquardt E. The management of infants with malformation of the extremities. In: Swinyard CA (ed.). Limb Development and Deformity: Problems of Evaluation and Rehabilitation. Springfield, Illinois: Charles C. Thomas Publishers, 1969: 363–378
- Fatone S. Gait Biomechanics and Prosthetic Management of Children with Proximal Femoral Focal Deficiency. ACPOC News, 2003; 9 (1): 5–13
- Greitemann B, Brückner L, Schäfer M, Baumgartner R. Amputation und Prothesenversorgung. Indikationsstellung – operative Technik – Nachbehandlung – Funktionstraining. 4., vollständig überarbeitete Auflage. Stuttgart, New York: Thieme Verlag, 2016: 504–531
- Schäfer M, Gawron O. Neue Techniken in der prothetischen Versorgung nach Amputationen. Der Orthopäde, 2015; 44: 445–457
- Bellmann M, Blumentritt S, Pusch M, Schmalz T, Schönemeier M. Das 3D L.A.S.A.R. – eine neue Generation der Statik-Analyse zur Optimierung des Aufbaus von Prothesen und Orthesen. Orthopädie Technik, 2017; 68 (12): 18–25
- Schäfer M. Individuelle kosmetische Gestaltungsvarianten in der Beinprothetik. Med Orth Tech, 2006; 126 (5): 71–78
- Achterman C, Kalamchi A. Congenital Deficiency of the Fibula. J Bone Joint Surg Br, 1979; 61‑B (2): 133–137
- Greitemann B, Brückner L, Schäfer M, Baumgartner R. Amputation und Prothesenversorgung. Indikationsstellung – operative Technik – Nachbehandlung – Funktionstraining. 4., vollständig überarbeitete Auflage. Stuttgart, New York: Thieme Verlag, 2016: 504–531
- Sabharwal S (ed.). Pediatric Lower Limb Deformities. Principles and Techniques of Management. Berlin, New York: Springer Verlag, 2016: 428 ff., 455 ff.
- Greitemann B, Brückner L, Schäfer M, Baumgartner R. Amputation und Prothesenversorgung. Indikationsstellung – operative Technik – Nachbehandlung – Funktionstraining. 4., vollständig überarbeitete Auflage. Stuttgart, New York: Thieme Verlag, 2016: 504–531
- Greitemann B, Brückner L, Schäfer M, Baumgartner R. Amputation und Prothesenversorgung. Indikationsstellung – operative Technik – Nachbehandlung – Funktionstraining. 4., vollständig überarbeitete Auflage. Stuttgart, New York: Thieme Verlag, 2016: 504–531
- Sabharwal S (ed.). Pediatric Lower Limb Deformities. Principles and Techniques of Management. Berlin, New York: Springer Verlag, 2016: 428 ff., 455 ff.
- Greitemann B, Brückner L, Schäfer M, Baumgartner R. Amputation und Prothesenversorgung. Indikationsstellung – operative Technik – Nachbehandlung – Funktionstraining. 4., vollständig überarbeitete Auflage. Stuttgart, New York: Thieme Verlag, 2016: 504–531
- Weber M, Schröder S, Berdel P, Niethard F. Register zur bundesweiten Erfassung angeborener Gliedmaßenfehlbildungen. Zeitschrift für Orthopädie und Unfallchirurgie, 2005; 143 (5): 534–538
- Jones D, Barnes J, Lloyd-Roberts GC. Congenital Aplasia and Dysplasia of the Tibia with intact fibula. Classification and Management. J Bone Joint Surg Br, 1978; 60 (1): 31–39
- Kalamchi A, Dawe RV. Congenital Deficiency of the Tibia. J Bone Joint Surg Br, 1985; 67 (4): 581–584
- Hefti F. Kinderorthopädie in der Praxis. 3., vollständig überarbeitete Auflage. Berlin, Heidelberg: Springer, 2015: Kap. 6.6.3. Tibialer Längsdefekt, Kap. 5.7.2.2. Longitudinale Femurfehlbildungen
- Epps CH Jr, Tooms RE, Edholm CD, Kruger LM, Bryant DD 3rd. Failure of Centralization of the Fibula for congenital longitudinal Deficiency of the Tibia. J Bone Joint Surg Am, 1991; 73 (6): 858–867
- Brown FW. The Brown operation for total hemimelia tibia. In: Aitken G (ed.): Selected lower limb anomalies. Washington, DC: National Academy of Sciences, 1971: 20
- Aitken GT. Proximal femoral focal deficiency – definition, classification, and management. In: Aitken GT (ed.). Proximal femoral focal deficiency: a congenital anomaly. A symposium held in Washington, D. C., June 13, 1968. Washington, D.C.: National Academy of Sciences, 1969: 1–22. http://myplace.frontier.com/~pffdvsg1/med-aitken69.htm (Zugriff am 24.11.2017)
- Pappas AM. Congenital abnormalities of the femur and related lower extremity malformations: classification and treatment. J Pediatr Orthop, 1983; 3 (1): 45–60
- Paley D, Standard SC. Lengthening reconstruction surgery for congenital femoral deficiency. In: Rozbruch SR, Ilizarov S (eds). Limb lengthening and reconstruction surgery. New York, NY: Informa Healthcare, 2007: 393–428
- Greitemann B, Brückner L, Schäfer M, Baumgartner R. Amputation und Prothesenversorgung. Indikationsstellung – operative Technik – Nachbehandlung – Funktionstraining. 4., vollständig überarbeitete Auflage. Stuttgart, New York: Thieme Verlag, 2016: 504–531
- Pohlig K, Baise M, Correll J. PFFD – Neue Möglichkeiten zur Versorgung des proximalen Femurdefektes. MOT, 2016; 116 (4): 208–211
- Weber M, Schröder S, Berdel P, Niethard F. Register zur bundesweiten Erfassung angeborener Gliedmaßenfehlbildungen. Zeitschrift für Orthopädie und Unfallchirurgie, 2005; 143 (5): 534–538