Einleitung
Spastische Lähmungen (SL) können infolge von Krankheiten und Unfallleiden wie Schlaganfall (Stroke), Multipler Sklerose (MS), Amyotropher Lateralsklerose (ALS), Schädel-Hirn-Trauma (SHT) und einigen mehr entstehen 1 2 3 4. Eine häufige Folge dieser Erkrankungen ist eine zentrale oder spastische Parese. Infolge der spastischen Parese kommt es zu funktionellen Muskelverkürzungen und folglich zu einer eingeschränkten Beweglichkeit der betroffenen Extremitäten bis hin zur Gelenkversteifung 5 6. Dieses Phänomen äußert sich in Einschränkungen der Lebensqualität sowie der Alltagsfunktionen. Patienten sind dann nur eingeschränkt oder gar nicht mehr in der Lage, lange Strecken zu bewältigen sowie alltäglichen Tätigkeiten (z. B. Hausarbeit) nachzugehen. Auch soziale Strukturen können unter dem Symptom der SL leiden und sich verringern 7. Bis zum heutigen Tag können SL nicht geheilt werden, sodass im Alltag in enger Zusammenarbeit von Hilfs- und Heilmittelerbringern versucht wird, zumindest einer Progredienz der Symptomatik vorzubeugen 8.
Im Rahmen eines Kooperationsprojektes im Kontext des Zentralen Innovationsprogramms Mittelstand (ZIM) des Bundeswirtschaftsministeriums (BMWi) werden Assistenzsysteme bzw. Therapieunterstützungssysteme für Patienten mit spastischen Paresen infolge neuromuskulärer Erkrankungen erforscht, um die genannten Sekundärkomplikationen bei SL der unteren Extremität zu reduzieren. Das hier vorgestellte Assistenzsystem beruht auf einer orthetischen Versorgung mit integrierter Sensorik zur Erfassung der körperlichen Aktivität und des Bewegungsumfangs (Range of Motion, ROM). In diesem Zusammenhang wurde vom BMWi ein Kooperationsprojekt gefördert, bestehend aus folgenden Teilnehmern:
- Thorsis Technologies Gmbh, Magdeburg,
- Orthopädietechnik Scharpenberg e. K., Rostock,
- Otto-von-Guericke-Universität Magdeburg,
- Universitätsmedizin Rostock.
Ziel des Vorhabens war die Entwicklung des Prototyps einer motorisierten Sprunggelenk-Fuß-Orthese (Ankle Foot Orthosis, AFO), die einen dynamischen Therapiemodus, einen statischen Quengelungsmodus und einen Monitoringmodus umfassen sollte.
Prototyp
Die „Moto-AFO“-Orthese besteht aus einem eigens entwickelten Gelenk mit Antriebseinheit, Sensorik und Akku sowie aus Schalenbauteilen, die von einem Orthopädietechniker individualisiert werden (Abb. 1a–c). Die Motoreinheit ist in der Lage, eine statische und dynamische Regelung der SL infolge von Schlaganfällen oder Multipler Sklerose vorzunehmen. Mittels Therapiemodus, Spastikdetektion, stetiger Quengelung und eines Monitoringprogramms wird der Muskeltonus individuell an den Patienten und die jeweilige Situation angepasst, um einen interdisziplinären Therapieerfolg zu sichern. Auf drei dieser Modi wird im Folgenden genauer eingegangen.
Therapiemodus
Dieser Modus erzeugt eine rhythmisch-dynamische Bewegung in Dorsalextension und Plantarflexion. Im Speziellen sind in diesem Modus folgende Parameter frei wählbar:
- Pausenzeit,
- Bewegungszeit,
- Drehmoment (bis zu 6,6 Nm) und
- Geschwindigkeit des Fußbügels.
Die Orthese soll Bewegungen imitieren, die im Rahmen einer klassischen Physiotherapie durchgeführt werden, um eine zusätzliche Reduzierung der Muskelspannung außerhalb der Therapiephasen zu gewährleisten. Nutzungszeiträume müssen dabei individuell mit dem Therapeuten und dem Arzt bestimmt werden.
Spastikdetektion
Erhöht sich infolge der SL der Druck auf die Orthese bis zu einem vorgegebenen Schwellenwert, gibt das Knöchelgelenk (der elastische Antrieb) den Widerstand sofort frei. Nach einer vom Arzt, Techniker oder Therapeuten festgelegten Pausenzeit unter Einschätzung der Tonussituation nimmt die Orthese ihre Funktion wieder auf.
Basismodus (dynamische Quengelung)
Die Orthese ist in der Lage, den State of the Art mechanischer Quengelgelenkschienen elektrisch abzubilden. Zudem können folgende Parameter vom Arzt, Techniker oder Therapeuten definiert werden:
- das Bewegungsausmaß (Range of Motion, ROM),
- die Motorkraft (in Nm),
- Pausenzeiten sowie
- die Geschwindigkeit.
Durch ein Monitoringprogramm und die damit verbundene Auswertung werden dem medizinischen Fachpersonal entsprechende Daten bereitgestellt, um die Therapie anzupassen.
Methodik/Design der Evaluationsstudie
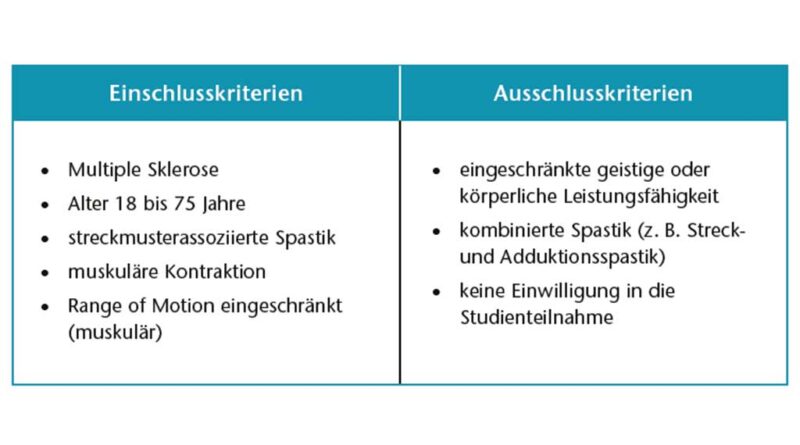
Im Zeitraum von Anfang Januar 2019 bis Ende Dezember 2021 wurde das Vorhaben der Entwicklung, Umsetzung und Evaluierung der Orthese durchgeführt. Eine entsprechende Crossover-Untersuchung mit bis zu 4 Probanden mit MS wurde von der ständigen Ethikkommission der Universitätsmedizin Rostock genehmigt. Die 4 MS-Patienten wurden in Bezug auf die in Tabelle 1 aufgeführten Ein- und Ausschlusskriterien untersucht.
In der vorliegenden Untersuchung wird die Umsetzung des Assistenzsystems im Hinblick auf die Therapieunterstützung, d. h. die Detonisierung der spastischen Muskulatur mittels Bewegungen, evaluiert. Das Interventionsmodell war in 3 Phasen unterteilt:
A: 4 Wochen kein Tragen der Orthese (klinische Tests)
B: 4 Wochen Tragen der Orthese zusätzlich zur Physiotherapie (Monitoring durch Orthese)
A: 4 Wochen kein Tragen der Orthese (klinische Tests)
Zur Beurteilung der Funktionen und der Lebensqualität dienten folgende Assessments und klinische Untersuchungen:
- Messung der ROM (Range of Motion/Bewegungsfreiheit);
- modifizierte Ashworth-Skala (Instrument, um die Spastizität eines Muskels zu messen);
- Timed 25-Foot Walk Test (T25FW; Gehen einer 7,62 m langen Strecke).
In beiden A‑Phasen wurden zusätzlich das Beck Depression Inventory (BDI) und der Short Form (12) Health Survey (SF-12) angewendet. In Phase B übernahm die Orthese selbst die Messung der ROM und die Intervention. Die Patienten wurden aufgefordert, zweimal am Tag sowohl den Basismodus als auch den Therapiemodus für jeweils 15 Minuten zu nutzen. Es wurde empfohlen, nach dem Aufstehen und am Abend jeweils eine Einheit, bestehend aus Basis- und Therapiemodus, durchzuführen. An die vierwöchige Tragezeit schloss sich eine erneute Phase A an.
Ergebnisse
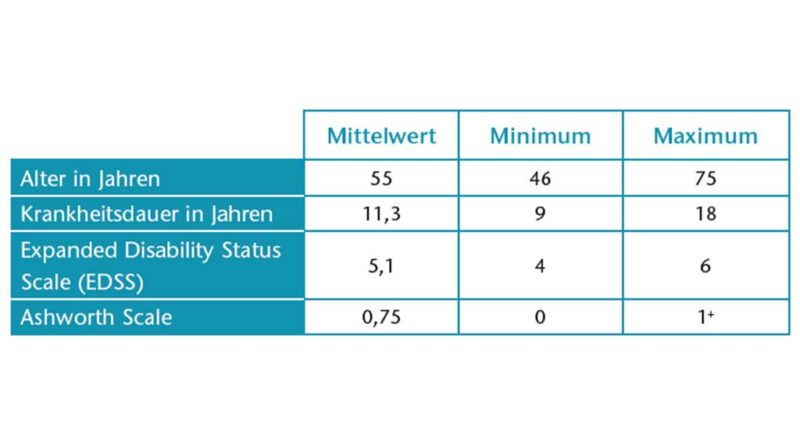
Vier Patienten haben die Untersuchung zum Zeitpunkt der Einreichung der Publikation (Stand: Januar 2022) abgeschlossen (Tab. 2). Zwei männliche Teilnehmer und zwei Frauen haben bis zu diesem Zeitpunkt an der Untersuchung teilgenommen. Das durchschnittliche Alter betrug 55 Jahre; die durchschnittliche Krankheitsdauer lag bei 11,3 Jahren. Alle Patienten konnten gehen und waren kognitiv in der Lage, die Orthese zu bedienen.
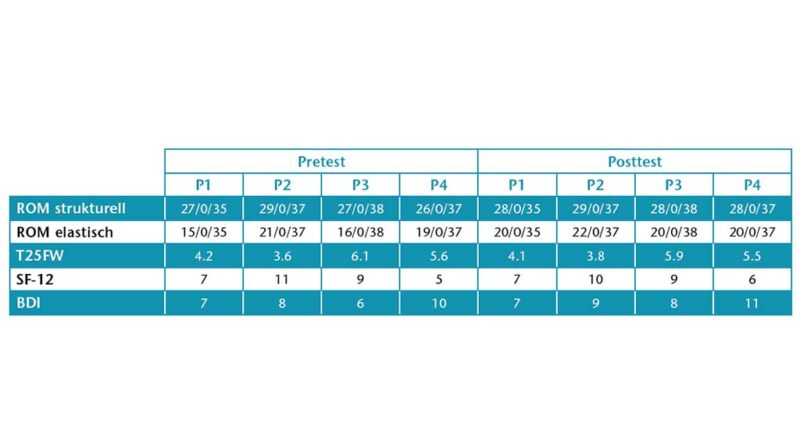
Im Mittel gab es bei 3 von 4 Probanden eine leichte Muskeltonuserhöhung infolge einer abrupten Flexionsbewegung, was in der Ashworth-Skala mit 1 bis 1+ gewertet wird. Die ROM wird in einen strukturellen Anschlag und einen elastischen Stopp unterteilt, um eine potenzielle Verbesserung durch eine Bewegungsförderung zu gewährleisten und eine Kontraktur auszuschließen. Bei allen Beteiligten stimmten elastischer Stopp und strukturelles Bewegungsende nicht überein (Tab. 3), sodass die motorisierte Orthese in diesem Bereich mobilisieren konnte.
Im Vergleich zu den klinischen Eingangs- und Abschlusstests waren im SF-12, beim BDI und bei den T25FW-Tests keine großen Veränderungen sichtbar. Dennoch gaben alle Probanden am Ende der Phase B an, dass sich unmittelbar nach dem Einsatz der Orthese eine verbesserte Gangqualität einstellte, die im häuslichen Umfeld jedoch nicht objektiv gemessen wurde.
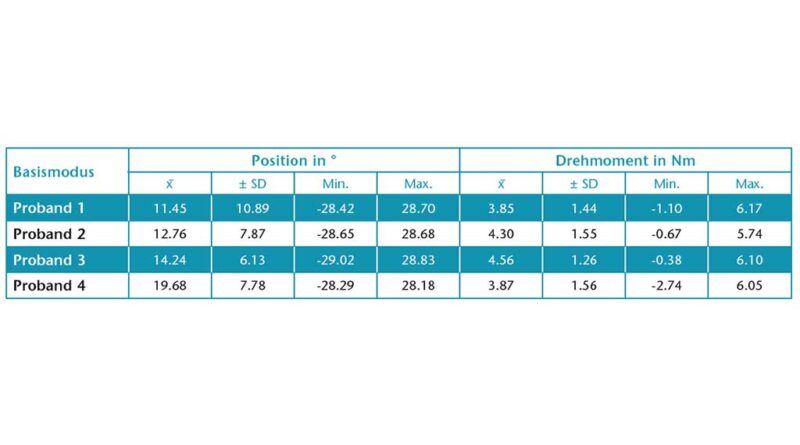
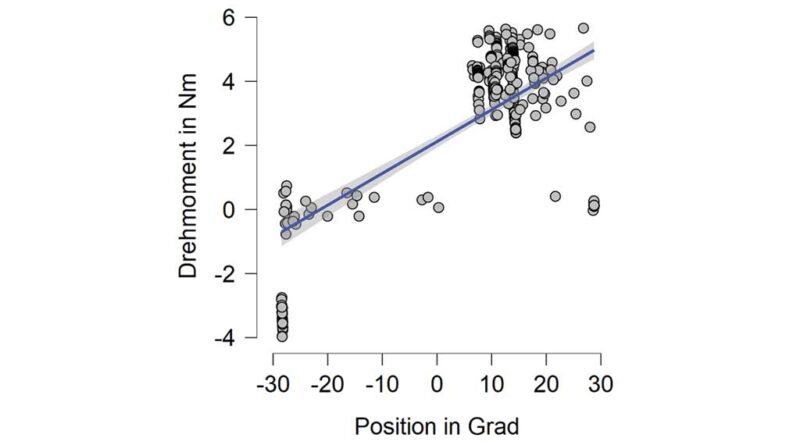
Unter Einsatz der Orthese konnten Veränderungen zwischen der elastischen und der strukturellen ROM im Basismodus aufgezeigt werden (Tab. 4). Die „Moto-AFO“ konnte mit einem Drehmoment von 5.74 Nm bis 6.17 Nm die klinisch gemessene Dorsalextension (max.) im Basismodus erreichen. Es ist allerdings anzumerken, dass die Orthese maximal 6.6 Nm aufbringen kann. Im Mittel wurden von der „Moto-AFO“ 3.85 ± 1.26 bis 4.56 ± 1.55 Nm aufgebracht, sodass das maximale Potenzial der Orthese ausgeschöpft werden konnte (Abb. 2).
Im Basismodus ist weiterhin zu sehen, dass der Prototyp in der Lage ist, das Drehmoment gegen den Widerstand bei größer werdendem Winkel zu adaptieren (s. Abb. 1). Im Diagramm ist deutlich zu erkennen, dass im Bereich von 10 bis 30 Grad das Drehmoment zunimmt, um den Winkel zu erreichen. Dabei kann der Prototyp das Drehmoment nahezu linear beschleunigen. Daten, die für die Messung (s. Abb. 1) genutzt werden, beinhalten das Monitoring, beginnend mit dem Ende der Spastikdetektion. Dabei wird ersichtlich, dass beispielsweise bei einer kompletten Freigabe aus der Plantarflexion von ‑30 Grad die Messung aufgezeichnet wurde und somit dieser Wert berücksichtigt wurde. Im Therapiemodus wurde eine rhythmisch-dynamische Bewegung vom elastischen Motor der Orthese durchgeführt und gleichzeitig gemessen. Das verdeutlichen die exemplarisch gemessenen Daten an Proband 1. Der Therapiemodus wurde bei allen Patienten oberhalb der elastischen Schwelle eingestellt, sodass von der Orthese keine Gefahr der Überdehnung ausgeht.
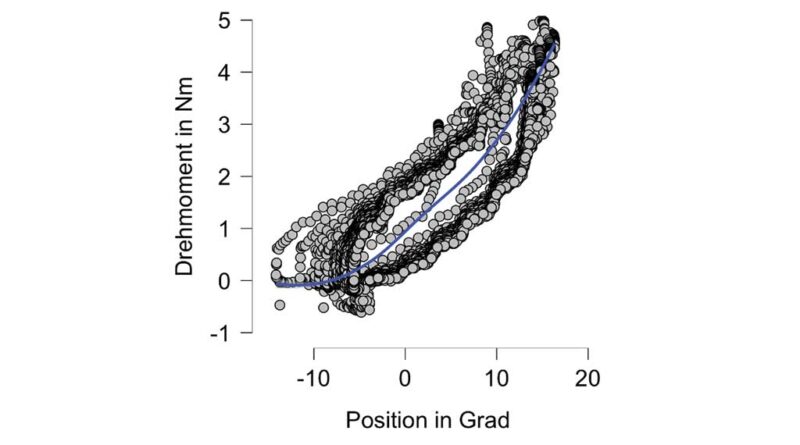
In Abbildung 3 wird ersichtlich, dass bei der Dorsalextension durch die rhythmisch-dynamische Bewegung die Punktverläufe nicht deckungsgleich sind, während bei der Rückbewegung (Plantarflexion) eine annähernde Gleichheit dieser Verläufe vorliegt. Während der Motor in der Rückbewegung von einem positiven in ein negatives Drehmoment mit geringem Widerstand unter Berücksichtigung der Schwerkraft übergeht, ist bei der Dorsalextension der Aufwand für den Motor wesentlich höher. Aus diesem Grund entstehen weniger deckungsgleiche Punktverläufe, was ein Indikator für die ständige Anpassung des Drehmomentes und des Widerstandes ist.
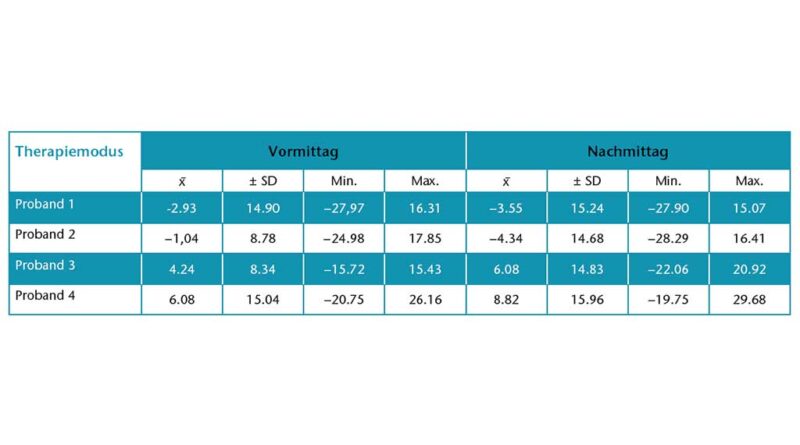
Eine Verbesserung der ROM innerhalb der gesamten Untersuchungsdauer konnte nicht gegen den Zufall abgesichert werden. Hingegen konnten mit Hilfe der Orthese in Phase B Daten gesammelt werden, um zeitliche Veränderungen zu messen (Tab. 5). Es ist zu erkennen, dass die ROM im Mittel am Vormittag im Vergleich zum Nachmittag geringer war.
Diskussion
Die Untersuchung demonstrierte in erster Linie die Machbarkeit und Umsetzung des Projektvorhabens. Alle Funktionen der Orthese sowie die korrekte Funktionsweise konnten messbar dargelegt werden. Zusätzlich konnte unter Einsatz der Orthese kein negativer Einfluss festgestellt werden. Hinsichtlich der geringen Probandenzahl infolge der ethischen Sicherheitskriterien für einen Prototyp ist eine statistische Analyse zwar nicht möglich – jedoch sind durchaus positive Trends in den Messungen zu beobachten. In therapeutischen Interventionsstudien können minimale signifikante Veränderungen erst über einen Zeitraum von 8 bis 10 Wochen nachgewiesen werden 9 10 11. Die effektive Tragezeit betrug in der vorliegenden Untersuchung jedoch nur 4 Wochen. In dieser Zeit benutzten die Probanden täglich am Vor- und Nachmittag für jeweils 15 Minuten den Basis- und den Therapiemodus, sodass eine effektive Therapiezeit von einer Stunde pro Tag eingehalten wurde. Ein Ausbleiben von signifikanten Verbesserungen kann daher in der relativ geringen Therapiedosis begründet sein. Die Ergebnisse einer Meta-Analyse in Bezug auf das Laufbandtraining deuten darauf hin, dass die Therapiedauer länger sein muss 12.
Demgegenüber ist anzumerken, dass dies der erste Versuch ist, eine neue prototypische „intelligente“ Orthese mit Spastikdetektion zu konzipieren. Ein derzeit noch brachliegendes Verbesserungspotenzial besteht in der Verbindung vielseitigerer Mobilisationsebenen. Die „Moto-AFO“ ist derzeit nur in der Lage, eine Bewegungsrichtung mit ihren Modi zu begleiten. Studien legen nahe, dass die Zuhilfenahme mehrerer Ebenen und Achsen eine Verbesserung der SL erreichen könnte. Jedoch gibt es in den entsprechenden Interventionsstudien nur eine unzureichend hohe Evidenz 13.
Ein weiteres Verbesserungspotenzial stellt das Drehmoment dar, das vom Motor aufgebracht wird. In der vorliegenden Untersuchung wurde im Basismodus ein Winkel von 28.70 Grad mit einer Motorkraft von 6,17 Nm erreicht. Folglich kann mit einem höheren Drehmoment ein gesteigerter positiver Reiz auf die spastische Muskulatur aufgebracht werden.
Schlussfolgerung
In diesem Projekt konnte die Machbarkeit einer prototypischen Orthese überprüft und Bewegungsdaten bezüglich SL detektiert werden. Aufgrund der mangelnden Evidenz im Hinblick auf die Therapieparameter und die geringe Anzahl der Probanden sind jedoch weitere Untersuchungen nötig, um eine genauere Aussage über die Wirksamkeit der Orthese treffen zu können. Das im Projekt aufgebrachte Drehmoment von 6,6 Nm ist zwar in der Lage, den Fuß über die elastische ROM-Grenze zu bewegen. Jedoch wird dabei oft das maximale Drehmoment erreicht, sodass ein stärkerer Motor für weitere erfolgversprechende Wirksamkeitsstudien notwendig ist. Alle Probanden berichteten, dass unmittelbar nach der Behandlung eine subjektive Verbesserung der Gangqualität aufgetreten sei. Die „Moto-AFO“ kann somit dazu beitragen, dass unter Mitwirkung aller interdisziplinären Leistungserbringer wie Physio- und Ergotherapeuten eine Verbesserung bezüglich SL in der unteren Extremität erreicht wird.
Interessenkonflikt
Das Projekt wurde über Drittmittel für alle beteiligten Kooperationspartner gefördert. Zwei der Partner halten Patentrechte am Prototyp der Orthese.
Projektförderung
Vom 01.01.2019 bis zum 31.12.2021 wurde das Kooperationsprojekt „Moto-AFO – Entwicklung einer Ankle Foot Orthese mit motorisiertem Knöchelgelenk (Moto-AFO) zur Therapie und Langzeitbehandlung von spastischen Lähmungen der unteren Extremitäten“ mit Mitteln des Zentralen Innovationsprogramms Mittelstand (ZIM) gefördert.
Hinweis
Im Rahmen eines Vortrages wurde die Orthese auf dem 65. Kongress der Fortbildungsvereinigung für Orthopädie-Technik e. V. (FOT) im September 2021 in digitaler Form vorgestellt.
Für die Autoren:
Maximilian Moyé, M. Sc., Physiotherapeut
EUFH Hochschule für Gesundheit,
Soziales & Pädagogik
Werftstraße 5
18057 Rostock
m.moye@eufh-medica.de
& Klinik und Poliklinik für Neurologie
Universitätsmedizin Rostock
Gehlsheimer Straße 20
18147 Rostock
Prof. Dr. med. Uwe Klaus Zettl
Leiter der Sektion Neuroimmunologie
Klinik und Poliklinik für Neurologie
Universitätsmedizin Rostock
Gehlsheimer Straße 20
18147 Rostock
Begutachteter Beitrag/reviewed paper
Moyé M, Merbold D, Zettl UK, Scharpenberg R. „Moto-AFO“: motorisierte AFO (Ankle Foot Orthosis) gegen spastische Bewegungserscheinungen. Orthopädie Technik, 2022; 73 (3): 28–33
- Entwicklung eines zum physiologischen Gangbild kongruenten polyzentrischen Knieorthesengelenks – Zwischenstand eines Forschungsprojektes — 10. April 2026
- Mikroprozessorgesteuerte stand- und schwungphasenkontrollierte Ganzbeinorthesen (SSCO): Entwicklung, Systeme und Versorgungsrealität in der orthopädietechnischen Praxis — 9. April 2026
- Gips oder Orthese bei distalen Radiusfrakturen? — 8. April 2026
- Burke D et al. Pathophysiology of spasticity in stroke. Neurology, 2013; 80 (3, Suppl 2): S20–S26
- Bose P et al. Traumatic Brain Injury (TBI)-Induced Spasticity: Neurobiology, Treatment, and Rehabilitation. In: Kobeissy FH (ed.). Brain Neurotrauma: Molecular, Neuropsychological, and Rehabilitation Aspects. Boca Raton (FL): CRC Press/Taylor & Francis, 2015: 1–28
- Hardiman O et al. Amyotrophic lateral sclerosis. Nat Rev Dis Primers, 2017; 3: 17071
- Patejdl R, Zettl UK. Spasticity in multiple sclerosis: Contribution of inflammation, autoimmune mediated neuronal damage and therapeutic interventions. Autoimmun Rev, 2017; 16 (9): 925–936
- Reich DS et al. Multiple Sclerosis. N Engl J Med, 2018; 378 (2): 169–180
- Zettl U et al. MS in Deutschland: Symptome und Behandlungsdefizite. NeuroTransmitter, 2018; 29 (6): 42–44
- Baumstarck K et al. Health-related quality of life as an independent predictor of long-term disability for patients with relapsing-remitting multiple sclerosis. Eur J Neurol, 2013; 20 (6): 907–914, e78–79
- Zorowitz RD et al. Poststroke spasticity: sequelae and burden on stroke survivors and caregivers. Neurology, 2013; 80 (3 Supplement 2): S45–S52
- Ahmadi A et al. Comparison of the Effect of 8 weeks Aerobic and Yoga Training on Ambulatory Function, Fatigue and Mood Status in MS Patients. Iran Red Crescent Med J, 2013; 15 (6): 449–454
- Conradsson D et al. The Effects of Highly Challenging Balance Training in Elderly With Parkinson’s Disease: A Randomized Controlled Trial. Neurorehabil Neural Repair, 2015; 29 (9): 827–836
- Robinson AG et al. Treadmill training may be an effective form of task-specific training for improving mobility in people with Parkinson’s disease and multiple sclerosis: a systematic review and meta-analysis. Physiotherapy, 2019; 105 (2): 174–186
- Robinson AG et al. Treadmill training may be an effective form of task-specific training for improving mobility in people with Parkinson’s disease and multiple sclerosis: a systematic review and meta-analysis. Physiotherapy, 2019; 105 (2): 174–186
- Barbosa P et al. Physiotherapy interventions for the treatment of spasticity in people with spinal cord injury: a systematic review. Spinal Cord, 2021; 59 (3): 236–247