Einleitung
Die Zahl der schulterprothetischen Versorgungen in Deutschland steigt stetig an. Es kommt insbesondere zu einem Anstieg sogenannter inverser Schulterprothesen, deren Zahl inzwischen auf mehr als 11.000 Implantationen pro Jahr angestiegen ist.
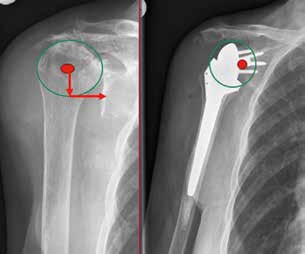
Weltweit werden die meisten Schulterprothesen von Operateuren implantiert, die weniger als zehn Implantationen pro Jahr durchführen 1. Das bringt die Gefahr mit sich, dass sich die Zahl der Komplikationen erhöht. Die inverse Schulterprothetik führt durchaus zu einer guten Rekonstruktion der Funktion bei Patienten mit Rotatorenmanschettendefekten 2. Durch die Umkehrung von Konvexität am Glenoid und Konkavität am Humerus wird das Drehzentrum distalisiert und medialisiert, was zu einer Reduktion des Drehmoments und zu einem zusätzlichen Recruitment von Deltafasern führt (Abb. 1a u. b) 3.
Distalisierung:
- Vorteil: Verbesserung des Momentarms für den M. deltoideus um 25 %
Medialisierung:
- Vorteil: Rotationszentrum in Projektion auf den glenoidalen Knochen reduziert die Implantat-Knochen-Belastung
- Nachteile: Scapula-Notching, Verlust der Deltoidkontur, Reduktion des Momentarms für den M. infraspinatus
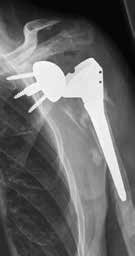
Gleichzeitig entstehen jedoch Komplikationen wie Instabilitäten mit Luxation (Abb. 2), akromiale Frakturen sowie Lockerungen glenoidaler und humeraler Komponenten, die in dieser Art bei den bisherigen Prothesen nicht bekannt waren. Villacis et al. (2016) 4 untersuchten die Komplikationen nach Schultervollprothesen im Vergleich mit inversen Prothesen bei 10.844 Prothesen. Die Komplikationsrate bezüglich Infektion und Dislokation war unterschiedlich zu Ungunsten der inversen Prothesen.
Inzidenz von Luxationen nach inversen Schulterprothesen
Die Luxation ist eine der häufigsten Komplikationen der inversen Prothetik. Zumstein et al. (2011) 5 berichteten in einer Reviewarbeit über eine Inzidenz von 4,7 %. Andere Autoren berichteten über eine Luxationsrate von 2,4 bis 31 % 6 7 8 9 10 11 12. Die Richtung der Luxation ist üblicherweise nach vorne und erfolgt durch Extension, Adduktion und Innenrotation. Generell wird die Frühinstabilität (innerhalb der ersten 3 Monate) von der Spätinstabilität (später als 3 Monate nach der Erstimplantation) unterschieden 13.
Ursachen für Instabilitäten
Faktoren für eine Instabilität können eine nicht ausreichende Weichteilspannung, ein mechanisches Impingement, eine falsche Version der glenoidalen Komponente oder eine falsche Torsion der humeralen Komponente sein. Bei den von Kohan et al. (2017) 14 untersuchten Patienten mit einer instabilen inversen Prothese zeigten 68 % eine ungenügende Weichteilspannung und 10 % eine N.-axillaris-Schädigung. Viele Patienten hatten einen asymmetrischen Abrieb im Bereich des Polyethylens. Ein asymmetrischer Polyethylenabrieb war für 60 % der Spätdislokationen verantwortlich. Eine erneute Instabilität konnten die Autoren bei 29 % der Frühluxationen und bei 40 % der Spätluxationen ermitteln.
Geschlecht und BMI
Chalmers et al. (2014) 15 zeigten eine Inzidenz an Frühluxationen von 2,9 %, wobei besonders voroperierte Patienten eine Risikogruppe darstellten. 64 % waren männliche Patienten; 82 % hatten einen BMI von 32,2. Eine geschlossene Reposition war bei 44 % erfolgreich; 45 % benötigten einen Wechsel des Polyethyleninlays.
Padegimas et al. (2016) 16 zeigten, dass Patienten mit einer primären Defektarthropathie ein geringeres Dislokationsrisiko aufweisen. Auch hier stellte ein hoher BMI einen Risikofaktor dar. Keine Dislokation konnte durch eine geschlossene Reposition behandelt werden; alle wurden operativ behandelt.
Humerale Inklination
Erickson et al. (2015) 17 untersuchten den Einfluss der humeralen Inklination anhand eines Literatur-Reviews bei 2.222 Schultern. Von diesen hatten 79,3 % eine Inklination von 155 Grad und 20,7 % von 135 Grad. Die Inzidenz des Scapula-Notchings betrug 2,83 % in der 135-Grad-Gruppe und 16,8 % in der 155-Grad-Gruppe; die Rate der Dislokation betrug 1,74 % in der 135-Grad-Gruppe und 2,33 % in der 155-Grad-Gruppe. Die Autoren schlussfolgerten daraus, dass das Scapula-Notching signifikant häufiger bei Prothesen mit 155 Grad Inklination als bei Prothesen mit 135 Grad Inklination vorkommt und dass sich die Dislokationsrate nicht signifikant unterscheidet.
Offset
Eine adäquate Weichteilspannung ist essentiell für die Stabilität der inversen Prothese. Hierzu zählen das vertikale Offset (Distanz Acromion zum Tub. majus) sowie das laterale Offset (Distanz Tub. majus zum Glenoid) 18.
Clouthier et al. (2013) 19 zeigten in einer biomechanischen Untersuchung auf, dass die Verwendung eines erhöhten Offsets zur Stabilität beiträgt. Henninger et al. (2012) 20 zeigten ebenso, dass eine Lateralisation des Rotationszentrums die Stabilität der inversen Prothesen erhöht, was jedoch durch eine Zunahme der deltoidalen Abduktionskraft erkauft wird.
Lädermann et al. (2014) 21 untersuchten die Länge des Humerus bei inversen Prothesen. Sie ermittelten in ihrem Literaturreview eine Änderung der humeralen Länge von ‑5 bis + 5 mm und einen Unterschied in der Gesamtlänge des Arms zwischen 5 und 27 mm. Die akromiohumerale Distanz betrug 22 mm. Eine humerale Verkürzung erhöhte das Risiko der Dislokation und führte zu einer deutlichen Verschlechterung der anterioren aktiven Elevation. Die Autoren schlussfolgerten daraus, dass eine Rekonstruktion der humeralen Länge für die postoperative Funktion entscheidend ist, um eine Dislokation zu verhindern. Es kann eine Verlängerung von 0 bis 2 cm erfolgen; darüber hinaus ist mit neurologischen Komplikationen zu rechnen.
M. subscapularis
Es fehlt eine Evidenz, um eine Subscapularisrekonstruktion zur besseren Stabilität zu belegen. Edwards et al. (2009) 22 empfehlen dennoch die Subscapularisrekonstruktion, weil sie darin einen Vorteil gegenüber der Luxationsprophylaxe sehen. Andererseits ergibt der superolaterale Zugang mit Schutz des Subscapularis eine erhöhte Luxationsrate 23. Als Nachteil der Subscapularisrekonstruktion wird unter anderem das Risiko einer Nervus-axillaris-Schädigung, eine Zunahme des Scapula-Notchings und die schwierigere Exposition bis hin zur Deltoid-Schädigung angesehen 24.
Ackland et al. (2010) 25 und Jerrett et al. (2013) 26 sehen den oberen Anteil des Muskels als Abduktor und den unteren Anteil als Adduktor an, der zu einer erhöhten Stabilität beiträgt. Edwards und Mitarbeiter (2009) 27 untersuchten 138 Patienten mit inverser Schulterprothetik und ohne Subscapularis-Rekonstruktion. Alle postoperativen Luxationen waren bei Patienten mit nicht wiederherstellbarem Subscapularis eingetreten. Auch Chalmers et al. (2014) 28 sahen als Risikofaktor einen Subscapularisdefekt und eine Revisionsoperation an.
Erfahrung des Operateurs
Walch et al. (2012) 29 verglichen 240 konsekutive inverse Prothesen, die von identischen Operateuren zwischen Mai 1995 und Juni 2003 sowie im Zeitraum zwischen Juli 2003 und März 2007 implantiert wurden. Die postoperative Komplikationsrate fiel in diesem Zeitraum von 19 % auf 10,8 %; bei Instabilitäten zeigte sich eine Reduktion von 7 % auf 3,2 % und bei Infekten von 4 % auf 0,9 %.
Therapie der instabilen inversen Schulterprothese
Allgemein wird empfohlen, nach einer Dislokation mit geschlossener Revision zunächst eine Immobilisation in einer Schlinge mit Vermeidung von Extension, Adduktion und Innenrotation durchzuführen 30. Weitaus besser ist die Versorgung der Patienten mit einer Abduktionsschiene für sechs Wochen. Kam die Luxation in Zusammenhang mit einem signifikanten Trauma zustande oder ist die Reposition nicht zu halten, müssen Prothesenpositionierung und Weichteilspannung sowie die Operationstechnik überprüft werden. Nach einer Luxation sollten mögliche Ursachen, die beeinflussbar sind, evaluiert werden. Hierzu zählen Armlänge, Weichteilspannung, Version der glenoidalen Komponente, Torsion der humeralen Komponente und das laterale glenohumerale Offset.
Teusink et al. (2014) 31 zeigten bei akuter Dislokation bei inversen Prothesen in 50 % der Fälle vorhergehende Operationen; 80 % waren bereits zuvor mit einer Endoprothese versorgt worden; 62 % waren Frühdislokationen innerhalb der ersten 90 Tage. Nach einer durchschnittlichen Nachuntersuchungszeit von 28 Monaten waren 62 % der Prothesen stabil, 29 % benötigten eine weitere Operation, 9 % verblieben instabil. Die Autoren schlussfolgerten daraus, dass bei einer ersten Luxation bei inverser Prothese eine geschlossene Reposition in etwas mehr als 50 % der Fälle mit einer anschließenden Immobilisationsphase in einer Orthese erfolgreich sein kann.
Hernandez und Mitarbeiter (2017) 32 berichteten über eine Serie von Patienten, die nach instabiler Schulterprothese eine inverse Prothese erhielten. Zwischen Januar 2004 und Juli 2017 führten die Autoren 82 Revisionen bei instabilen Schulterprothesen durch. Davon waren 62 totale Schulterprothesen, 13 Hemiprothesen und 7 inverse Endoprothesen. Die luxationsfreie Überlebensrate betrug nach 2 Jahren 87 % und nach 5 Jahren 79 %. 10 der 65 Patienten (15 %) hatten eine Luxationsepisode nach der Revisionsoperation. Eine persistierende Instabilität lag insbesondere bei Patienten mit hohem BMI (> 35 kg pro qm) und bei vorheriger Hemiprothese vor. Die Autoren schlussfolgerten daraus, dass eine inverse Prothese bei Protheseninstabilitäten eine gute Indikation darstellt. Etwa einer von 7 Patienten wird voraussichtlich eine neue Instabilität erleiden. Bei Patienten mit persistierenden Instabilitäten empfehlen die Autoren eine große Glenosphäre und eine Erhöhung des lateralen Offsets.
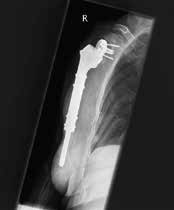
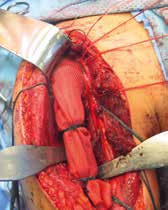
Für den Fall, dass nach adäquater Diagnostik keine Ursache für die Instabilität ermittelt werden kann, kann in Einzelfällen mit Hilfe eines Anbindungsschlauchs Stabilität erreicht werden 33 (Abb. 3). Anschließend ist nach Auffassung der Autoren die Immobilisation in einer Orthese für 3 Monate zu empfehlen.
Klinische Relevanz
Die Instabilität einer inversen Schulterprothese stellt eine klinisch relevante Komplikation mit einer Inzidenz zwischen 3 % und mehr als 10 % dar. Ein Risikofaktor ist insbesondere die fehlende Weichteilspannung. Diese kann unter anderem durch eine Verkürzung des Humerus oder durch ein reduziertes glenoidales oder humerales Offset verursacht sein. Weiterhin können eine problematische Einstellung des Glenoids (Version oder Inklination) oder des Humerus (Torsion) sowie auch Lähmungen des N. axillaris oder Frakturen im Bereich des Acromions zur Instabilität führen.
Fazit
Bei einer Instabilität gilt es, zunächst die oben dargestellten Faktoren zu evaluieren (Rotations-CT sowie ArmGanzaufnahmen im Vergleich zur Gegenseite). Finden sich hier Auffälligkeiten, sollte keine geschlossene Reposition, sondern eine operative Revision erfolgen. Lassen sich keine Auffälligkeiten ermitteln, kann eine geschlossene Reposition in etwa 50 % der Fälle erfolgreich sein. Hieran sollte sich für 6 Wochen eine Immobilisation – idealerweise in einem Abduktions-Brace – anschließen. Finden sich keine biomechanischen Auffälligkeiten im Bereich der Prothesengeometrie, kann in Einzelfällen mit einem Anbindungsschlauch eine Stabilisierung versucht werden. Danach empfehlen die Autoren bis zur narbigen Einheilung eine Brace-Anwendung für 3 Monate.
Für die Autoren:
Prof. Dr. med. Dr. h. c. Jörg Jerosch
Chefarzt der Klinik für Orthopädie,
Unfallchirurgie und Sportmedizin
Johanna-Etienne-Krankenhaus gGmbH
Am Hasenberg 46
41462 Neuss
j.jerosch@ak-neuss.de
Begutachteter Beitrag/reviewed paper
Jerosch J, Herwig M. Komplikationen und Komplikationsmanagement nach inversen Schulterendoprothesen. Orthopädie Technik, 2018; 69 (7): 46–49
- Myoelektrische Orthesenversorgung bei Plexusverletzung der oberen Extremität – Vorstellung eines hybriden bionischen Konzepts — 6. Mai 2026
- Entwicklung eines zum physiologischen Gangbild kongruenten polyzentrischen Knieorthesengelenks – Zwischenstand eines Forschungsprojektes — 10. April 2026
- Mikroprozessorgesteuerte stand- und schwungphasenkontrollierte Ganzbeinorthesen (SSCO): Entwicklung, Systeme und Versorgungsrealität in der orthopädietechnischen Praxis — 9. April 2026
- Day JS, Paxton ES, Lau E, Gordon VA, Abboud JA, Williams GR. Use of reverse total shoulder arthroplasty in the Medicare population. J Shoulder Elbow Surg, 2015; 24 (5): 766–772. doi: 10.1016/j.jse.2014.12.023
- Frankle M et al. The reverse shoulder prosthesis for glenohumeral arthritis associated with severe rotator cuff deficiency. A minimum 2‑year follow-up study of 60 patients. J Bone Joint Surg Am, 2005; 87 (8): 1697–1705. doi: 10.2106/JBJS.D.02813
- Farshad M, Gerber C. Reverse total shoulder arthroplasty – from the most to the least common complication. Int Orthop, 2010; 34 (8): 1075–1082. doi: 10.1007/s00264-010‑1125‑2
- Villacis D, Sivasundaram L, Pannell WC, Heckmann N, Omid R, Hatch GF 3rd. Complication rate and implant survival for reverse shoulder arthroplasty versus total shoulder arthroplasty: results during the initial 2 years. J Shoulder Elbow Surg, 2016; 25 (6): 927–935. doi: 10.1016/j.jse.2015.10.012
- Zumstein MA et al. Problems, complications, reoperations, and revisions in reverse total shoulder arthroplasty: a systematic review. J Shoulder Elbow Surg, 2011; 20 (1): 146–157. doi: 10.1016/j.jse.2010.08.001
- Cheung E et al. Complications in reverse total shoulder arthroplasty. J Am Acad Orthop Surg, 2011; 19 (7): 439–449
- Engesaeter LB, Lie SA, Espehaug B, Furnes O, Vollset SE, Havelin LI. Antibiotic prophylaxis in total hip arthroplasty; effects of antibiotic prophylaxis systemically and in bone cement on the revision rate of 22,170 primary hip replacements followed 0–14 years in the Norwegian Arthroplasty Register. Acta Orthop Scand, 2003; 74 (6): 644–651
- Werner CM et al. Treatment of painful pseudoparesis due to irreparable rotator cuff dysfunction with the Delta III reverseball-and-socket total shoulder prosthesis. J Bone Joint Surg Am, 2005; 87 (7): 1476–1486. doi: 10.2106/JBJS.D.02342
- Bufquin T et al. Reverse shoulder arthroplasty for the treatment of three- and four-part fractures of the proximal humerus in the elderly: a prospective review of 43 cases with a shortterm follow-up. J Bone Joint Surg (Br), 2007; 89 (4): 516–520. doi: 10.1302/0301–620X.89B4.18435
- Cazeneuve JF, Cristofari DJ. The reverse shoulder prosthesis in the treatment of fractures of the proximal humerus in the elderly. J Bone Joint Surg (Br), 2010; 92 (4): 535–539. doi: 10.1302/0301–620X.92B4.22450
- Gerber C, Pennington SD, Nyffeler RW. Reverse total shoulder arthroplasty. J Am Acad Orthop Surg, 2009; 17 (5): 284–295
- Valenti P, Boutens D, Nerot C. Delta 3 reversed prosthesis for arthritis with massive rotator cuff tear: Long term results (> 5 years). In: Walch G, Boileau P, Molé D (eds). 2000 shoulder prostheses: two to ten year follow-up. Montpellier: Sauramps Medical, 2001: 253–259
- Kohan EM, Chalmers PN, Salazar D, Keener JD, Yamaguchi K, Chamberlain AM. Dislocation following reverse total shoulder arthroplasty. J Shoulder Elbow Surg, 2017; 26 (7): 1238–1245. doi: 10.1016/j.jse.2016.12.073
- Kohan EM, Chalmers PN, Salazar D, Keener JD, Yamaguchi K, Chamberlain AM. Dislocation following reverse total shoulder arthroplasty. J Shoulder Elbow Surg, 2017; 26 (7): 1238–1245. doi: 10.1016/j.jse.2016.12.073
- Chalmers PN et al. Early dislocation after reverse total shoulder arthroplasty. J Shoulder Elbow Surg, 2014; 23 (5): 737–744. doi: 10.1016/j.jse.2013.08.015
- Padegimas EM, Zmistowski BM, Restrepo C, Abboud JA, Lazarus MD, Ramsey ML, Williams GR, Namdari S. Instability after reverse total shoulder arthroplasty: which patients dislocate? Am J Orthop (Belle Mead NJ), 2016; 45 (7): E444–E450
- Erickson BJ, Frank RM, Harris JD, Mall N, Romeo AA. The influence of humeral head inclination in reverse total shoulder arthroplasty: a systematic review. J Shoulder Elbow Surg, 2015; 24 (6): 988–993. doi: 10.1016/j.jse.2015.01.001
- Cheung E et al. Complications in reverse total shoulder arthroplasty. J Am Acad Orthop Surg, 2011; 19 (7): 439–449
- Clouthier AL, Hetzler MA, Fedorak G, Bryant JT, Deluzio KJ, Bicknell RT. Factors affecting the stability of reverse shoulder arthroplasty: a biomechanical study. J Shoulder Elbow Surg, 2013; 22 (4): 439–444. doi: 10.1016/j.jse.2012.05.032
- Henninger HB, Barg A, Anderson AE, Bachus KN, Burks RT, Tashjian RZ. Effect of lateral offset center of rotation in reverse total shoulder arthroplasty: a biomechanical study. J Shoulder Elbow Surg, 2012; 21 (9): 1128–1135. doi: 10.1016/jjse.2011.07.034
- Lädermann A, Edwards TB, Walch G. Arm lengthening after reverse shoulder arthroplasty: a review. Int Orthop, 2014; 38 (5): 991‑1000. doi: 10.1007/s00264-013‑2175‑z
- Edwards TB et al. Subscapularis insufficiency and the risk of shoulder dislocation after reverse shoulder arthroplasty. J Shoulder Elbow Surg, 2009; 18 (6): 892–896. doi: 10.1016/j. jse.2008.12.013
- Walch G, Wall B, Mottier F. Complications and revision of the reverse prosthesis: a multicenter study of 457 cases. In: Walch G, Boileau P, Molé P, Farvard L, Lévigne C, Sirveaux F (eds.). Reverse shoulder arthroplasty: clinical results, complications, revision. Montpellier: Sauramps Médical, 2006 : 335–352
- Seebauer L. Total reverse shoulder arthroplasty: European lessons and future trends. Am J Orthop (Belle Mead NJ), 2007; 36 (12 Suppl. 1): 22–28
- Ackland DC, et al. Moment arms of the shoulder musculature after reverse total shoulder arthroplasty. J Bone Joint Surg Am, 2010; 92 (5): 1221–1230. doi: 10.2106/JBJS.I.00001
- Jarrett CD, Brown BT, Schmidt CC. Reverse shoulder arthroplasty. Orthop Clin North Am, 2013; 44 (3): 389–408. doi: 10.1016/j.ocl.2013.03.010
- Edwards TB et al. Subscapularis insufficiency and the risk of shoulder dislocation after reverse shoulder arthroplasty. J Shoulder Elbow Surg, 2009; 18 (6): 892–896. doi: 10.1016/j. jse.2008.12.013
- Chalmers PN et al. Early dislocation after reverse total shoulder arthroplasty. J Shoulder Elbow Surg, 2014; 23 (5): 737–744. doi: 10.1016/j.jse.2013.08.015
- Walch G, Bacle G, Lädermann A, Nové-Josserand L, Smithers CJ. Do the indications, results, and complications of reverse shoulder arthroplasty change with surgeon’s experience? J Shoulder Elbow Surg, 2012; 21 (11): 1470–1407. doi: 10.1016/j.jse.2011.11.010
- Cheung E et al. Complications in reverse total shoulder arthroplasty. J Am Acad Orthop Surg, 2011; 19 (7): 439–449
- Teusink MJ, Pappou IP, Schwartz DG, Cottrell BJ, Frankle MA(5). Results of closed management of acute dislocation after reverse shoulder arthroplasty. J Shoulder Elbow Surg, 2015; 24 (4): 621–627. doi: 10.1016/j.jse.2014.07.015
- Hernandez NM, Chalmers BP, Wagner ER, Sperling JW, Cofield RH, Sanchez-Sotelo J. Revision to reverse total shoulder arthroplasty restores stability for patients with unstable shoulder prostheses. Clin Orthop Relat Res, 2017; 475 (11): 2716–2722. doi: 10.1007/s11999-017‑5429‑z
- Manzke M, von Engelhardt LV, Jerosch J. Rezidivierende Instabilität nach periprothetischer Humerusschaftfraktur bei inverser Schulterprothese. Der Anbindungsschlauch als zusätzliche Therapieoption? OUP, 2017; 11: 574–576. doi: 10.3238/oup.2017.0574–0576