Einleitung
Bestehen bei einem Patienten ein oder mehrere geschwollene Gelenke, kommt der exakten Anamneseerhebung eine hohe Bedeutung zu. Zu erfragen sind u. a. die Zeitdauer der vorliegenden Beschwerden, eventuell stattgehabte Traumata oder Infektionen, ggf. mit Fieberentwicklung. Im Zusammenhang mit einem opulenten Mahl kann bei bestehender Hyperurikämie ein Gichtanfall ausgelöst werden, häufig bei jungen Männern und oft auch am Knie. Patienten mit rheumatischer Erkrankung berichten vielfach über Abgeschlagenheit, eine ausgeprägte Morgensteifigkeit von mehr als 60 Minuten und vornehmlich betroffene kleine Gelenke an Händen und Füßen. Bei der Anamnese sind zudem Fragen nach einer Schuppenflechte (Angehörige?), chronisch-entzündlichen Darmerkrankungen sowie das grundsätzliche Vorkommen von Erkrankungen am muskuloskelettalen System in der Familie wichtig.
Die klinische Untersuchung beinhaltet die Beurteilung der bestehenden Gelenkschwellung sowie Überwärmung und Rötung. Die Bestimmung der Gelenkbeweglichkeit erfolgt nach der Neutral-Null-Methode (auch im Vergleich mit der Gegenseite). Der palpatorische Verdacht auf einen intraartikulären Erguss wird ggf. direkt mit einer sonographischen dynamischen Untersuchung bildgebend festgehalten und dokumentiert. Die ergänzende Laboruntersuchung erfolgt in erster Intention mit einem Blutbild, Entzündungswerten (CRP, BSG), Harnsäure sowie (zur Abklärung rheumatischer Erkrankungen) der Kontrolle der Anti-CCP-AK (ACPA) und des Rheumafaktors. Röntgenaufnahmen des betroffenen Gelenkes werden grundsätzlich in 2 Ebenen gefertigt.
Im Rahmen der Primärdiagnostik einer Gelenkschwellung ist der Ausschluss des potenziell folgenschwersten „Notfalles“ wichtig: der septischen Arthritis. Bei Verdacht (Hitze, Funktionsdefizit, massive Schmerzen, deutliche Rötung) sollte umgehend eine Punktion unter sterilen Kautelen 1 erfolgen. Dabei wird ein Abstrich zur umgehenden bakteriologischen Untersuchung entnommen, genau wie ein Direktpräparat, und in der Synovia-Analyse (u. a.) die Zellzahl bestimmt. Zeigt sich im Punktat ein putrides Sekret, ist die umgehende operative Gelenksanierung (Spiegelung/offen) angezeigt.
Reaktive Arthritis
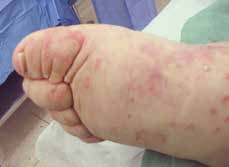
Die Reaktive Arthritis (ReA) hat eine Inzidenz von 30–40/100.000 im Jahr und tritt bei Männern und Frauen gleich häufig auf 2 3. In 70 bis 80 % der Fälle ist sie mit einem positiven HLA‑B 27 assoziiert. In der Regel treten artikuläre Schwellungen mit Synovialitiden 1 bis 6 Wochen nach stattgehabter bronchopulmonaler, urologischer oder gastrointestinaler Infektion auf. Typischerweise sind Gelenke der unteren Extremität asymmetrisch befallen, vor allem Knie oder Sprunggelenk. Meist liegt der Befall eines oder weniger Gelenke vor; nicht selten tritt eine Daktylitis auf. Extraartikuläre Manifestationen finden sich dabei u. a. an Haut (z. B. Erythema nodosum), Augen (Konjunktivitis, Keratitis, Iridozyklitis), Urogenitalsystem (Balanitis, Urethritis, Zervizitis), Schleimhäuten und – selten – an inneren Organen.
Diagnostisch entscheidend sind die Anamnese und das charakteristische klinische Bild. Im Labor erfolgt die Bestimmung der Entzündungsparameter, der Versuch des Nachweises eines Erregers (Antikörper) sowie ggf. von HLA‑B 27. Therapeutisch ist die Gabe von NSAR (nichtsteroidalen Antirheumatika) angezeigt, gelegentlich von Glukokortikoiden (systemisch oder intraartikulär), Physiotherapie und physikalische Therapie. Bei den sehr seltenen chronischen Verläufen kommen auch Methotrexat und Sulfasalazin zum Einsatz. Eine Antibiotikatherapie dient der Sanierung des zugrunde liegenden systemischen Infektes (nicht des Ergusses) und hat auf die reaktive Arthritis selbst keinerlei Einfluss.
Septische Arthritis
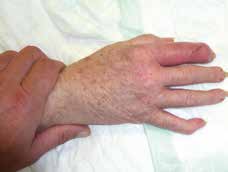
Der bakterielle arthritische Gelenkbefall stellt einen seltenen, jedoch dringlichen Notfall in der täglichen Praxis dar 4 5 6. Unterschieden werden dabei grundsätzlich primäre (exogene) Infekte – verursacht z. B. durch Punktion oder Operation bzw. nach Trauma – von sekundären (endogenen) Infekten, beispielsweise auf der Grundlage hämatogener Streuung eines gelenkfernen Bakterienbefalls (Zähne, Blasenentzündungen, Endokarditis, intravasale Katheter etc.). Das klinische Bild wird geprägt durch starke Schmerzen, eine deutliche Rötung, Schwellung, Überwärmung und Bewegungseinschränkung des Gelenkes (Abb. 1). Zusätzlich können Fieber oder – im schlimmsten Fall – eine Sepsis auftreten. In der Regel ist nur ein Gelenk befallen, in 95 % der Fälle ein großes Gelenk.
In der Labordiagnostik erfolgt die Bestimmung von Entzündungsparametern (zur differentialdiagnostischen Klärung auch der Harnsäure). Es kann ein sehr deutlicher BSG-/CRP-Anstieg vorliegen. Ein Differentialblutbild zeigt ggf. eine Leukozytose. Unverzichtbar zur sicheren Klärung ist die Punktion des betroffenen Gelenkes (unter sterilen Bedingungen!). Putrides Sekret bzw. eine Zellzahl von mehr als 50.000 gelten als Beweis für eine bakterielle Infektion. Therapeutisch sind eine umgehende operative Gelenkspülung (arthroskopisch oder offen), ggf. auch wiederholt, und eine intravenöse Antibiotikagabe angezeigt.
Gichtarthritis
Die Arthritis auf dem Boden einer Hyperurikämie (Gicht, im Endstadium mit einer entsprechenden Arthropathie) gilt in den Industrieländern als häufigste Gelenkentzündung mit einer Prävalenz von 1 bis 2 % 7 8 9. Hierbei sind (junge) Männer deutlich häufiger betroffen als Frauen (2:1 vs. 9:1).
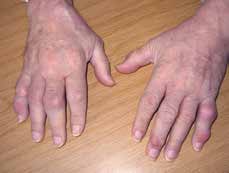
Bei zu hohem Harnsäurespiegel kommt es zur Ablagerung von Harnsäurekristallen (Uraten) im Gelenk. „Klassisch“ kommt es dabei zu einer Erstmanifestation im Rahmen einer Podagra (Großzehengrundgelenkarthritis); im weiteren Verlauf können jedoch nahezu alle Gelenke betroffen sein (Abb. 2). Klinisch ist vielfach das Knie symptomatisch. Der Patient berichtet über akut einsetzende starke bis stärkste Schmerzen. Diese treten vor allem während der Nacht bzw. am Morgen auf und gehen mit einer Erhöhung der Entzündungsparameter einher. Nur in 60 % der Fälle ist dabei eine manifeste Hyperurikämie nachweisbar (aber: doppeltbrechende intrazelluläre Kristalle im Punktat unter dem Mikroskop). Die Akuttherapie erfolgt medikamentös mittels NSAR oder Kortikoiden. Zur Prophylaxe weiterer Gichtanfälle empfiehlt sich im späteren Verlauf eine Reduktion/Normalisierung des Harnsäurespiegels durch das Absetzen auslösender Medikamente, die Anpassung des Lebensstils (purinkörperarme Ernährung) und die Gabe von Uratsenkern (z. B. Allopurinol).
Aktivierte Arthrose
Bei der Arthrose handelt es sich um degenerative Veränderungen der Gelenke. Im pathophysiologischen Mittelpunkt stehen Alterationen des hyalinen Knorpels, die (in jüngeren Jahren) vielfach traumatisch induziert werden und sich im höheren Alter symptomatisch bemerkbar machen (Schmerzen, Bewegungsdefizit, Deformitäten, Einschränkungen bei den täglichen Aktivitäten etc.). Arthrosen können klinisch – auch bei deutlichen radiologischen Alterationen – ganz blande verlaufen. Oft führen (Knorpel-)Abriebprodukte jedoch zu einer Entzündung der Schleimhaut, und eine aktivierte Situation entsteht. Diese imponiert vielfach mit einer Rötung und Überwärmung und bereitet mitunter Schwierigkeiten bei der differentialdiagnostischen Abgrenzung zu anderen akuten Gelenkschwellungen. Laborchemisch findet sich meist nur eine geringe Erhöhung der Akute-Phase-Parameter CRP und BSG. Im Röntgenbild zeigen sich die typischen degenerativen Veränderungen der Arthrose (u. a.) in Gelenkspaltverschmälerungen, Geröllzysten, subchondralen Sklerosierungen und Osteophyten.
Die konservative Behandlung der Arthrose erfolgt symptomatisch über den Einsatz von NSAR, lokale Kühlung, Stromtherapie, Bandagen, Krankengymnastik, Röntgenreizbestrahlung, (partielle) Entlastung, Schuhzurichtungen und relative Schonung. In der aktivierten Situation können Punktionen mit Infiltrationen Hilfe bringen. Zuletzt sind endoprothetische Versorgungen (respektive bei Bedarf Versteifungen) ein Segen für die Betroffenen.
Rheumatoide Arthritis
Die Rheumatoide Arthritis (RA) hat eine Häufigkeit von 0,5 bis 0,8 % in der erwachsenen Bevölkerung 10 11 12. Das mittlere Erkrankungsalter liegt zwischen dem 55. und dem 65. Lebensjahr, wobei Männer eher später erkranken als Frauen; Frauen sind jedoch dreimal häufiger betroffen als Männer.
Die Rheumatoide Arthritis tritt meist in Form einer symmetrischen Polyarthritis auf. Betroffen sind hierbei häufig die kleinen Gelenke (Fingergrund- und ‑mittelgelenke, Zehengrundgelenke); im Verlauf kann jedoch jedes Gelenk befallen sein (einschließlich der kleinen Wirbelgelenke und der Kiefergelenke) (Abb. 3). Typisch ist das Auftreten einer Morgensteifigkeit von mehr als 60 Minuten; die Symptome bestehen meist bereits über mehrere Wochen. Zusätzlich können auch rasche Ermüdbarkeit, Leistungsschwäche, Appetitlosigkeit mit Gewichtsverlust, Fieberschübe, Hyperhidrosis an den Händen, gelegentlich auch intermittierende Parästhesien in Händen und Füßen auftreten. Extraartikuläre Manifestationen sind z. B. Rheumaknoten (später), das Sicca-Syndrom der Augen sowie Glomerulonephritiden.
Die Erkrankung verläuft chronisch-progredient und führt unbehandelt zu Gelenkdestruktionen mit typischen Deformitäten. „Rheumatiker“ haben ein erhöhtes Risiko für eine kardiovaskuläre Ko-Morbidität und ein erhöhtes Infektionsrisiko (1,5- bis 15-fach). Die Mortalität ist gegenüber der Normalbevölkerung erhöht, kann jedoch heute durch eine möglichst schnelle therapeutische (medikamentöse) Einstellung praktisch normalisiert werden.
Zur diagnostischen Abgrenzung gegenüber anderen Erkrankungen wurde früher vornehmlich die Klassifikation der Amerikanischen Gesellschaft für Rheumatologie (ACR, 1987) verwendet (Tab. 1). Die Diagnose gilt als gesichert, wenn 4 von 7 Kriterien zutreffen; die Kriterien 1 bis 4 müssen hierbei mindestens 6 Wochen bestehen.
Heute werden im Allgemeinen die Klassifikationskriterien der European League against Rheumatism (EULAR) für die Diagnosesicherung einer RA genutzt, die unter bestimmten Umständen dazu geeignet sind. Folgende Voraussetzungen gelten für eine Arthritis: Es besteht eine Synovialitis (Sono-Dokumentation) ohne andere erkennbare Ursache und keine typische radiologische Erosion (damit die Klassifikationskriterien auch für das Stellen der Diagnose genutzt werden können). Es gilt: Bei einer radiologisch festgestellten Erosion besteht grundsätzlich eine rheumatoide Arthritis. Bei einem Score von 6 oder mehr Punkten wird die RA als gesichert angenommen und sofort medikamentös therapiert (Tab. 2). Dieses Vorgehen ist für eine günstige Prognose des Krankheitsverlaufes von eminenter Bedeutung.
Im Labor sind ein erhöhtes CRP sowie eine beschleunigte Blutsenkung auffällig. Der Rheumafaktor ist zur Frühdiagnostik nicht geeignet, wird aber bei 80 % der Patienten im Laufe der Erkrankung positiv. Er dient heute vor allem als Verlaufsparameter. Mit einer Spezifität von 95 % sind die ACPA ein deutlicher Hinweis auf die Entwicklung zu einer rheumatoiden Arthritis und gehen bei hohen Titern häufig mit einer ausgeprägten Gelenkdestruktion einher. In der radiologischen Untersuchung zeigen sich im Verlauf eine Gelenkspaltverschmälerung, periartikuläre Weichteilschwellungen und im fortgeschrittenen Stadium Erosionen der Gelenkflächen bis zur völligen Destruktion. Die Einteilung nach Larsen, Dale und Eek (1977) ist gängig. Sie ist für die Frühdiagnostik jedoch nicht geeignet.
Eine frühe respektive sofortige medikamentöse Therapie und Behandlung ist essentiell, da bereits aufgetretene Gelenkerosionen irreversibel sind. Diese erfolgt vornehmlich mit Methotrexat (Mittel der ersten Wahl und „Gold-Standard“) als klassischem DMARD. Alternativen bzw. Kombinationspartner bei unzureichender Wirksamkeit sind Leflunomid, Sulfasalazin und Hydroxychloroquin.
Zur Überbrückung der Zeit bis zum Wirkeintritt der DMARDs erfolgt die Akuttherapie mittels Glukokortikoiden (verhindert dabei die radiologisch fassbare Destruktion der Gelenke), nur bei Bedarf mit NSAR. Bei Therapieresistenz werden sehr rasch die sogenannten Biologika eingesetzt. Hierzu zählen TNF-α-Inhibitoren, IL1- oder IL6-Rezeptor-Antagonisten und andere. Eine sehr eng terminierte Kontrolle ist heute Standard („treat-to-target“).
Spondyloarthritiden
Die Prävalenz der sogenannten Spondyloarthritiden in Deutschland beträgt ca. 0,5 % 13 14 15. Zum Formenkreis gehören die Spondylitis ankylosans (Morbus Bechterew), die Psoriasisarthritis, Arthritiden bei chronisch-entzündlichen Darmerkrankungen, das SAPHO-Syndrom, die juvenile Spondyloarthropathie, die Lyme-Arthritis, rheumatisches Fieber und Poststreptokokkenarthritis, Arthritis bei Sarkoidose, Morbus Whipple sowie die undifferenzierte Spondyloarthropathie u. a. Als gemeinsame Symptome haben diese Erkrankungen einen Befall des Achsenskeletts mit Sakroiliitis, Spondylitis, Spondylodiszitis (nichtbakteriell), Spondylarthritis, Enthesitis der Sehnenansätze und eine periphere Oligoarthritis (vorwiegend an Gelenken der unteren Extremität) sowie spezifische Organmanifestationen wie Psoriasis an der Haut, anteriore Uveitis und entzündliche Darmveränderungen.
Man unterscheidet zwei Gruppen:
- die axiale Spondylarthritis mit vorwiegend axialen Symptomen wie entzündlichen Rückenschmerzen und Morgensteifigkeit,
- die periphere Spondylarthritis mit vorwiegend peripheren Symptomen wie Arthritis, Enthesitis oder Daktylitis (Abb. 4).
Für den „entzündlichen Rückenschmerz“ ist Folgendes charakteristisch (ASAS-Kriterien): ein Auftreten vor dem 40. Lebensjahr, Schmerzen vor allem in der zweiten Nachthälfte, Beschwerden über mehr als 3 Monate, ein gutes Ansprechen auf NSAR und eine Besserung durch Bewegung. In der bildgebenden Diagnostik ist eine im MRT nachgewiesene Sakroiliitis (STIR-Sequenz) diagnostisch entscheidend. Im Labor zeigt sich ein erhöhtes CRP; die Wahrscheinlichkeit der Diagnose wird durch ein positives HLA‑B 27 erhöht. Initial erfolgt eine Therapie mittels NSAR, die bei hoher entzündlicher Aktivität bzw. Therapieresistenz um TNF-α-Inhibitoren erweitert werden kann. Bei den peripheren Spondyloarthritiden erfolgt die Therapie meist mittels Sulfasalazin oder – bei deutlichem Gelenkbefall – Methotrexat. Auch hier können bei fehlendem Therapieerfolg Biologika zum Einsatz kommen. Zusätzlich ist eine begleitende Physiotherapie zum Funktionserhalt empfehlenswert.
Fazit
Zusammenfassend zeigt sich, dass im klinischen Alltag im Fall eines geschwollenen Gelenkes etliche Differentialdiagnosen in Betracht gezogen werden müssen. Eine ausführliche Anamnese und fundierte Untersuchung sind hierbei sehr hilfreich. Insbesondere der Ausschluss einer septischen Arthritis – als orthopädischer Notfall – hat hierbei einen hohen Stellenwert, jedoch hat das frühzeitige Erkennen und Behandeln einer Erkrankung des rheumatischen Formenkreises eine große prognostische Bedeutung.
Für die Autoren:
Verena Töppner, Assistenzärztin
Klinik für Orthopädie und Unfallchirurgie
Chefarzt: Prof. Dr. med. Stefan Rehart
Agaplesion Frankfurter Diakonie Kliniken gGmbH
Agaplesion Markus Krankenhaus
Wilhelm-Epstein-Straße 4
60431 Frankfurt am Main
verena.toeppner@fdk.info
Begutachteter Beitrag/reviewed paper
| Morgensteifigkeit von mindestens 60 Minuten Dauer |
|---|
| Gelenkschwellungen oder Gelenkerguss an mindestens 3 Gelenkregionen |
| Arthritis der Hand- und/oder Fingergelenke |
| symmetrischer Befall derselben Gelenke beider Körperhälften |
| Vorliegen von Rheumaknoten |
| positiver Rheumafaktor und/oder ACPA im Serum |
| gelenknahe Osteoporose oder Erosionen im Röntgen |
| GELENKE (0–5) | |
|---|---|
| 1 großes Gelenk | 0 |
| 2 – 10 große Gelenke | 1 |
| 1 – 3 kleine Gelenke (große Gelenke nicht gezählt) | 2 |
| 4 –10 kleine Gelenke (große Gelenke nicht gezählt) | 3 |
| > 10 Gelenke (mindestens 1 kleines Gelenk) | 5 |
| SEROLOGIE (0–3) | |
| negativer RF und negativer ACPA | 0 |
| niedrig positiver RF oder niedrig positiver ACPA | 2 |
| hoch positiver RF oder hoch positiver ACPA | 3 |
| SYMPTOMDAUER (0–1) | |
| 6 Wochen | 0 |
| ≥ 6 Wochen | 1 |
| AKUTE-PHASE-PROTEINE (0–1) | |
| normales CRP und normale BSG | 0 |
| erhöhtes CRP oder erhöhte BSG | 1 |
- Entwicklung eines zum physiologischen Gangbild kongruenten polyzentrischen Knieorthesengelenks – Zwischenstand eines Forschungsprojektes — 10. April 2026
- Mikroprozessorgesteuerte stand- und schwungphasenkontrollierte Ganzbeinorthesen (SSCO): Entwicklung, Systeme und Versorgungsrealität in der orthopädietechnischen Praxis — 9. April 2026
- Gips oder Orthese bei distalen Radiusfrakturen? — 8. April 2026
- Schett G. Frühe rheumatoide Arthritis. Der Internist, 2008, 49 (3): 263–270
- Rehart S, Henniger M, Bernateck M. Rheumatische Gelenk- und Weichteilerkrankungen. In: Wirth C, Mutschler W, Kohn D, Pohlemann T (Hrsg.). Praxis der Orthopädie und Unfallchirurgie. 3., vollständig überarbeitete Auflage. Stuttgart: Thieme-Verlag, 2013
- Zink A, Minden K, List SM (Hrsg.). Entzündlich-rheumatische Erkrankungen. Berlin: Robert Koch-Institut, 2010 (Gesundheitsberichterstattung des Bundes, 49)
- Diefenbeck M, Abitzsch D, Hofmann GO. Die Gelenkinfektion. Der Unfallchirurg, 2012, 115 (6): 489–495
- Deutsche Gesellschaft für Unfallchirurgie e. V. (DGU). S1-Leitlinie „Bakterielle Gelenkinfektionen“ (AWMF-Leitlinienregister 012/010). Stand: 05.06.2014, gültig bis 14.06.2019. http://www.awmf.org/uploads/tx_szleitlinien/012–010l_S1_Bakterielle_Gelenkinfektionen_2014-06.pdf
- Henniger M, Jahn-Mühl B, Rehart S. Septische Arthritiden – Wandel des Erregerspektrums und Rolle des orthopädischen Rheumatologen. Aktuelle Rheumatologie, 2015; 54 (3): 202–208
- Mikuls TR, Farrar JT, Bilker WB, Fernandes S, Schumacher HR, Saag KG. Gout epidemiology: results from the UK General Practice Research Database, 1990–1999. Annals of the Rheumatic Diseases, 2005; 64 (2): 267–272
- Deutsche Gesellschaft für Rheumatologie. S2e-Leitlinie „Gichtarthritis – fachärztliche Versorgung“ (AWMF-Leitlinienregister Nr. 060/005). Stand: 30.04.2016, gültig bis 31.12.2020. http://www.awmf.org/uploads/tx_szleitlinien/060–005l_S2e_Gichtarthritis_2016-08.pdf
- Deutsche Gesellschaft für Allgemeinmedizin und Familienmedizin (DEGAM). S1-Leitlinie „Gicht: Häufige Gichtanfälle und Chronische Gicht in der hausärztlichen Versorgung“ (AWMF-Leitlinienregister 053/032a). Stand: 30.09.2013 (in Überarbeitung), gültig bis 30.09.2018. http://www.awmf.org/uploads/tx_szleitlinien/053–032al_S1_Chronische_Gicht_2014-05.pdf
- Schett G. Frühe rheumatoide Arthritis. Der Internist, 2008, 49 (3): 263–270
- Schneider M, Lelgemann M, Abholz H‑H, Caratti R, Flügge C, Jäniche H, Kunz R, Krüger K, Rehart S, Specker C. Interdisziplinäre Leitlinie Management der frühen rheumatoiden Arthritis. Berlin u. a.: Springer-Verlag, 2007
- Rehart S, Henniger M. Rheumatische Erkrankungen. Orthopädie und Unfallchirurgie up2date 7, 2012; (02): 147–162
- Deutsche Gesellschaft für Rheumatologie e. V. (DGRh). S3-Leitlinie „Axiale Spondyloarthritis inklusive Morbus Bechterew und Frühformen“ (AWMF-Leitlinienregister 060/003). Stand: 30.11.2013 (in Überarbeitung), gültig bis 30.11.2018. http://www.awmf.org/uploads/tx_szleitlinien/060–003l_S3_Axiale_Spondyloarthritis_Morbus_Bechterew_2013-11.pdf
- Poddubnyy D, Sieper J. Diagnostik und Klassifikation der Spondyloarthritiden 2012. Aktuelle Rheumatologie, 2013; 38 (2): 86–91
- Braun J, Pincus T. Krankheitsverlauf bei Patienten mit Spondylitis ankylosans und Mortalität. In: Braun J, Sieper J (Hrsg.). Spondylitis ankylosans. Bremen: Uni-Med Verlag, 2002: 40–47