Als etablierte Diagnosen gelten die Behandlung von iliosakralgelenkbedingten Beschwerden, Beckenringfrakturen, Sakrumfrakturen, Instabilitäten des Beckenringes sowie schwangerschaftsassoziierten Beschwerden. Auch in der Frührehabilitation von Patienten mit Totalendoprothesen des Hüftgelenkes hat sich der Einsatz von Beckenkompressionsbandagen bewährt. Für die Behandlung der Trochantertendopathie gibt es positive Erfahrungen. Studien oder größere Anwendungsbeobachtungen stehen hier allerdings noch aus. Zusammengefasst stellen Kompressionsorthesen eine wertvolle Bereicherung des therapeutischen Repertoires zur Behandlung eines breiten Spektrums von Erkrankungen des Beckens dar. Weitere Studien sind erforderlich, um die Wirksamkeit von Beckenbandagen bei der Behandlung von Affektionen des Beckens besser validieren zu können.
Einleitung
Das Konzept der Behandlung verschiedener muskuloskelettaler Pathologien des Beckens mittels Kompressionsorthesen findet seinen Ursprung im alten Ägypten. Dort wurde bereits um das Jahr 5000 v. Chr. bei überwiegend traumatologischen Indikationen ein Verband aus zirkulären und unter Zug verknoteten Papyrusbinden eingesetzt 1. Seitdem findet eine stetige Weiterentwicklung dieser seit jener Zeit bewährten Behandlungsmethode statt. Heute existiert eine Vielzahl verschiedenster Orthesen, die sich hinsichtlich ihres biomechanischen Wirkungsprinzips, ihrer Indikation und ihrer wissenschaftlichen Evidenz erheblich unterscheiden. Im Folgenden wird diesbezüglich ein Überblick über sechs ausgewählte Einsatzgebiete vermittelt.
Material und Methoden
Ausgangspunkt der Untersuchung ist eine extensive Literaturrecherche sowie die Berücksichtigung von Expertenmeinungen zum Einsatz kommerzieller Beckenbandagen von Juni 1995 bis April 2016. Ausgewertet wurden alle relevanten in der Fachliteratur publizierten Studien mit den Stichworten „pelvic binder“, „pelvic compression“, „bandage“, „Beckenkompression“ und „Beckenorthese“. Die Datenlage wurde in Abhängigkeit von den jeweiligen Indikationen aufgeschlüsselt.
ISG-Syndrom
Unspezifische Rückenschmerzen gelten als zweithäufigste Schmerzursache im deutschen Gesundheitswesen. In 10 bis 62 % der Fälle werden die Iliosakralgelenke (ISG) als Ursache für diesen Schmerz identifiziert 2 3. Das Beschwerdebild unterliegt häufig einer multifaktoriellen Pathogenese, die sowohl intra- als auch extraartikuläre Faktoren beinhaltet. Als mögliche Ursachen werden in diesem Zusammenhang vorrangig degenerative Veränderungen, posttraumatische oder kongenitale Deformitäten der ISG, entzündliche Erkrankungen, Z. n. lumbosakraler Fusion, Beinlängendifferenzen und Infektionen angeführt 4 5.
Trotz seiner klinischen Signifikanz gibt es keinen universell akzeptierten Goldstandard, um das ISG differentialdiagnostisch von den Facettengelenken und Bandscheiben als Schmerzursache abzugrenzen. Die empfohlenen Diagnosestandards sehen jeweils drei positive Provokationstests 6 bzw. zwei positive intraartikuläre Testblockaden mit unterschiedlich lang wirkenden Lokalanästhetika unter Sicherung der korrekten Lage der Injektionskanüle mittels Kontrastmittel unter Bildwandlerkontrolle vor (Abb. 1). Diese invasiven diagnostischen Verfahren stellen zwar die beste verfügbare Methode zur Diagnosesicherung dar, jedoch verlieren sie aufgrund der hohen Invasivität und des Mangels an Praktikabilität in der alltäglichen Praxis an Bedeutung 7.
Die Erstlinientherapie des ISG-Syndroms erfolgt konservativ. Kompressionsorthesen stellen eine etablierte Behandlungsmethode mit guter Evidenz dar, welche die Lebensqualität der Patienten verbessern kann (s. Abb. 1) 8 9. Prospektive Studien zu ihrer Wirksamkeit gibt es derzeit jedoch nicht. Weitere Behandlungsoptionen sind der Einsatz von Physiotherapie, intraartikulären Infiltrationen und Radiofrequenzbehandlungen sowie die operative Versteifung des Gelenks.
Beckenringfrakturen
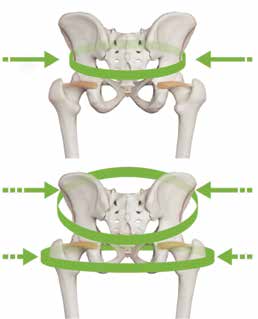
Frakturen des Beckenringes sind ein häufiges Krankheitsbild im klinischen Alltag. Als zugrundeliegende Pathologie lässt sich in diesem Zusammenhang in der Mehrzahl der Fälle eine Osteoporose identifizieren, seltener sind auch Hochrasanztraumen ursächlich. In der Akutversorgung steht die Verringerung der Mortalität im Vordergrund. Diese liegt bei allen Patienten mit Beckenringfraktur bei 5 bis 30 % und wird maßgeblich durch den unmittelbar durch die Fraktur verursachten Blutverlust beeinflusst, der bis zu 5.000 ml betragen kann. Im Falle eines hierdurch bedingten Volumenmangelschocks steigt die Mortalität auf 42 % an. Die Wirksamkeit des Einsatzes von Kompressionsorthesen zur Verminderung der Mortalität ist gut belegt. Ferner konnte gezeigt werden, dass Beckenorthesen in der Lage sind, die normale knöcherne Anatomie wiederherzustellen 10 11 12 13. Vor diesem Hintergrund gehören Beckenkompressionsschlingen zur Basisausstattung in der Versorgung polytraumatisierter Patienten. Seit der Implementierung der ersten Beckenkompressionsorthese (Geneva Belt) zur Frakturkonsolidierung durch Vermeulen et al. im Jahre 1999 wurden zahlreiche weitere Modelle entwickelt. Als Beispiele sind hier der Stuart-Splint, der London-Splint, der Dallas Pelvic Binder, das Trauma Pelvic Orthotic Device (T‑POD) und die Basko-Beckenbandage zu nennen. Diese werden generell auf Höhe der Trochanteren sowie der Symphysis pubis angewendet 14.
Sakrumfrakturen
Frakturen des Kreuzbeines sind für 45 % aller Beckenfrakturen verantwortlich. Überwiegend bestehen dabei osteoporotische Insuffizienzfrakturen, erst an zweiter Stelle rangieren Unfälle als Ursache 15. Aufgrund des unspezifischen klinischen Bildes bei häufig fehlendem Trauma, Schmerzen beim Gehen und eventuell bekannter Osteoporose handelt es sich hierbei um eine unterdiagnostizierte Erkrankung. Auf Nativ-Röntgenaufnahmen sind die Frakturen zudem zumeist nicht zu erkennen, sodass die Diagnose häufig nur mittels Computertomographie gestellt werden kann. Die überwiegende Mehrzahl der Sakrumfrakturen kann konservativ therapiert werden. Hierbei wird zur Verringerung der Komplikationsrate und zur Verbesserung des Behandlungsergebnisses eine schnelle Frühmobilisation angestrebt. Die Therapie beinhaltet neben adäquater Schmerztherapie sowie einer medikamentösen Behandlung der Osteoporose die Ruhigstellung der Fraktur mittels Kompressionsorthese 16. Dass letztere Vorgehensweise den Schmerzmittelbedarf deutlich senkt, ist weitestgehend unumstritten. Es liegt jedoch bis dato keine aussagekräftige Studie vor, die dies untersucht.
Schwangerschaftsassoziierte Beschwerden im Beckenbereich
Jede zweite Frau erleidet während der Schwangerschaft mindestens eine Episode unspezifischer Schmerzen des Beckens. Bei einem Drittel dieser Patientinnen sind die Schmerzen so stark, dass hierdurch die Lebensqualität beeinflusst wird. Man geht auch bei diesem Beschwerdebild von einer multifaktoriellen Pathogenese aus, deren Mechanismus noch inkomplett verstanden ist. Verschiedene biomechanische Modelle ziehen jedoch eine Verlagerung des Körperschwerpunkts aufgrund der Gewichtszunahme mit konsekutiver Mehrbelastung des lumbosakralen Übergangs und der ISG sowie einer erhöhten Ermüdung der Stützmuskulatur in Erwägung. Die Behandlung mittels stabilisierender Beckenbandagen kann durch Physiotherapie, Nervenstimulation, medikamentöse Schmerztherapie, Massage und Bewegungstherapie komplettiert werden 17 18.
Die Wirksamkeit von Beckenbandagen in der Behandlung dieser Beschwerden ist in mehreren Studien belegt, wobei Hu et al. die verminderte Beweglichkeit in den ISG sowie die Zunahme der Schließkraft des Beckenringes dafür verantwortlich machen konnten 19. Mens et al. wiesen darauf hin, dass die Beckenkompression kaudal zur Spina iliaca anterior superior erfolgen muss 20. Auch das Royal College of Obstetricians and Gynaecologists empfiehlt bei schwangerschaftsassoziierten Beckenbeschwerden den Einsatz von Beckenorthesen 21.
Postoperative Versorgung von Hüftendoprothesen
In Deutschland werden pro Jahr ca. 200.000 künstliche Hüftgelenke implantiert. Die sofortige postoperative Versorgung mit einem Kompressionsverband um Becken und betroffenen Oberschenkel mittels Kornährenverband ist geläufige Therapie.
Neuere Untersuchungen ergeben, dass suffiziente Beckenkompressionsbandagen in der Lage sind, die Häufigkeit von Re-Operationen aufgrund septischer Komplikationen zu reduzieren sowie die Wundheilung zu verbessern. Ferner wurde angemerkt, dass sich eine Vielzahl qualitativ unzureichender Produkte auf dem Markt befindet 22.
Trochantertendopathie
Synonyme sind Bursitis trochanterica, oberes Tractus-Scheuersyndrom sowie „greater trochanteric pain syndrome“ (GTPS). Die Prävalenz der Trochantertendopathie liegt bei 15,0 % . Leitsymptom dieses Krankheitsbildes sind Schmerzen im äußeren Hüftbereich mit Druckschmerz über dem großen Trochanter 23. Das typische klinische Bild ergibt sich aus der Zusammenschau von Anamnese, körperlichem Untersuchungsbefund und den entsprechenden apparativen Befunden. Differentialdiagnostisch müssen vertebrale sowie intra- und extraartikuläre Pathologien der Hüfte ausgeschlossen werden. Die definitive Diagnose wird mittels MRT gestellt.
Die Erkrankung kann in einer Vielzahl der Fälle erfolgreich konservativ behandelt werden. Operative Verfahren sind refraktären Therapieverläufen vorbehalten. Die Erfolgsrate konservativer Maßnahmen liegt in Abhängigkeit vom Patientenkollektiv zwischen 49 und 100 % 24. Diese umfassen v. a. Krankengymnastik mit Dehnungsbehandlungen, lokale Infiltrationen mit entzündungshemmenden Substanzen, NSAR und Stoßwellenbehandlung. Für die Behandlung des Syndroms mit einer Beckenkompressionsorthese gab es bisher kaum wissenschaftlich fundierte Daten 25 26. In einer eigens durchgeführten Single-Center-Studie an 27 Patienten, die konservativ erfolglos vorbehandelt waren, gaben 19 eine wesentliche (> 50 %) Besserung der Schmerzen durch eine dreimonatige Anwendung einer Beckenbandage an, die Kompression über den Trochanteren ausübt. Die Publikation der Studie wird für Dezember 2016 erwartet. Für die Besserung der Beschwerden sehen die Untersucher im Wesentlichen zwei Erklärungsmöglichkeiten: Zum einen kann die Bandage das Rutschen des Tractus iliotibialis über den großen Trochanter reduzieren, indem sie diesen durch äußere Druckeinwirkung fixiert. Dies würde dem Bild des „oberen Tractus-Scheuersyndroms“ als Pathomechanismus entsprechen. Zum anderen führt die Bandage auch zu einer Kompression der Glutealmuskulatur, was zu einer Entlastung der Muskelansätze am großen Trochanter führt.
Interessenkonflikt
Der Hauptautor besitzt Gebrauchsmusterschutz auf eine Beckenkompressionsbandage, die von Basko Health Care vermarktet wird.
Für die Autoren:
Dr. med. Fritjof Schmidt-Hoensdorf
Orthopäde und Unfallchirurg
Bajuwarenstr. 7, 85435 Erding
fschmidth@t‑online.de
Begutachteter Beitrag/reviewed paper
Schmidt-Hoensdorf F, Schmidt-Hoensdorf T. Zum Einsatz von Beckenkompressionsbandagen in Orthopädie und Unfallchirurgie. Orthopädie Technik, 2016; 67 (12): 42–44
- Die orthopädietechnische Versorgung mit einer dynamischen Fingerstreckorthese als eigenständige Therapie bei der Dupuytren’schen Kontraktur — 26. März 2026
- Vergleichende Prüfung konventioneller und additiv gefertigter Prothesenschäfte in Anlehnung an DIN EN ISO 10328:2016 — 10. März 2026
- Easypreg – ein Faserverbundwerkstoff zum Tiefziehen — 9. März 2026
- Stahel PF, Hammerberg EM. History of pelvic fracture management: a review. World J Emerg Surg, 2016; 11: 18
- Simopoulos TT, Manchikanti L, Singh V, Gupta S, Hameed H, Diwan S, et al. A systematic evaluation of prevalence and diagnostic accuracy of sacroiliac joint interventions. Pain Physician, 2012; 15 (3): E305–E344
- Forst SL, Wheeler MT, Fortin JD, Vilensky JA. The sacroiliac joint: anatomy, physiology and clinical significance. Pain Physician, 2006; 9 (1): 61–67
- Cohen SP, Chen Y, Neufeld NJ. Sacroiliac joint pain: a comprehensive review of epidemiology, diagnosis and treatment. Expert Rev Neurother, 2013; 13 (1): 99–116
- Shaffrey CI, Smith JS. Stabilization of the sacroiliac joint. Neurosurg Focus, 2013; 35 (2 Suppl): Editorial
- Cohen SP, Chen Y, Neufeld NJ. Sacroiliac joint pain: a comprehensive review of epidemiology, diagnosis and treatment. Expert Rev Neurother, 2013; 13 (1): 99–116
- Simopoulos TT, Manchikanti L, Singh V, Gupta S, Hameed H, Diwan S, et al. A systematic evaluation of prevalence and diagnostic accuracy of sacroiliac joint interventions. Pain Physician, 2012; 15 (3): E305–E344
- Cohen SP, Chen Y, Neufeld NJ. Sacroiliac joint pain: a comprehensive review of epidemiology, diagnosis and treatment. Expert Rev Neurother, 2013; 13 (1): 99–116
- Huijbregts PA. Evidence-based diagnosis and treatment of the painful sacroiliac joint. J Man Manip Ther, 2008; 16 (3): 153–154
- Scott I, Porter K, Laird C, Greaves I, Bloch M. The prehospital management of pelvic fractures: initial consensus statement. Emerg Med J, 2013; 30 (12): 1070–1072
- Krieg JC, Mohr M, Mirza AJ, Bottlang M. Pelvic circumferential compression in the presence of soft-tissue injuries: a case report. J Trauma, 2005; 59 (2): 470–472
- Pavic R. Use of the trauma pelvic orthotic device (T‑POD) for provisional stabilisation of anterior-posterior compression type pelvic fractures: a cadaveric study [Injury, Int J Care Injured 2008; 39: 903–6]. Injury, 2009; 40 (6): 673; author reply 673–674
- Prasarn ML, Horodyski M, Conrad B, Rubery PT, Dubose D, Small J, et al. Comparison of external fixation versus the trauma pelvic orthotic device on unstable pelvic injuries: a cadaveric study of stability. J Trauma Acute Care Surg, 2012; 72 (6): 1671–1675
- Scott I, Porter K, Laird C, Greaves I, Bloch M. The prehospital management of pelvic fractures: initial consensus statement. Emerg Med J, 2013; 30 (12): 1070–1072
- Tsiridis E, Upadhyay N, Giannoudis PV. Sacral insufficiency fractures: current concepts of management. Osteoporos Int, 2006; 17 (12): 1716–1725
- Longhino V, Bonora C, Sansone V. The management of sacral stress fractures: current concepts. Clin Cases Miner Bone Metab, 2011; 8 (3): 19–23
- Perkins J, Hammer RL, Loubert PV. Identification and management of pregnancy-related low back pain. J Nurse Midwifery, 1998; 43 (5): 331–340
- Katonis P, Kampouroglou A, Aggelopoulos A, Kakavelakis K, Lykoudis S, Makrigiannakis A, et al. Pregnancy-related low back pain. Hippokratia, 2011; 15 (3): 205– 210
- Hu H, Meijer OG, van Dieen JH, Hodges PW, Bruijn SM, Strijers RL, et al. Muscle activity during the active straight leg raise (ASLR), and the effects of a pelvic belt on the ASLR and on treadmill walking. J Biomech, 2010; 43 (3): 532–539
- Mens JM, Damen L, Snijders CJ, Stam HJ. The mechanical effect of a pelvic belt in patients with pregnancy-related pelvic pain. Clin Biomech (Bristol, Avon), 2006; 21 (2): 122–127
- Royal College of Obstetricians & Gynaecologists. Pelvic girdle pain and pregnancy. 2015. https://www.rcog.org.uk/globalassets/documents/patients/patient-information-leaflets/pregnancy/pi-pelvic-girdle-pain-and-pregnancy.pdf (Zugriff am 25.10.2016)
- Labek G, Hipmair G, Utermann A, Hinterreiter E, Böhler N. Influence of compression bandage on wound healing after total hip arthroplasty. Orthopaedic Proceedings, 2006; Supp I: 40. Abstract: http://www.bjjprocs.boneandjoint.org.uk/content/88‑B/SUPP_I/40.3 (Zugriff am 25.10.2016)
- Segal NA, Felson DT, Torner JC, Zhu Y, Curtis JR, Niu J, et al. Greater trochanteric pain syndrome: epidemiology and associated factors. Arch Phys Med Rehabil, 2007; 88 (8): 988–992.
- Arnold I, Guttke T. Perikoxale Schmerzsyndrome – nicht immer einfach zu diagnostizieren. Ursachen und therapeutische Aspekte. Arthritis und Rheuma, 2016; 36 (1): 9–14. Abstract: http://www.schattauer.de/de/magazine/uebersicht/zeitschriften-a‑z/arthritis-rheuma/inhalt/archiv/issue/2306/manuscript/25497/show.html (Zugriff am 25.10.2016)
- Lustenberger DP, Ng VY, Best TM, Ellis TJ. Efficacy of treatment of trochanteric bursitis: a systematic review. Clin J Sport Med, 2011; 21 (5): 447–453
- Williams BS, Cohen SP. Greater trochanteric pain syndrome: a review of anatomy, diagnosis and treatment. Anesth Analg, 2009; 108 (5): 1662–1670