Einleitung: Geschichte der Osseointegration
Bis in die Antike reichende Beschreibungen zeigen Versuche, die verlorene Funktion nach einer Amputation durch technische Hilfsmittel zu ersetzen. Zur Sicherung der privaten und beruflichen Selbstständigkeit sind prothetische Versorgungen aus der heutigen Zeit nicht mehr wegzudenken. Geht es beim Verlust des Armes um die bestmögliche Wiederherstellung der Greif- und Haltefunktion, hat die Beinprothese die Aufgabe, den Anwender zu tragen und zu bewegen. Dabei sei aber bedacht, dass ein Amputationsstumpf aus biologischer Sicht kein optimaler Lastträger ist und es immer zu unphysiologischen Belastungen der Weichteile, der Knochen und der angrenzenden Gelenke kommt. Eine Beinprothese muss dabei die konträren und schwierigen Aufgaben, in der Standphase bestmögliche Standsicherheit und in der Schwungphase eine optimale Bewegung zu ermöglichen, sicher meistern. Zudem darf es auch nicht zum Prothesenverlust mit daraus resultierender Sturzneigung kommen.
Durch die mechanischen Belastungen kommt es immer wieder zu Beeinträchtigungen des Amputationsstumpfes mit der Folge einer eingeschränkten Prothesennutzbarkeit. Dies führt nicht selten dazu, dass Prothesenanwender nicht immer wunschgemäß ihren täglichen Aktivitäten nachgehen können und den Tagesablauf immer “um die Prothesennutzung herum” planen. Der Traum, die Prothese direkt mit dem Knochen zu verbinden, besteht daher schon seit Langem. Die unmittelbare Kontrolle der Prothese verspricht eine wesentliche Verbesserung der Prothesennutzung sowie geringere Einschränkungen der angrenzenden Gelenke und somit der Lebensqualität.
Bereits 1843 sammelte der französische Chirurg Joseph-François Malgaigne Erfahrungen mit Metallstiften, die durch die Haut und unmittelbar in den Knochen geführt wurden. Damals war noch das Ziel – ähnlich dem Fixateur externe heutzutage, komplizierte Brüche über Wochen zu stabilisieren. Unabhängige Versuche, Prothesen am Knochen zu befestigen, unternahmen in den 1940er Jahren der deutsche Arzt Dümmer bei vier Patienten sowie die Chirurgen Elliott, Cutler und Blodgett in den USA bei Hunden. Die damaligen Implantate konnten jedoch aufgrund des Implantatmaterials noch nicht osseointegriert werden. Ein Biofilm zwischen Implantat und Knochen führte langfristig zum infektionsbedingten Implantatverlust. So beschrieb Dümmer, dass er alle vier Implantate wieder entfernen musste 1.
In den 40er Jahren des vergangenen Jahrhundert wurden etliche Untersuchungen, unter anderem mit Vitallium (Legierung aus Kobalt, Chrom und Molybdän) unternommen, um die Biokompatibilität von Legierungen bei Implantaten zu untersuchen 2. Der schwedische Orthopäde Per-Ingvar Brånemark unternahm in den 1960er Jahren Experimente an Kaninchen, um Messungen der Knochendurchblutung vorzunehmen. Zufällig entdeckte er damals eine sich entwickelnde Knochen-Implantat-Verbindung, die nur durch mechanische Gewalt wieder getrennt werden konnte. Er benutzte Titanimplantate und bezeichnete dieses Phänomen als “Osseointegration”. Brånemark entwickelte aus dieser Erkenntnis heraus erste auf Dauer in den Kiefer eingebrachte Titanimplantate, welche die Schleimhaut durchdringen und eine Zahnprothetik mechanisch fest am Kiefer verankern 3. Die weitere chirurgische und materialtechnische Entwicklung mündete in den folgenden Jahrzehnten in die heutige Standardversorgung: die Osseointegration von Dentalimplantaten zum Tragen von Zahnprothesen.
Rickard Brånemark, der Sohn von Per-Ingvar Brånemark, entwickelte ein Implantat zur Verankerung von Exoprothesen bei Menschen mit transfemoraler Amputation. 1990 wurde bei einer Patientin mit doppelter Amputation die erste beständige Osseointegration bei Prothesen der unteren Extremität durchgeführt. Mittlerweile werden in Schweden Patienten nach dem OPRA-3-Protokoll (OPRA = Osseointegrated Prostheses for the Rehabilitation of Amputees) betreut. Das Vorgehen ist von der präoperativen Planung bis zum Abschluss der Rehabilitation standardisiert.
Über die Jahre entwickelte sich die Technik der Osseointegration weiter. In den 90er Jahren entwickelte eine Arbeitsgruppe aus Lübeck um Horst-Heinrich Aschoff und Hans Grundei ein völlig neues Implantatdesign: Im Gegensatz zum aus der Dentalchirurgie übernommenen Prinzip des eingeschraubten schwedischen Implantates wurde dabei ein Implantat analog zur Vorgehensweise bei Endoprothesenstielen entwickelt. Sowohl die Zentren in Schweden als auch in Lübeck wurden von zahlreichen weiteren Arbeitsgruppen besucht. Mittlerweile existieren etwa zehn Zentren weltweit, die transkutan osseointegrierte Prothesensysteme (TOPS) anbieten. Es besteht kein weltweites Register, aber anlässlich der OT-World 2018 schätzten verschiedene Referenten etwa insgesamt 800 bis 1000 durchgeführte Versorgungen mittels TOPS.
Wichtige weltweite Zentren und deren Implantatdesigns
Es existieren aktuell verschiedenste TOPS; allen Systemen gemeinsam ist aber der grundsätzliche Aufbau: In einem chirurgischen Eingriff wird ein enostales Implantat. Es wird demnach osseointegriert. Das Implantat wird über Verbindungsmodule mit einem speziellen Adapter und anschließend einer Exoprothese verbunden. Die meisten Systeme verfolgen das Ziel möglicher Standardkonnektionen, beispielsweise mittels Pyramidenadapter. Im Folgenden werden verschiedene, käufliche Implantatvarianten angeführt:
Göteborg (Schweden): OPRA-Implantat (Osseointegrated Prostheses for the Rehabilitation of Amputees)
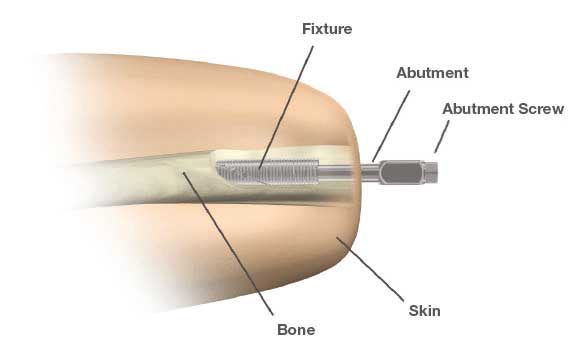
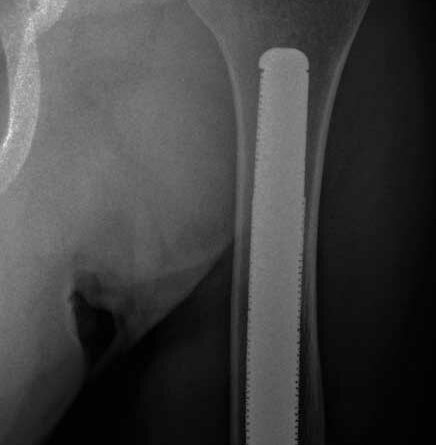
Im Department of Orthopaedics der Universität Gothenburg nutzt Rickard Brånemark das OPRA-Implantat der Firma Integrum. Mit diesem TOPS bestehen die längsten Erfahrungswerte. Die enostale Komponente wird analog zu Dentalimplantaten in den Markraum des Knochens geschraubt. Am distalen Ende ist das Implantat mit einem Innengewinde versehen, um das kutane Verbindungsstück (Abutment) aufzunehmen. Dabei besteht allerdings aus Sicht der Autoren aufgrund des aus dieser Konstruktion resultierenden maximalen möglichen Durchmessers des Abutments eine mögliche mechanische Schwachstelle (Abb. 1).
Hannover: Endo-Exo-Prothese nach Grundei
Im Fachbereich Endo-/Exoprothetik der Klinik für Unfallchirurgie der Medizinischen Hochschule Hannover setzt Horst-Heinrich Aschoff seine in Lübeck begonnene Arbeit fort. Mittlerweile hat er in fast 20 Jahren über 150 Versorgungen durchgeführt. Im Rahmen des TOPS-Konzeptes werden sowohl Standardimplantate als auch Custom-made-Implantate der Firma ESKA Orthopaedic GmbH verwendet. Die enostalen Implantate zeichnen sich durch eine besondere Oberflächenstruktur aus, welche die Osseointegration begünstigen. Eine Beschreibung erfolgt weiter unten. Die Arbeitsgruppe um Aschoff wurde von Teams aus den USA, den Niederlanden und Australien besucht. Hieraus entstanden weitere Zentren mit eigenen Implantaten, die das Grundprinzip der Endo-Exo-Prothese nach Aschoff/ Grundei übernahmen.
Nijmegen (Niederlande): Custom-made-Implantate/3D-Titandruckverfahren
Im Radboud Universitair Medisch Centrum im niederländischen Nijmegen wurde zunächst mit dem OPRA-Implantat und einem Endo-Exo-Prothesensystem gearbeitet. Seit 2015 wird das in Australien verwendete Implantat (OPL) verwendet. Für kurze knöcherne Stumpfverhältnisse werden Custom-made-Implantate mit einem Titan-3D-Drucker produziert (Radboud University Medical Centre 3D Laboratory Nijmegen, Niederlande) (Abb. 2).
Salt Lake City (Utah, USA): DLPOPS (Distally Loading Percutaneous Osseointegrated Prosthetic System)
Dieses Implantat wurde vom Orthopaedic Research Laboratory University Orthopaedic Center Salt Lake City in den USA entwickelt. Das Endomodul dieses Systemes integriert knöchern im Gegensatz zur Endo-Exo-Prothese auf einer deutlich kürzeren Strecke. Zudem ist die Integration unmittelbar am knöchernen Stumpfende, in der lasttragenden Ebene, vorgesehen. Der Direkter des Orthopedic Research Laboratory der Universität Utah, Kent Bachus, war maßgeblich an der Entwicklung dieses Implantates beteiligt. 2016 wurde eine Zulassungsstudie unter Aufsichtder FDA an 10 Soldaten gestartet. Endgültige Langzeitergebnisse für dieses Implantat stehen noch aus (Abb. 3).
Sydney (Australien):OGAP-OPL (Osseointegration Group of Australia Osseointegration Prosthetic Limb)
Die Osseointegration Group of Australia (OGA) unter der Leitung von Munjed Al Muderis mit Sitz in Sydney hat ein Implantat entwickelt, das dem Endo-Exo-Prothesensystem ähnlich ist. Das Grundprinzip der rauen Oberfläche wurde übernommen, die grundsätzliche Stielform des Endomodules ebenso. Die OGA hat sowohl landesweite als auch internationale Kooperationspartner; Al Muderis berichtete in einem Vortrag von über 260 Versorgungen allein in Sydney. Im Gegensatz zu den anderen Zentren führt die OGA auch ein Behandlungsprotokoll mit einem einzeitigen operativen Vorgehen durch (OGAAP‑2) (Abb. 4) 4.
Pittsburgh (Pennsylvania, USA): Biomed Compression System
An der Universität Pittsburgh führt Rickard McGough ein völlig anderes Konzept durch. Dieses System geht aus einer Zulassung für Endoprothesen der Firma Biomed hervor. Das enostale Modul besteht aus einer proximalen Komponente, die analog zu osteosynthetischen Versorgungen mit Verriegelungsstiften fixiert wird. Distal wird das Implantat von einer tellerartigen Komponente begrenzt, die durch eine Schraubverbindung gegen den Knochen gepresst wird und den perkutanen Verbindungsadapter aufnimmt. Nach Auffassung der Autoren ist die Osseointegration bei diesem Implantat vermutlich nicht vergleichbar mit den anderen Systemen: Es fehlt an der lastaufnehmenden rauen Oberflächenstruktur. Sollte es zu keiner Osseointegration des Implantates kommen, ist die Stabilisierung mittels proximaler Verriegelung bruchgefährdet. Es muss unweigerlich nach vielen Lastzyklen zur Materialermüdung kommen, wenn keine hinreichende zusätzliche Stabilität durch Osseointegration besteht. Nach den bekannten Publikationen wurden bisher 13 Versorgungen mit diesem TOPS vorgenommen. Die Langzeitergebnisse bleiben abzuwarten 5 (Abb. 5).
Grundzüge der Osseointegration
Die direkte eingeheilte Verbindung zwischen Implantat und Knochen wird als “Osseointegration” bezeichnet. Die Abläufe der Osseointegration ähneln denen nach Knochenbrüchen und auch denen während des Knochenwachstums. Da es sich bei den Implantaten nicht um biologisches Material handelt, kann das Immunsystem jedoch einen entscheidenden Störfaktor darstellen. Und nur ein ungestörtes Einheilen kann den langfristigen Erfolg des Implantates sichern. Bei vielen Materialien findet daher eine sogenannte Fremdkörperreaktion statt: Es kommt zur Entzündungsreaktion um das Implantat mit einer sich bildenden Bindegewebsschicht, welche die Osseointegration verhindert. Titan dagegen ruft keine nachweisbare Immunreaktion hervor und ist somit ideal für die Osseointegration. Auch Chrom-Kobalt-Molybdän-Legierungen lösen kaum eine Reaktion des Immunsystems aus. Die Osseointegration findet in drei Schritten statt:
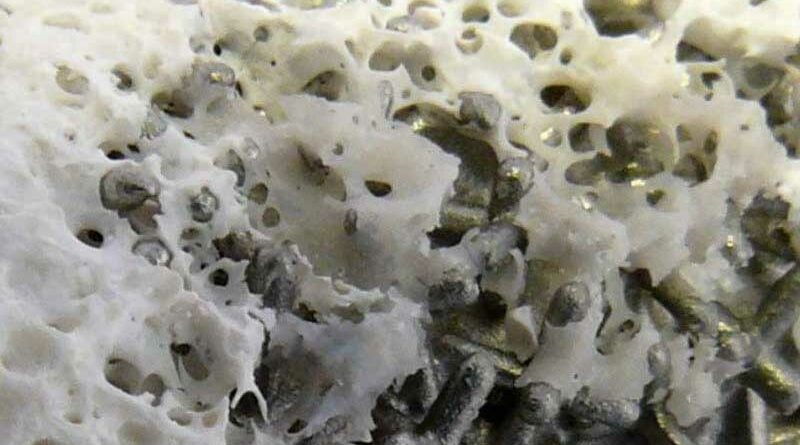
- Im ersten Schritt, der Osteokonduktion, migrieren Osteoblasten (knochenbildende Zellen) durch das Gewebe sowie das periimplantäre Hämatom und suchen Kontakt zur Implantatoberfläche, um dort ortsständig zu werden. Dabei stellen bereits größere Blutkoagel oder immunologische Reaktionen (Fremdkörperreaktion/Infektion) ein Hindernis dar. Eine komplexe Mikrostruktur, die eine günstige Porengröße aufweist, begünstigt diesen Vorgang durch optimale Oberflächenvergrößerung. (Abb. 6a u. b).
- In der zweiten Phase (De-Novo-Knochenbildung) bildet sich zunächst eine spezielle Bindegewebsmatrix, die letztendlich im Rahmen der Calciumphosphateinlagerungen verknöchert. Dabei wird die Grenzschicht zwischen Implantat und kollagener Calciumphosphat-Matrix als “kontaktosteogenetischer Bereich” bezeichnet.
- Im dritten Schritt bildet sich zwischen dieser Schicht und dem originären Knochen weiterer fester Knochen, und das Implantat ist osseointegriert (Distanzosteogenese) 6.
Dieser Vorgang darf nicht durch Mikrobewegungen (im Mikrometerbereich) gestört werden, da es sonst zu einer fehlerhaften Anheftung der neuen Knochenmatrix am Implantat kommt und eine ungewollte Bindegewebsschicht entsteht 7. Die Primärstabilität des Implantates ist daher ein entscheidender Faktor für das Gelingen der Osseointegration. Aus diesem Grund führen die Verfasser weiterhin ein zweizeitiges Vorgehen durch, um Mikrobewegungen zwischen Implantat und Knochen in den ersten Wochen zu vermeiden.
Der Stomakanal
Als eigentlicher Kritikpunkt der Versorgungstechnik mittels TOPS wird von vielen Fachkollegen das Vorhandensein des Stomakanals angesehen. In der klassischen operativen Orthopädie und Unfallchirurgie ist es undenkbar, dass Implantate, die permanent im Körper verbleiben, nicht durch Weichteile gedeckt sind. Es wird in diesem Zusammenhang grundsätzlich von einer Infektion des Implantatlagers ausgegangen.
Die Arbeiten von Aschoff und Brånemark in den vergangenen fast 30 Jahren haben gezeigt, dass eine obligate Besiedlung des Stomakanals mit Bakterien naturgemäß vorhanden ist, dass aber tiefergehende Infektionen mit einer resultierenden Osteitis oder Implantatinfektion zwar auftreten, aber im niedrigen Prozentbereich ein vertretbares Risiko darstellen 8 9. In den Anfängen der Lübecker Zeit bestanden in der Tat relevante Probleme mit Stomakanalinfektionen. Die Veränderung des Implantatdesigns durch Entfernung des bucket attachments(zusätzliche, ventral dem Femur anliegende Inplantatstützstruktur), Änderung der distalen Implantatoberfläche auf eine Titanium-Oxynitridbeschichtung und eine veränderte Operationstechnik bei der Stomakanalanlage senkten die Rate der tiefen Infektionen auf ein Niveau vergleichbar mit unfallchirurgisch-orthopädischen Eingriffen. Im Gegensatz zur ursprünglichen Idee eines langen Weichteilmantels mit guter Muskeldeckung des Endmoduls wird aktuell ein Stomakanal mit einer maximalen Länge von 20 mm favorisiert. Dies gewährleistet nach Abschluss der zirkulären Narbenbildung eine gute Pflege des Stomakanals bis zur Knochengrenze und verhindert die Bildung von Flüssigkeitsverhalten im Stomakanalbereich. Dieses Konzept des Unterschiedes des feuchten und trockenen Stomakanals wird auch von anderen Arbeitsgruppen vertreten 10.
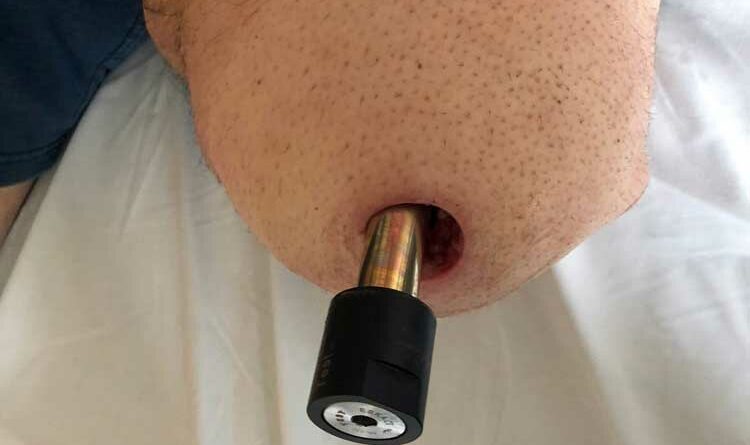
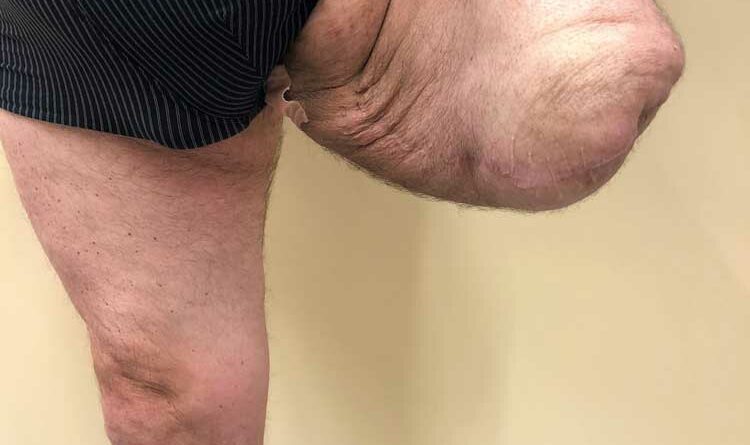
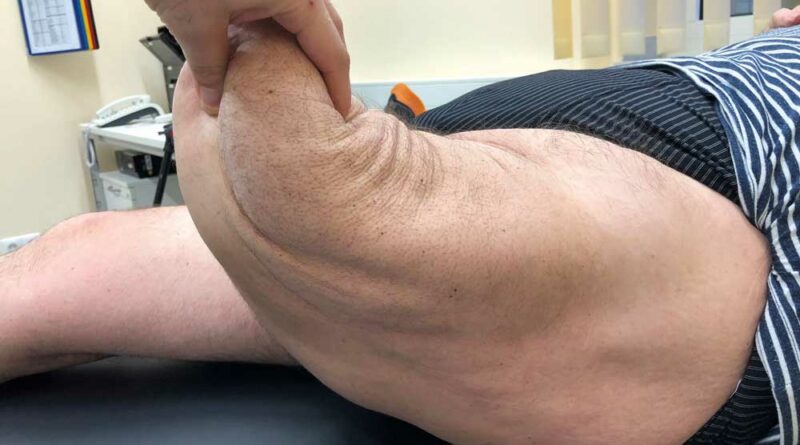
Der operativ frisch angelegte Stomakanal wird zunächst unter sterilen Kautelen verbunden. Täglich wird eine antiseptische Wundbehandlung durchgeführt. Im Laufe der folgenden Wochen kommt es zur deutlichen Abnahme des Wundsekrets und einer zirkulären Narbenbildung um das einliegende Implantat. Der Prothesenanwender soll den Kanal mindestens einmal täglich mit herkömmlichen hygienischen Mitteln reinigen. Der Kanal darf ausgeduscht werden. Zudem soll er manuell mobilisiert werden, um ein Verkleben des Unterhautund Hautgewebes mit dem Implantat zu verhindern. Nach mehreren Monaten bildet sich aus einem großvolumigen Stomakanal ein gut mobilisierbar narbiger Ring. Je geringer die Weichteilbedeckung bis zur Knochengrenze ist, desto weniger Wundsekret wird über den Kanal abgesondert. Einige Anwender berichten auch von trockenen Stomakanälen (Abb. 7a u. b).
Transkutane osseointegrierte Prothesensysteme am Klinikum Bergmannstrost
Aus den vorhandenen TOPS wurde am Klinikum Bergmannstrost Halle das Endo-Exo-Prothesensystem der Firma ESKA Orthopaedic GmbH (Abb. 8) ausgewählt. Der Endostiel von ESKA zeichnet sich durch eine besondere Oberflächenstruktur aus. In den 90er Jahren entwickelt Hans Grundei eine offenporige metallene Oberflächenstruktur, um einen spongiösen Knochen nachzuempfinden. Als “Metallspongiosa II” wurde diese Technologie sehr erfolgreich bei Endoprothesen benutzt. Die optimale Porengröße, entsprechend den biologischen Anforderungen entwickelt, ermöglicht ein sehr gutes Einwachsen des Knochens ins Implantat. Zudem reichen die Erfahrungen mit diesem Implantatsystem bereits 20 Jahre zurück. Für die erste Versorgung am Klinikum Bergmannstrost konnte Dr. Aschoff als Co-Operateur gewonnen werden. Somit konnte das Team direkt von seinen Erfahrungen profitieren. Die Klinik für Unfallund Wiederherstellungschirurgie am BG Klinikum Bergmannstrost hat im Jahr 2017 in Anlehnung an das Vorgehen von Dr. Aschoff ein eigenes Protokoll für das TOPS etabliert und führt dieses seit Anfang 2018 durch (Tab. 1).
Anwender, die sich für das TOPS interessieren, stellen sich in der interdisziplinären Sprechstunde für Amputationsmedizin vor. Bei einem ersten Treffen wird in einem Gespräch die Erwartungshaltung des Anwenders ermittelt, das Verfahren der TOPS erläutert und geprüft, ob eine Versorgung überhaupt in Frage kommt. An einem zweiten Termin wird zusammen mit dem später versorgenden Orthopädietechniker der geplante Versorgungsablauf und die zwingend nötige Rehabilitation besprochen. Mittels einer ambulanten oder stationären Diagnostik der Nebenerkrankungen wird das Risiko eines Versagens der Osseointegration bewertet. Dabei wird besonders die Durchblutung der Extremität, das Vorhandensein eines Diabetes und die knöcherne Qualität beurteilt. Höhergradige Durchblutungsstörungen (ab AVK IIb nach Fontaine) oder ein Diabetes mellitus gestatten aufgrund des Infektionsrisikos keine Versorgung mittels TOPS (Tab. 2).
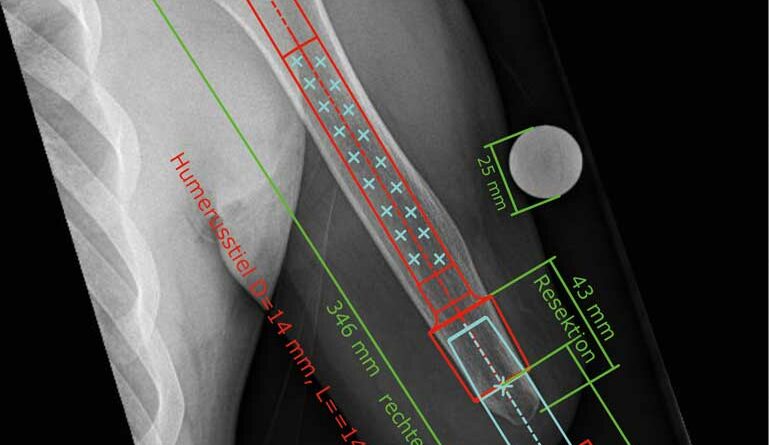
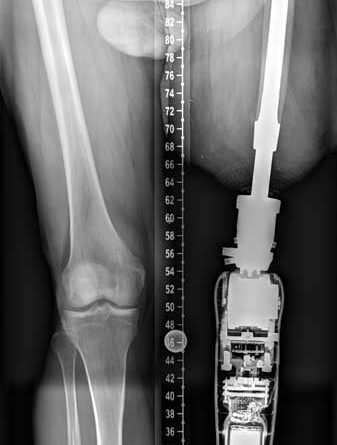
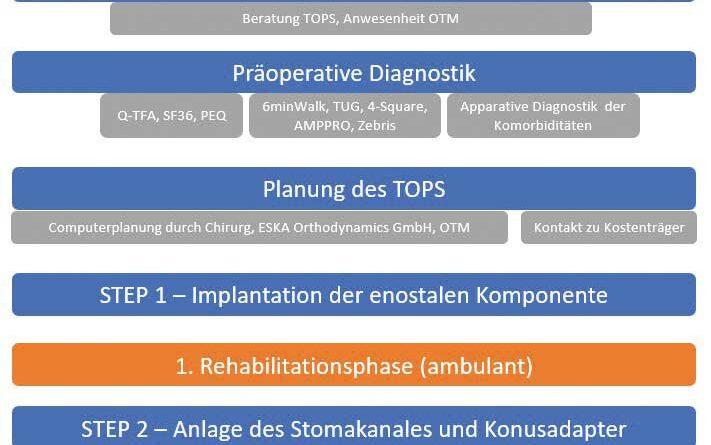
Um Funktionsvergleiche und Prothesennutzung vor und nach der Versorgung zu ermöglichen, werden zudem Daten per Fragebögen erhoben und klinische Testverfahren durchgeführt. Vor der ersten Operation wird zusammen mit dem Orthopädietechniker, dem Operateur und der ESKA Orthopaedic GmbH die Planung für die TOPS an referenzierten Röntgenaufnahmen vorgenommen (Abb. 9). Dabei fließen die Aufbauhöhe der geplanten Passteile, die Implantatgröße und die ossäre Struktur des Implantatlagers in die Planung ein. Anschließend wird bereits Kontakt zum Kostenträger gesucht, um das Vorgehen zu erläutern und Probleme im Versorgungsablauf zu vermeiden. Der weitere Verlauf:
- Im ersten Schritt (“Step 1″) erfolgt die Implantation des Endomoduls. Wichtig dabei ist, dass die Weichteile hinreichend gekürzt werden, um die spätere Stomakanalbildung mit einer Gesamtlänge von max. 20 mm zu erreichen. Daher unterscheidet sich das Vorgehen erheblich von klassischen stumpfkorrigierendenden Operationen. Denn die sonst angestrebte Muskeldeckung des knöchernen Stumpfendes muss zugunsten eines kurzen Stomakanals vermieden werden. Trotzdem muss auf eine balancierte Muskelanheftung am Knochen geachtet werden, um eine adäquate Prothesenführung zu gewährleisten. Der Hautverschluss berücksichtigt bereits die spätere Stomakanalposition (Abb. 10 a–c). Der Patient wird etwa 7 Tage nach der Operation entlassen. Es schließt sich eine ambulante Physiotherapie zur allgemeinen Konstitutionsverbesserung und Kontrakturbehandlung der proximalen Gelenke an. Weitere klassische physiotherapeutische Nachbehandlungen analog zu einem Amputationsstumpf werden aufgrund der Methodik der TOPS nicht durchgeführt.
- 6 Wochen nach dem ersten Operationsschritt erfolgt im zweiten Schritt (“Step 2″) die Anlage des Stomakanals und die Implantation des Doppelkonusadapters. Dieser wird mit einem temporären Verschlussstück gesichert.
- Bei unauffälligem Verlauf erfolgt durch den Orthopädietechniker in “Step 3″ eine Woche nach Operation der Austausch des temporären Verschlussstückes gegen den Brückenzylinder. Der statische Aufbau der Exoprothese wird nach Aufbauempfehlung der Firma ESKA durchgeführt.
Über einen Zeitraum von 6 bis 12 Wochen wird sukzessive die Teilbelastung der TOPS bis zur Vollbelastung gesteigert. Trotz theoretischer axialer Vollbelastbarkeit des Endomodules bestehen anfänglich individuelle Unterschiede bezüglich der Toleranz der Lastaufnahme: Der erste Kontakt zum Boden über die Prothese wird meist als kurzzeitig schmerzhaft empfunden. Sobald der Patient mit Unterarmgehstützen voll mobilisiert ist, schließt sich eine stationäre Rehabilitation an. Diese ist zwingend nötig, da sich das Laufverhalten grundsätzlich von einer schaftgeführten Prothese unterscheidet. Insbesondere die Osseoperzeption (der unmittelbar vermittelte Bodenkontakt durch das TOPS) beeinflusst den Bewegungsablauf erheblich. Zudem muss der Anwender geschult werden, übermäßige Torsion über die Prothese zu vermeiden.
Mittelfristige Verlaufskontrollen richten sich nach den Bedürfnissen des Anwenders. Obligate Vorstellungen finden 6 und 12 Monate nach “Step 3″ und anschließend jährlich statt. Dabei werden erneut die klinischen Testverfahren und Fragebögen erhoben.
Statischer Prothesenaufbau und Besonderheit des Brückenzylinders
Die Grundprinzipien des Prothesenaufbaus unterscheiden sich beim TOPS nicht von schaftgeführten Prothesen; die Passteile werden entsprechend den Herstellerinformationen aufgebaut. Die Besonderheit stellt die unmittelbare knöcherne Verbindung der Prothese dar. Aus diesem Grund sollten dem Orthopädietechniker beidseitige Ganzbeinaufnahmen zur Verfügung stehen. Hierdurch kann eine exakte Position der Längs- und Drehachsen der Knie- und Fußpassteile erreicht werden. Für die unmittelbare Verbindung der Exoprothese mit dem Brückenzylinder ist aus statischen Gründen ein Rückverlagerungsadapter notwendig. Die Größe des Modules ergibt sich aus den Anforderungen der Passteile sowie einer ggf. bestehenden Hüftbeugekontraktur. Insbesondere Letztere ändert sich innerhalb der ersten Wochen aber deutlich, sodass Anpassungen der Rückverlagerungsadapter notwendig sein können. Für den Fall ungewollter sehr hohe
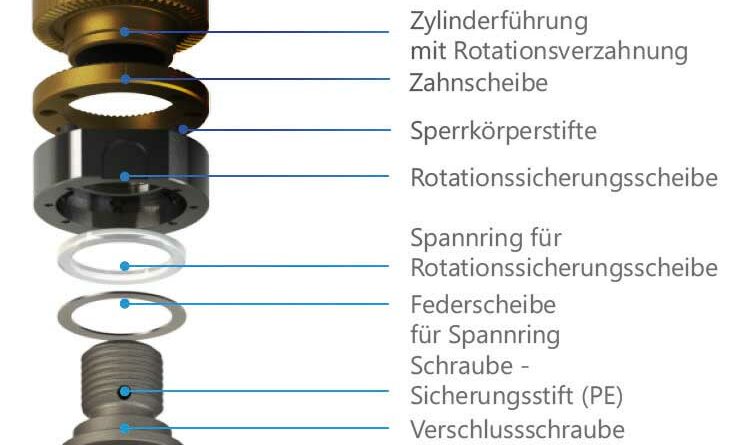
Torsionsmomente von der Prothese auf den Knochen, welche zur Periimplantierenbrüchen führen würden, befindet sich innerhalb des Brückenzylinder eine Sollbruchstelle (Abb. 11). Diese wird durch Torsionssperrkörperelemente (50–130 Nm) eingestellt und muss an die aktuelle Belastung und Gewichtssituation angepasst sein. Somit kommt es zur gewollten Aufnahme der Torsionsspannung in den Brückenzylinder mit kontrolliertem Brechen der Sperrstifte und ein Knochenbruch kann vermieden werden.
Da ein Brückenzylinder und ein Rückverlagerungsadapter bei diesem Endo-Exo-Prothesensystem vorkommen, ist im Rahmen der ersten Versorgung, die ein Orthopädietechniker durchführt, eine Schulung durch die Anwesenheit eines Mitarbeiters von ESKA vorgesehen. Zudem soll ein spezieller Servicekoffer mit Werkzeugen und Testadaptern verwendet werden.
Eine Besonderheit stellen Anwender mit Unterschenkelamputation dar. Ganganalytische Untersuchungen durch Blumentritt haben belegt, dass es beim herkömmlichen statischen Aufbau der Prothese unter Zuhilfenahme von Kraftmessplatten, Kompromissdrehachsen und Aufbaulinien zu einer übermäßigen Beanspruchung des Kniegelenkes kommt. Trotz eines korrekten Aufbaus musste die Position des Prothesenfußes nach lateral und dorsal angepasst werden, um einem ungünstigen Drehmoment im Kniegelenk entgegenzuwirken. Dies wird von den Patienten anfänglich nicht verspürt; nach Einsetzen von Beschwerden kann aber möglicherweise eine Arthroseentwicklung bereits begünstigt worden sein. Aus diesem Grund empfehlen die Autoren grundsätzlich, bei Patienten mit Unterschenkelamputation nach erfolgter Anpassung eine apparative Ganganalyse durchzuführen, um die entstehenden Drehmomente und Belastung der Gelenke bewerten zu können.
Versorgungsbeispiele transfemoral und transhumeral
Versorgungsbeispiel transfemoral: Patient A, 59 Jahre
Amputationsgrund: Gefäßembolie (2016) ohne begleitende arterielle Verschlusskrankheit
Passteile: rückverlagernder Anschlussadapter, Rheo-3-Kniegelenk, Proflex-Fuß
Die Versorgung gestaltete sich aufgrund einer schwierigen Weichteilsituation am Stumpfende, im Beckenbereich sowie am proximalen medialen Oberschenkel kompliziert. Trotz mehrfacher Anpassungsversuche einer schaftgeführten Exoprothese konnte für den Patienten keine zufriedenstellende Mobilisation erreicht werden. Zudem bestanden Probleme beim Prothesenhalt mit Sturzgefährdung. Nach Durchführung der Voruntersuchungen wurde protokollgemäß am 5 März 2018 “Step 1″ und am 18. April “Step 2″ durchgeführt (Abb. 12a– c).
“Step 3″ besteht nicht nur im Erstaufbau der Prothese, sondern ist ein mehrere Wochen umfassender Versorgungsschritt. Der Patient sollte die ersten 4 Wochen zumindest einmal wöchentlich durch den Orthopädietechniker begutachtet werden. Wichtige Aspekte der jeweiligen Vorstellung:
- Anpassen des Rückverlagerungsadapters (Vermessung der Femurflexion, Abstandsmessung zwischen Aufbaulinie und Brückenzylinder, Prüfung der zentralen Fixierungsschraube)
- Kontrolle mittels L.A.S.A.R. Posture
- Anpassung des Brückenzylinders mit den Torsionsperrelementen an das Belastungsniveau
- Protheseneinweisung (Pflege der Module, Funktionsprinzip der Einhandprothesenkonnektion)
- Wundkontrollen (ggf. Rücksprache mit Mediziner)
- erste Gehversuche mit Auslösung des Kniegelenkes (mit Gehhilfen)
In den folgenden sechs Wochen steigerte der Patient sukzessive die Belastung mit der Prothese, sodass sich die stationäre Rehabilitation im Juni und Juli 2018 anschließen konnte. Aktuell ist der Patient vollständig mobilisiert und trägt die Prothese den ganzen Tag. Stomaproblematiken sind bisher nicht aufgetreten, und die Röntgenverlaufskontrollen weisen eine unauffällige Implantatlage auf.
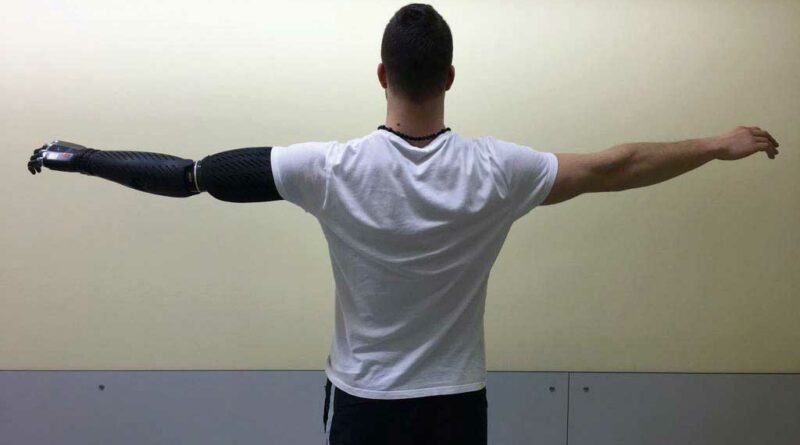
Versorgungsbeispiel transhumeral: Patient B, 29 Jahre
Amputationsgrund: Polytrauma OAAmputation links, US-Amputation rechts
Passteile: Bebionic-Hand, Rotationseinheit, ErgoArm Hybrid, Zweikanalsteuerung mit MyoBock-Elektroden, Silikonhaltebandage zur kontralateralen Seite (nur vor TOPS)
Die Rehabilitation einer traumatischen Oberarmamputation mit konventionellem Schaftsystem gestaltet sich bei kurzen Stümpfen oft schwierig. Die Probleme bestehen in einer nicht zufriedenstellenden Schulterbewegung der amputierten Seite und einer durch die Schulterbandage eingeschränkten kontralateralen Seite.
Patient B wurde im August 2015 mit einem individuellen HTV-Silikonliner mit Velcro-Verschlusssystem und einer HTV-Silikonhaltebandage zur kontralateralen Seite versorgt. Die Versorgung wird myoelektrisch betrieben; somit war die Positionssicherung der Prothese entscheidend für die Ansteuerung. Durch die Kürze des Stumpfes war das Ergebnis aber nur wenig zufriedenstellend. Die Montage der Prothese wurde nach den herkömmlichen Aufbaurichtlinien und unter Berücksichtigung des Eigengewichts der Passteilkomponenten vorgenommen. Das Brückenmodul ist distal mit einer Pyramidenaufnahme versehen, an dem ein Custommade-Adapter befestigt wurde, um die Verbindung zum ErgoArm Hybrid herzustellen. Nach vierwöchigem Tragen wurde festgestellt, dass sich die muskuläre Situation im Schultergürtel des Patienten deutlich verändert hat: Nach deutlicher Atrophie der amputierten Seite findet sich nun eine verbesserte muskuläre Situation. Dies hatte Konsequenzen für den statischen Prothesenaufbau. Die Ellenbogenachse hatte sich durch erhöhte Abduktion im Schulterbereich verändert, wiederum mit Einfluss auf den Custom-made-Adapter und die Passteile. Somit war es notwendig, den Aufbau anzupassen.
Aufbau und Sitz der Prothese wurden in regelmäßigen Abständen überprüft, und nach etwa 3 Monaten konnten keine signifikanten Veränderungen mehr feststellt werden. Somit war es möglich, die kosmetische Verkleidung herzustellen, die mittels Scan und Spiegelung der kontralateralen Seite per 3D-Druck in Polyamid gefertigt wurde. Es wurde jeweils eine Verkleidung für den Unterarm und für den Oberarm gedruckt. Diese sind atmungsaktiv und nachstellbar im Sinne einer statischen Veränderung und einer Volumenänderung. Die Verkleidung für den Oberarm ist mit einem Magnetverschluss versehen und daher zur schnellen und eigenständigen An- und Abnahme geeignet. Heute ist der Patient voll in seinen Alltag integriert und beschreibt eine deutlich bessere Positionierung der Prothese sowie eine sehr leichte Handhabung. Durch die knochengeführten Bewegungen erlangte er eine bessere Krafteinleitung sowie eine osteoperzeptive Fähigkeit. Daher wird eine physiologische Belastungsfähigkeit erreicht (Abb. 13a–c). Die knochengeführten Prothesensysteme sind eine Möglichkeit Patienten, welche nicht oder nur ungenügend mit einer schaftgeführten Prothese rehabilitierbar sind, exoprotetisch zu versorgen. Damit ist eine deutliche Teilhabeverbesserung zu erreichen. Insbesondere für Patienten mit transhumeraler Amputation ist die knochengeführte Prothesenverankerung eine Technologie, mit welcher das Schultergelenk im Bewegungsumfang nicht beeinträchtigt wird und eine sichtbare Verbesserung der Körpersymetrie erreich werden kann.
Für die Autoren:
Patrick Schröter
Facharzt für Allgemeinchirurgie
Zertifikat Technische Orthopädie
Notfallmedizin
Klinik für Unfall- und
Wiederherstellungschirurgie
BG Klinikum Bergmannstrost Halle
Merseburger Straße 165
06112 Halle
patrick.schroeter@bergmannstrost.de
Hinweis:
Widmung:
Lieber Herr PD Dr. Lutz Brückner,
das Team am Bergmannstrost Halle möchte Ihnen an dieser Stelle herzlichste Grüße zu Ihrem 75. Geburtstag aus Halle senden. Wir danken Ihnen für die vielen schönen und lehrreichen Jahre der gemeinsamen Arbeit. Sie haben mit Ihrem unerschöpflichen Wissen auf dem Gebiet der Amputationsmedizin und Technischen Orthopädie über fast zwei Jahrzehnte die Arbeit an unserem Haus maßgeblich geprägt. Insbesondere Ihre Herzlichkeit und Offenheit im Umgang mit unseren Patienten haben wir bewundert und vermissen diese. Trotz Ihres wohlverdienten Ruhestandes stehen Sie uns weiterhin mit Rat und Tat zur Seite. Wir hoffen weiterhin auf eine Fortführung der regen Zusammenarbeit über viele Jahre. Im Namen des gesamten Teams der Technischen Orthopädie des Bergmannstrost darf ich Ihnen alles erdenklich Gute und vor allem viel Gesundheit wünschen.
Ihr Patrick Schröter
Schröter P, Müller CH, Oelßner B. Transkutane osseointegrierte Prothesensysteme (TOPS). Orthopädie Technik, 2020; 71(8): 30
- Die orthopädietechnische Versorgung mit einer dynamischen Fingerstreckorthese als eigenständige Therapie bei der Dupuytren’schen Kontraktur — 26. März 2026
- Vergleichende Prüfung konventioneller und additiv gefertigter Prothesenschäfte in Anlehnung an DIN EN ISO 10328:2016 — 10. März 2026
- Easypreg – ein Faserverbundwerkstoff zum Tiefziehen — 9. März 2026
- Murphy EF. History and philosophy of attachment of prostheses to the musculo-skeletal system and of passage through the skin with inert materials. Journal of Biomedical Materials Research, 1973; 7 (3): 275–295
- Rudy, R. J., Levi Jr, P. A., Bonacci, F. J., Weisgold, A. S., & Engler-Hamm, D. (2008). Intraosseous anchorage of dental prostheses: an early 20th century contribution. Compendium, 29(4), 220.
- Brånemark P‑I et al. Intra-osseous anchorage of dental prostheses: I. Experimental studies. Scandinavian Journal of Plastic and Reconstructive Surgery, 1969; 3 (2): 81–100
- Al Muderis M et al. Single-stage osseointegrated reconstruction and rehabilitation of lower limb amputees: the Osseointegration Group of Australia Accelerated Protocol‑2 (OGAAP‑2) for a prospective cohort study. BMJ open, 2017; 7 (3): e013508
- McGough RL et al. The Compress® transcutaneous implant for rehabilitation following limb amputation. Der Unfallchirurg, 2017; 120 (4): 300–305
- Davis JE. Understanding peri-implant endosseous healing. Journal of Dental Education, 2003; 67 (8): 932–949
- Gradinger R, Gollwitzer H. Ossäre Integration. Heidelberg: Springer, 2006
- Juhnke D‑L et al. Fifteen years of experience with Integral-Leg-Prosthesis: Cohort study of artificial limb attachment system. Journal of Rehabilitation Research & Development, 2015; 52 (4): 407–420
- Hagberg K, Brånemark R. One hundred patients treated with osseointegrated transfemoral amputation prostheses—rehabilitation perspective. Journal of Rehabilitation Research & Development, 2009; 46 (3): 331–334
- Frolke JPM, Leijendekkers RA, Meent H. Osseointegrated prosthesis for patients with an amputation: Multidisciplinary team approach in the Netherlands. Der Unfallchirurg, 2017,120 (4), , 293–299