Einleitung
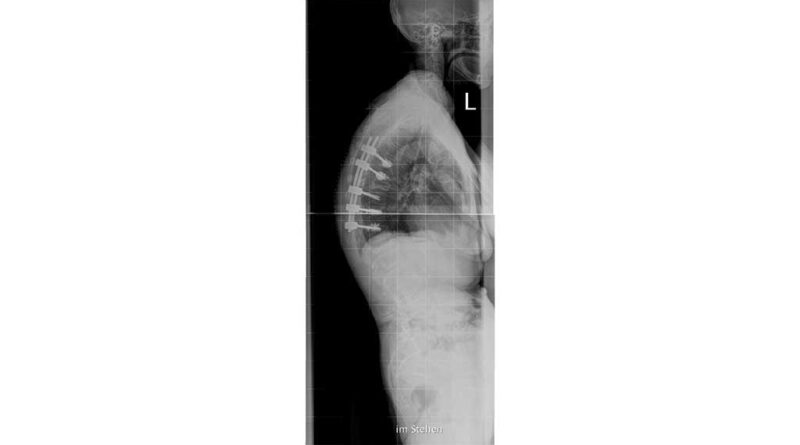
Osteoporose stellt in unserer alternden Gesellschaft eine stetig wachsende Herausforderung dar. Die Verminderung des Mineralgehaltes der Knochen führt zur Änderung der Spongiosa-Architektur und zur Reduktion der Knochenmasse, was Mikrofrakturen, Spontanfrakturen, Frakturen durch Bagatelltraumata sowie nachfolgende Fehlstellungen nach sich ziehen kann (Abb. 1).
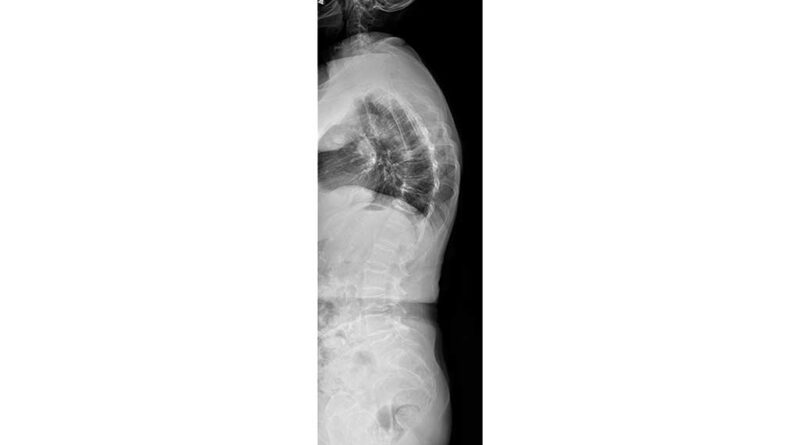
Eine häufig auftretende Begleiterscheinung der Osteoporose ist die Sarkopenie. Geprägt von einem degenerativen, altersbedingten Verlust von Muskelmasse, ‑kraft und ‑funktion hat auch diese Erkrankung weitreichende Folgen, die unter anderem mit einer Erhöhung des Sturzrisikos und dem Auftreten funktioneller bzw. motorischer Einschränkungen einhergehen. Von besonderer Bedeutung ist jedoch das Zusammenspiel beider Erkrankungen, vornehmlich im Hinblick auf die Wechselwirkungen von Knochen und Muskel. Einerseits kommt es durch die Sarkopenie durch mangelnde und falsche Beanspruchung des muskuloskelettalen Bewegungssystems zu arthromuskulären Defiziten sowie zu Dysbalancen, die wiederum über Verspannungen, Myogelosen und Blockierungen zu Schmerzen führen können. Andererseits ist durch die Sarkopenie das Sturzrisiko der Patienten deutlich erhöht, was das Auftreten von Frakturen bei ohnehin geschwächtem Knochen begünstigt. Die Frakturen machen häufig operative Stabilisierungen nötig (Abb. 2).
Die hohe Anzahl an Betroffenen sowie die daraus resultierenden hohen Behandlungskosten 1 2 erfordern eine strukturierte Versorgung. Neben der eigentlichen Behandlung der Osteoporose ist insbesondere eine adäquate Schmerztherapie notwendig. Diese findet primär im Rahmen unimodaler Therapiekonzepte statt und muss bei ungenügender Wirkung durch multimodale Behandlungskonzepte ergänzt werden. Unter einem multimodalen Behandlungskonzept versteht man ein Verfahren, bei dem gleichzeitig unterschiedliche medizinische Fachdisziplinen gemeinsam an der Therapie beteiligt sind und ihr Vorgehen miteinander koordinieren.
Schmerzentstehung bei Osteoporose
Die Genese der Schmerzentstehung bei Osteoporose ist multifaktoriell. Der Osteoporose liegt eine negative Skelettbilanz zugrunde; die sonst ausgewogene Balance zwischen Osteoblasten- und Osteoklastenaktivität ist dabei gestört. So führt eine verstärkte Osteoklastenaktivität nicht nur zum Absinken der Knochendichte, sondern auch zum Abfall des pH-Wertes, was eine Sensitivierung der Nozizeptoren (Schmerzrezeptoren) bedingt. Weiterhin wird die zentrale Schmerzverarbeitung sensibilisiert, und der Einfluss emotionaler Faktoren auf das Schmerzempfinden nimmt zu 3. Andere Autoren gehen davon aus, dass der Hauptanteil der Schmerzsymptomatik bei Patienten mit Osteoporose eher durch Folgeerscheinungen der Osteoporose hervorgerufen werde 4. Sie plädieren dafür, dass beim gleichzeitigen Vorliegen von Kreuzschmerzen und Osteoporose an begleitende Pathologien der Wirbelsäule gedacht werden müsse. Dabei stehen einerseits osteoporoseassoziierte Pathologien wie Frakturen, Hyperkyphosen und deren Kompensationsmechanismen, andererseits degenerative Erkrankungen der Wirbelsäule (Osteochondrosen, Facettengelenksdegenerationen) im Fokus. Insbesondere beim plötzlichen Auftreten starker Rückenschmerzen muss an eine Spontanfraktur eines Wirbelkörpers (Sinterungsfraktur) gedacht werden, wenn eine Osteoporose oder bestimmte Risikofaktoren (postmenopausale Frauen, Steroidmedikation, hohes Alter) vorliegen. Solche Sinterungsfrakturen können als Spontanfrakturen ohne vorausgegangenen Sturz auftreten.
Durch multisegmentale Frakturen kann es zu Deformitäten der Wirbelsäule und damit einhergehend zu einer zunehmenden Gestaltänderung mit Hyperkyphosierung kommen. Die dadurch entstehenden Überlastungen und Dysbalancen der rumpfstabilisierenden und aufrichtenden Muskulatur führen bei ohnehin oft gleichzeitig vorliegender Sarkopenie ebenfalls zu Schmerzen. Daraus resultiert eine multifaktorielle Schmerzgenese mit der Gefahr einer Chronifizierung der Schmerzen. Die Häufigkeit einer Chronifizierung liegt hierbei im zweistelligen Prozentbereich. Diese multifaktoriell ausgelösten Schmerzen sind einer rein unimodalen Schmerztherapie nicht ausreichend zugänglich und erfordern somit einen multimodalen Therapieansatz.
Daher werden in der Therapie der Osteoporose an sich und des damit verbundenen chronischen Osteoporoseschmerzes kombinierte Therapien aus pharmakologischen, physiotherapeutischen, psychotherapeutischen und in manchen Fällen operativen Methoden angewendet. Auch eine Orthesenversorgung mit muskelaktivierenden und aufrichtenden Orthesen kann diskutiert werden. Die Studienlage hierzu ist jedoch nicht eindeutig, da die beiden vielversprechenden deutschen Studien dazu zum einen firmenfinanziert sind, zum anderen in der statistischen Ausarbeitung Mängel aufweisen 5 6. Trotz dieser Einschränkungen scheint diesen Studien zufolge durch die Anwendung aktivierender spinaler Orthesen sowohl eine Schmerzreduktion als auch eine Muskelkräftigung und eine Haltungskorrektur erreicht zu werden. Zwei systematische Reviews zur Wirksamkeit spinaler Orthesen zeigen jedoch nur insignifikante Ergebnisse 7 8.
Zudem kann bereits die spezifische medikamentöse Therapie der Osteoporose durch die Vermeidung weiterer Frakturen die Schmerzen der Patienten reduzieren. Die alleinige Therapie der Grunderkrankung führt jedoch kurzfristig nicht zu einer ausreichenden Kontrolle der Schmerzsymptomatik.
Zur Abschätzung eines Chronifizierungsrisikos der Schmerzen müssen sogenannte „yellow flags“ eruiert werden. Dabei handelt es sich um psychosoziale Risikofaktoren wie Depression, Angst-Vermeidungsverhalten oder Neigung zur Somatisierung. Liegen solche „yellow flags“ vor, muss von einem deutlich erhöhten Risiko einer Chronifizierung der Schmerzen ausgegangen werden 9. Als etabliertes Therapiekonzept hat sich für die Therapie des osteoporoseassoziierten Schmerzes daher die multimodale Schmerztherapie bewährt.
Die multimodale Schmerztherapie
Grundlagen der multimodalen Schmerztherapie
Der multimodalen Schmerztherapie liegt ein biopsychosoziales Schmerzmodell zugrunde. Dieses bildet heute die Basis für das Verständnis des chronischen Schmerzes und ist Ausgangspunkt entsprechender therapeutischer Interventionen. Es wurde 1977 von dem amerikanischen Internisten und Psychiater George L. Engel entwickelt 10 und erfasst Schmerzen nicht nur auf somatischer Ebene, sondern diese werden als Störung biologischer, sozialer und psychischer Faktoren verstanden, die im Umkehrschluss in der Behandlung dieser Erkrankung alle gleichberechtigt adressiert werden müssen. Somit nehmen biografische Erlebnisse und soziale Faktoren ebenso Einfluss auf das Schmerzempfinden wie psychische und somatische Erkrankungen.
Die multimodale Schmerztherapie hat in der Behandlung chronischer Rückenschmerzen einen hohen Stellenwert. Die Effektivität dieser Therapie hat sich durch die Ergebnisse diverser Studien und Metaanalysen bestätigt und ist in Versorgungsleitlinien implementiert 11.
Diagnostik
Vor dem Beginn einer multimodalen Schmerztherapie steht ein interdisziplinäres Assessment. Dabei werden die Schmerzsymptomatik, der Einfluss der Schmerzen auf die Alltagsfunktion und auf die soziale Teilhabe, aber auch vorhandene Ressourcen evaluiert. Im Assessment müssen die den Schmerzen zugrundeliegenden Ursachen ermittelt werden, die einen dringenden – ggf. auch interventionellen – Behandlungsbedarf nach sich ziehen (sogenannte „red flags“). Zu diesen „red flags“ zählen u. a.:
- neurologische Ausfälle,
- instabile Frakturen,
- deutliche Schmerzverstärkung oder
- Hinweise auf zugrundeliegende Tumorerkrankungen oder Infektionen.
Zudem müssen im Assessment Ausschlusskriterien wie fehlende Änderungsmotivation oder fehlende körperliche Leistungsfähigkeit eruiert werden 12. Die multimodale Schmerztherapie eignet sich nicht nur für Patienten mit chronischen Rückenschmerzen, sondern auch für Patienten mit hohem Chronifizierungsrisiko oder bei Versagen der (ambulanten) unimodalen Therapie. Relative Kontraindikationen umfassen laufende Rentenverfahren und relative Operationsindikationen.
Zielsetzung
Als Ziel der multimodalen Therapie gilt im Wesentlichen die Schmerzreduktion sowie die Wiederherstellung bzw. Verbesserung der objektiven und subjektiven körperlichen sowie psychischen Leistungsfähigkeit. Auch die Steigerung der Kontrollfähigkeit und des Kompetenzgefühls der Patienten sowie die Stärkung vorhandener Ressourcen spielen für den langfristigen Therapieerfolg eine zentrale Rolle. Zudem werden bei berufstätigen Patienten arbeitsplatzbezogene Risikofaktoren erfragt und als „blue and black flags“ klassifiziert. Bei „blue flags“ handelt es sich um subjektiv empfundene Belastungen am Arbeitsplatz; unter „black flags“ werden objektivierbare soziale Rahmenbedingungen am Arbeitsplatz zusammengefasst.
Spezifische Patientenziele werden nach dem Assessment durch das interprofessionelle Team aus Ärzten, Physiotherapeuten und Psychologen erfragt und nehmen Einfluss auf den Therapieplan 13. Aktivierende Maßnahmen stehen dabei im Vordergrund; in Ausnahmefällen kann auf passive Maßnahmen wie Massagen und Infiltration zurückgegriffen werden.
Im Folgenden wird auf die Bausteine der multimodalen Therapie genauer eingegangen. Dabei handelt es sich um folgende Elemente:
- medikamentöse Schmerztherapie,
- nichtmedikamentöse Therapien,
- supportive Maßnahmen.
Medikamentöse Schmerztherapie
Die medikamentöse Schmerztherapie wird in Anlehnung an das Stufenschema der WHO strukturiert und sollte jeweils an die individuelle subjektive Schmerzintensität angepasst sein. Für geriatrische Patienten muss dieses Stufenschema unter Beachtung von Begleiterkrankungen und Komedikationen angepasst und ergänzt werden. Dabei bietet die sogenannte FORTA-Klassifikation (FORTA = Fit fOR The Aged) mit den Kategorien A („absolutely“) und B („beneficial“) Hilfestellung 14. Für die geriatrische Patientengruppe sei insbesondere auf die höhere Wahrscheinlichkeit einer Komedikation sowie einer eingeschränkten Leber- und Nierenfunktion hingewiesen, die eine besonders sorgfältige Dosierung und Medikationswahl erfordert, um das Risiko von Akkumulationen und Interaktionen zu reduzieren. Insbesondere bei Opioiden ist auf die Erhöhung des Sturzrisikos zu achten 15. Klassische Co-Analgetika wie selektive Serotonin-Wiederaufnahmeinhibitoren oder Pregabalin werden der FORTA-Kategorie C „questionable“ zugeordnet und sollten nur unter strenger Risiko-Nutzen-Abwägung angewendet werden 16.
Nichtmedikamentöse Therapien
Nichtmedikamentöse Therapien haben einen hohen Stellenwert in der multimodalen Schmerztherapie. Dabei sind die beiden Säulen „Psychotherapie“ und „Physiotherapie“ essenziell.
Psychotherapie
Psychologische Therapieansätze entstammen der kognitiven Verhaltenstherapie und umfassen eine Edukation zum biopsychosozialen Schmerzmodell. Unter anderem wird der Patient im Erkennen und in der Reflexion schmerzverstärkender bzw. ‑vermindernder Schmerzfaktoren geschult. Das Erkennen eigener Leistungsgrenzen sowie das Erlernen von Entspannungs- und Schmerzkompensationsstrategien reduziert die Überforderung und trägt so zur Verbesserung der Lebensqualität und zur Reduktion dysfunktionaler Muster der Schmerzbewältigung bei. Ziel der Therapeuten ist es, die Motivation zum selbstverantwortlichen Krankheitsmanagement zu stärken 17. Die Schulungen umfassen unter anderem folgende Elemente:
- Achtsamkeits- und Entspannungstraining,
- Einzel- und Gruppengespräche,
- Schmerzedukation sowie
- Atem- und Körperwahrnehmung.
Physiotherapie
Abgestimmt auf das Schmerz-Assessment sowie bestehende Diagnosen wird ein individueller Behandlungsplan erstellt. Ziel ist einerseits Muskelkräftigung und Verbesserung von Körperhaltung und Koordination, andererseits die Erstellung eines Heimübungsprogramms, das der Patient nach Abschluss der multimodalen Therapie selbstständig umsetzen kann.
Eine kurzzeitig angewandte Physiotherapie zeigt in den meisten prospektiven Studien nur einen geringen und kurzzeitigen positiven Effekt 18. Wird hingegen die Therapie mit Fokus auf Muskelkräftigung, Dehnung und Nachhaltigkeit durch Eigenübungsprogramme und eine physiotherapeutisch geleitete Gruppentherapie ergänzt, kann insbesondere in Kombination mit Tai Chi, Yoga und Entspannungstechniken eine nachhaltige Schmerzreduktion erreicht werden 19. Standardisierte Übungen zur Kräftigung der Rumpf- und Rückenmuskulatur führen zu Haltungskorrektur und Schmerzreduktion 20. Somit kann der Circulus vitiosus aus Schmerz, Bewegungsvermeidung und muskulärer Atrophie unterbrochen werden.
Weitere, ergänzende Therapieformen sind denkbar, jedoch muss dabei beachtet werden, dass aktive bzw. aktivierende Therapien im Vordergrund stehen und passive Maßnahmen nur eine kurzfristige Verbesserung des Wohlbefindens bewirken. Exemplarische ergänzende Therapieformen werden im Folgenden genannt, zudem sind der analgetische Effekt von Ultraschall- und Laserbehandlungen sowie die förderlichen Effekte von Ergotherapie beim geriatrischen Patienten zu nennen 21.
Die multimodale Schmerztherapie kann individuell um die weiter unten aufgeführten Therapien ergänzt werden. Passive Maßnahmen wie Akupunktur, Infiltrationstechniken und Massagen haben aufgrund ihres möglichen nachteiligen Effektes dagegen kaum Bedeutung.
Koordinationstraining
Ein Koordinationstraining ist nicht nur für das Training der Muskulatur relevant, sondern scheint auch zu einer Verbesserung der Knochendichte zu führen sowie zur Sturzprophylaxe beizutragen 22. Es wird meist in Mischprogrammen mit weiteren ergänzenden Trainingsformen angewandt.
Supportive Maßnahmen
Elektrotherapie
Der analgetische Effekt mittel- und niederfrequenter Stromformen ist bekannt und wird auch zur Verbesserung der Durchblutung und zur Muskelkräftigung eingesetzt. Kleine Therapiegeräte im Rahmen der transkutanen elektrischen Nervenstimulation (TENS) können zur analgetischen Eigentherapie im Heimgebrauch genutzt werden. Ihre Wirkung reicht für einen relevanten Muskelaufbau zwar nicht aus, zur alleinigen Schmerztherapie können sie jedoch genutzt werden 23.
Thermotherapie
Wärme- und Kälteapplikationen haben ihren festen Stellenwert in der Schmerztherapie. Überwärmung z. B. durch Fangopackungen oder Infrarotbestrahlung regen Stoffwechsel und Durchblutung an. Die Schmerzschwelle wird durch den beschleunigten Abbau schmerzauslösender Substanzen herabgesetzt. Lokale Kälteapplikation kann schmerzhafte Reizzustände und entzündliche Veränderungen lindern. Eine Ganzkörperbehandlung in Kältekammern wirkt über eine zentrale Hemmung schmerzsenkend 24.
Krankheitsbezogene Edukation
Im Rahmen der multimodalen Schmerztherapie kann zusätzlich eine Patientenschulung hinsichtlich des Krankheitsbildes und beeinflussender Faktoren des täglichen Lebens erfolgen. Insbesondere kann dabei auf knochengesunde Ernährung und Sturzprophylaxe eingegangen werden. Die Deutsche Rentenversicherung Bund stellt dazu ein Curriculum bereit, um eine standardisierte Patientenschulung zu ermöglichen 25. Der Nutzen einer Patientenschulung ist jedoch nicht wissenschaftlich belegt und bedarf weiterer randomisierter Forschung 26.
Hausinternes Vorgehen
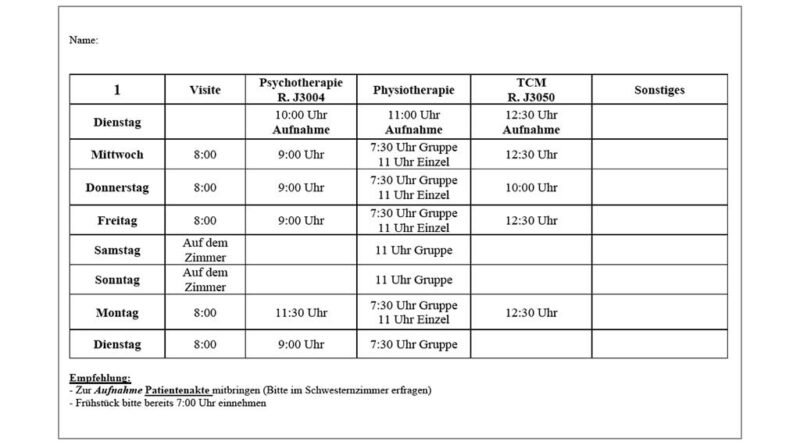
Am Klinikum der Autoren werden die oben genannten Maßnahmen im Rahmen der multimodalen Schmerztherapie in klarer zeitlicher Abfolge durchgeführt. Dabei sind die einzelnen Bausteine der multimodalen Schmerztherapie als gleichwertige und sich gegenseitig ergänzende Therapien zu betrachten. In Abbildung 3 ist exemplarisch ein Wochenplan aus der Klinik dargestellt, der den Patienten vor Beginn des stationären Aufenthaltes ausgehändigt wird. Die beschriebenen supportiven Maßnahmen sind fakultativ durchzuführen; alle anderen genannten Maßnahmen sind während der Therapie obligat.
Fazit
Osteoporose geht häufig mit Schmerzen einher, die in chronische Schmerzen übergehen können. Neben der spezifischen medikamentösen Osteoporosetherapie und physiotherapeutischen Maßnahmen ist eine adäquate Schmerztherapie daher meist unumgänglich. Die multimodale Schmerztherapie nimmt als interdisziplinäres Therapieangebot in der Behandlung osteoporoseassoziierter Schmerzen einen hohen Stellenwert ein. Da die Schmerzen auf mehrere Faktoren zurückzuführen sind, ist eine reine unimodale Therapie zur Behandlung der Schmerzen oft nicht ausreichend.
Die multimodale Schmerztherapie basiert auf dem biopsychosozialen Therapiekonzept und versucht über dieses vielseitige Konzept die Lebensqualität von Patientinnen und Patienten nachhaltig zu verbessern. Diese profitieren davon durch Schmerzedukation, das Erschließen und Aktivieren der eigenen Ressourcen sowie ein aktivierendes physiotherapeutisches Portfolio mit dem Ziel der Muskelaktivierung und der Steigerung der Mobilität. Mit dem Erlernen von Heimübungsprogrammen kann eine anhaltende Schmerzbesserung und eine Steigerung der Lebensqualität erzielt werden.
Die Autoren:
Dr. med. Elisabeth Roschke
Ärztin in Weiterbildung für
Orthopädie und Unfallchirurgie
Elisabeth.Roschke@medizin.uni-leipzig.de
Dr. med. Christian Pfeifle
Facharzt für Orthopädie und Unfallchirurgie, Spezielle Unfallchirurgie
Oberarzt im Bereich Wirbelsäulenchirurgie
Christian.Pfeifle@medizin.uni-leipzig.de
Prof. Dr. med. Christoph-Eckhard Heyde
Geschäftsführender Klinikdirektor
Leiter des Bereichs
Wirbelsäulenchirurgie
Klinik für Orthopädie, Unfallchirurgie und Plastische Chirurgie des
Universitätsklinikums Leipzig
Liebigstraße 20, Haus 4
04103 Leipzig
Christoph-Eckhard.Heyde@medizin.uni-leipzig.de
Begutachteter Beitrag/reviewed paper
Roschke E, Heyde CE, Pfeifle C. Stellenwert der multimodalen Schmerztherapie bei Osteoporose. Orthopädie Technik, 2022; 73 (3): 40–45
- Die orthopädietechnische Versorgung mit einer dynamischen Fingerstreckorthese als eigenständige Therapie bei der Dupuytren’schen Kontraktur — 26. März 2026
- Vergleichende Prüfung konventioneller und additiv gefertigter Prothesenschäfte in Anlehnung an DIN EN ISO 10328:2016 — 10. März 2026
- Easypreg – ein Faserverbundwerkstoff zum Tiefziehen — 9. März 2026
- Hadji P, Klein S, Haeussler B, Kless T, Linder R, et al. The bone evaluation study (BEST): Patient care and persistence to treatment of osteoporosis in Germany. Int J Clin Pharmacol Ther, 2012; 51: 868–872
- European Prospective Osteoporosis Study (EPOS) Group, Felsenberg D, Silman AJ, Lunt M, Armbrecht G, et al. Incidence of vertebral fracture in europe: results from the European Prospective Osteoporosis Study (EPOS). J Bone Miner Res, 2002; 17 (4): 716–724
- Catalano A, Martino G, Morabito N, Scarcella C, Gaudio A, Basile G, et al. Pain in osteoporosis: From pathophysiology to therapeutic approach. Drugs Aging, 2017; 34 (10): 755–765
- Minne HW, Pfeifer M, Begerow B, Pollähne W et al. Osteoporose. Orthop, 2002; 31 (7): 681–699
- Pfeifer M, Begerow B, Minne HW. Effects of a New Spinal Orthosis on Posture, Trunk Strength, and Quality of Life in Women with Postmenopausal Osteoporosis: A Randomized Trial. American Journal of Physical Medicine & Rehabilitation, 2004; 83: 177–186. https://doi.org/10.1097/01.PHM.0000113403.16617.93
- Pfeifer M, Kohlwey L, Begerow B, Minne HW. Effects of two newly developed spinal orthoses on trunk muscle strength, posture, and quality-of-life in women with postmenopausal osteoporosis: a randomized trial. Am J Phys Med Rehabil, 2011; 90: 805–815. https://doi.org/10.1097/PHM.0b013e31821f6df3
- Goodwin VA, Hall AJ, Rogers E, Bethel A. Orthotics and taping in the management of vertebral fractures in people with osteoporosis: a systematic review. BMJ Open, 2016; 6: e010657. https://doi.org/10.1136/bmjopen-2015–010657
- Newman M, Minns Lowe C, Barker K. Spinal Orthoses for Vertebral Osteoporosis and Osteoporotic Vertebral Fracture: A Systematic Review. Archives of Physical Medicine and Rehabilitation, 2016; 97: 1013–1025. https://doi.org/10.1016/j.apmr.2015.10.108
- Hallner D, Hasenbring M. Classification of psychosocial risk factors (yellow flags) for the development of chronic low back and leg pain using artificial neural network. Neurosci Lett, 2004; 361 (1–3):151–154
- Sabatowski R, Schäfer D, Kasper SM, Brunsch H, Radbruch L, et al. Pain Treatment: A Historical Overview. Curr Pharm Des, 2004; 10: 701–716
- Arnold B, Brinckschmidt T, Casser HR, Diezemann A, Gralow I, Irnich D et al. Multimodale Schmerztherapie für die Behandlung chronischer Schmerzsyndrome – Ein Konsensuspapier der Ad-hoc-Kommission „Multimodale Schmerztherapie“ der Deutschen Schmerzgesellschaft zu den Behandlungsinhalten. Schmerz, 2014; 28: 459–472
- Gosch M, Pils K, Venkat S, Singler K et al. Aspekte der multimodalen Schmerztherapie im Alter. Z Gerontol Geriat, 2021; 54: 823–832. https://doi.org/10.1007/s00391-021–01952‑1
- Sabatowski R, Kaiser U, Scharnagel R. Interdisziplinäre multimodale Schmerztherapie – Grundlagen und Fallstricke. Anästh Intensivmed, 2021; 62: 334–344. doi: 10.19224/ai2021.334
- Pazan F, Weiss C, Wehling M, FORTA. The FORTA (Fit fOR The Aged) list 2018: third version of a validated clinical tool for improved drug treatment in older people. Drugs Aging, 2019; 36 (5): 481–484
- Reid MC, Eccleston C, Pillemer K. Management of chronic pain in older adults. BMJ, 2015; 350: h532
- Heuchemer L, Emmert D, Bender T et al. Schmerztherapie bei Osteoporose. Schmerz, 2020; 34: 91–104. https://doi.org/10.1007/s00482-020–00445‑1
- Sabatowski R, Schäfer D, Kasper SM, Brunsch H, Radbruch L, et al. Pain Treatment: A Historical Overview. Curr Pharm Des, 2004; 10: 701–716
- Qaseem A, Wilt TJ, McLean RM, Forciea MA. Noninvasive treatments for acute, subacute, and chronic low back pain: a clinical practice guideline from the American College of Physicians. Ann Intern Med, 2017; 166 (7): 514–530
- Ozsoy G, Ilcin N, Ozsoy I, Gurpinar B, Buyukturan O, Buyukturan B, et al. The effects of myofascial release technique combined with core stabilization exercise in elderly with non-specific low back pain: a randomized controlled, single-blind study. Clin Interv Aging, 2019; 14: 1729–1740
- Liu-Ambrose T, Khan KM, Eng JJ, Janssen PA, Lord SR, McKay HA. Resistance and agility training reduce fall risk in women aged 75 to 85 with low bone mass: a 6‑month randomized, controlled trial. J Am Geriatr Soc, 2004; 52 (5): 657–665
- Sabatowski R, Schäfer D, Kasper SM, Brunsch H, Radbruch L, et al. Pain Treatment: A Historical Overview. Curr Pharm Des, 2004; 10: 701–716
- Liu-Ambrose T, Khan KM, Eng JJ, Janssen PA, Lord SR, McKay HA. Resistance and agility training reduce fall risk in women aged 75 to 85 with low bone mass: a 6‑month randomized, controlled trial. J Am Geriatr Soc, 2004; 52 (5): 657–665
- Hicks GE, Sions JM, Velasco TO, Manal TJ. Trunk muscle training augmented with neuromuscular electrical stimulation appears to improve function in older adults with chronic low back pain: a randomized preliminary trial. Clin J Pain, 2016; 32 (10): 898–906
- Sendera M, Sendera A. Wärme- und Kältetherapie. In: Dies. Chronischer Schmerz. Schulmedizinische, komplementärmedizinische und psychotherapeutische Aspekte. Wien: Springer, 2015: 236–237
- Deutsche Rentenversicherung. Curriculum Osteoporose. Standardisierte Patientenschulung. 2021. https://www.deutsche-rentenversicherung.de/SharedDocs/Downloads/DE/Experten/infos_reha_einrichtungen/gesundheitstraining/bewegung_osteoporose.html (Zugriff am 03.02.2022)
- Morfeld J‑C, Vennedey V, Müller D, Pieper D, Stock S,. Patient education in osteoporosis prevention: a systematic review focusing on methodological quality of randomised controlled trials. Osteoporos Int, 2017; 28: 1779–1803. https://doi.org/10.1007/s00198-017‑3946‑y