Zwanzig Personen (9 Frauen, 11 Männer) mit einem Durchschnittsalter von 68,65 Jahren (Bereich 47–86 Jahre) haben teilgenommen. Die Unterschenkelamputation erfolgte durchschnittlich 43 Monate vor Studienbeginn (Bereich 3–119 Monate). Mit dem getragenen Liner maßen beide Sensoren signifikant niedrigere TcPO2-Werte im Vergleich zu den Werten, die ohne Liner nach 10, 20 und 30 Minuten gemessen wurden (TTE: p < 0,001; SPC: p = 0,002). Es wurden keine signifikanten Unterschiede in den TcPO2-Spiegeln zwischen den zwei Sensoren gefunden. Es gab keine signifikanten Assoziationen zwischen den TcPO2-Spiegeln und Schmerzen, Raucherstatus, Alter, Dauer des täglichen Einsatzes des Liners, Mobilitätsgrad und Revisionsverlauf. Die TcPO2-Spiegel in Ruhe nahmen signifikant ab, wenn nur ein Liner ohne Prothese getragen wurde. Weitere Studien sind erforderlich, um die Auswirkung des Tragens eines Liners auf den TcPO2-Spiegel bei Aktivitäten zu untersuchen.
Einleitung
In der täglichen Praxis treffen Orthopädietechniker, Orthetiker oder orthopädische Chirurgen regelmäßig auf Personen mit Unterschenkelamputation („transtibial amputation“, TTA), die beim Tragen ihrer Prothese Schmerzen im Stumpf haben 1. Dementsprechend müssen Orthopädietechniker und Chirurgen gemeinsam nach möglichen Ursachen für die Schmerzen suchen, um die Verwendung der Prothese zu erleichtern. In der täglichen Praxis der Autoren in einem ambulanten Behandlungszentrum für orthopädische Chirurgie mit einer spezialisierten Abteilung für diabetische Füße, Amputationen sowie prothetische und orthetische Nachsorge sind sie jedoch mit einer beträchtlichen Anzahl von Patienten konfrontiert, bei denen die gründliche gemeinsame Untersuchung keine spezifische somatische Pathologie als Schmerzursache ergab. Im Rahmen der oben beschriebenen kollaborativen Untersuchung wurde identifiziert, ob der Patient an Stumpfschmerzen („residual limb pain“, RLP) oder an Phantomschmerzen leidet 2 3. Während Phantomschmerz als von der amputierten Extremität ausgehend empfunden wird, wird RLP als Schmerz definiert, der im distalen Teil des Stumpfs auftritt. RLP ist ein akuter nozizeptiver Schmerz 4 5. Die meisten gemeldeten Schmerzen, die noch sechs Monate nach einer Amputation auftreten, sind Stumpfschmerzen, wobei viele Fälle auf ungenügend angepasste Prothesen zurückzuführen sind 6 7. Sowohl RLP als auch Phantomschmerz wirken sich negativ auf die allgemeine Lebenszufriedenheit eines Patienten aus 8. Dwornik et al. beschrieben nicht weniger als 23 mögliche Ursachen für RLP (Tab. 1) 9. Die meisten Ursachen stellen mechanische Probleme dar: entweder intrinsische anatomische Anomalien im Stumpf oder extrinsische Probleme durch prothetische Fehlanpassungen, zu lange verwendete Liner, schlechte Handhabung der Liner oder Silikonallergien. Alle diese mechanischen Anomalien können durch Lösung der zugrunde liegenden mechanischen Probleme behoben werden 10. Eine weitere bekannte Ursache für RLP ist die periphere arterielle Verschlusskrankheit („peripheral artery disease“, PAD)11. Leider gibt es sehr wenig Literatur zur PAD-bezogenen Perfusionsänderung im Stumpf und deren Auswirkungen auf RLP.
Zwei Fallberichte 12 13 zeigen eine Verbindung von Perfusionsrückgang im Stumpf und RLP und heben die Notwendigkeit einer stärkeren Fokussierung auf dieses Thema hervor. Die natürlichen Ursachen von PAD können allmählich zu Gefäßverschlüssen im Stumpf und Stumpfschmerzen führen. Eine äußere Kompression des Stumpfes durch das entsprechende Prothesenschaftsystem kann ebenfalls zu einer Verringerung der Durchblutung des Stumpfs führen, insbesondere der lokalen Mikroperfusion, was möglicherweise RLP auslösen kann. Der Prothesenschaft ist die Schnittstelle zwischen den menschlichen und den mechanischen Teilen des Prothesensystems. Ein fester Sitz des Prothesenschafts ist erforderlich, da auch das Körpergewicht durch die Kompression der Weichteile übertragen wird. Die meisten Prothesenschaftsysteme verwenden einen Liner 14 15 16 für Vollkontakt mit gleichmäßigerer Druckverteilung über die Kontaktfläche des Stumpfes 17, basierend auf dem hydrostatischen Volumenprinzip 18 19. Der Hersteller des in dieser Studie verwendeten Liners gibt an, dass Silikonliner eine lineare Volumenreduzierung des Stumpfes von 3 % bis 5 % distal bis 0 % proximal erzeugen. Das Schaftvolumen in entgegengesetzter Richtung wird jedoch von 3 % bis 5 % proximal auf 0 % distal reduziert. Somit wird ein quasi hydrostatischer Druck von 3 % bis 5 % am Stumpf erzeugt. Je nach Zustand des Gewebes entspricht dieser hydrostatische Druck einem Arbeitsdruck von 40 bis 70 mmHg, wodurch ein erhöhter Druck auf den Stumpf im Ruhezustand erzeugt wird, obwohl die Lastübertragung und die daraus resultierenden erhöhten Drücke aufgrund äußerer Belastung noch gar nicht ausgeübt werden. Somit ist die durch Liner hervorgerufene anfängliche Druckerhöhung eine mögliche Erklärung für RLP, da dies die lokale Perfusion verringern und eine Gefäßkompression induzieren kann.
Die Bestimmung des transkutanen Sauerstoffpartialdrucks (TcPO2) ist eine bewährte Methode zur Beurteilung der lokalen Gewebeperfusion. Dabei wird der Druck des lokal an der Haut diffundierenden Sauerstoffs mit einer Elektrode, die als Gassensor dient, bestimmt. Durch die Erwärmung der Haut auf 43 bis 44 °C und die Kapillardilatation in der Haut zur Induktion des arteriellen Blutzuflusses nähert sich der Sauerstoffpartialdruck in dieser Hautregion dem arteriellen Sauerstoffpartialdruck im peripheren Gewebe. Dies ermöglicht eine nichtinvasive Bewertung der Mikrozirkulation in einer lokalen Region durch Analyse von TcPO2 20 21 22. TcPO2 wird üblicherweise als Prädiktor für das Wundheilungspotenzial bei Geschwüren oder zur Bestimmung des angemessenen Amputationsniveaus verwendet 23 24 25 26 27 28 29 30 31. Ein TcPO2-Wert von < 40 mmHg wurde beispielsweise mit schlechten Heilungsergebnissen bei Personen mit einer Unterschenkelamputation und einem zweifach erhöhten Risiko für die Umstellung auf eine Oberschenkelamputation in Verbindung gebracht 32.
Es gibt nur wenig Literatur zur Durchblutungsänderung bei Personen mit Unterschenkelamputation. Nur in wenigen Studien wurden TcPO2-Werte in Stümpfen analysiert, aber mögliche Verbindungen zwischen TcPO2-Werten und Schmerzen wurden nicht untersucht.
TcPO2 im Stumpf bei Personen mit einer Amputation der unteren Gliedmaßen ist erheblich reduziert. Rink et al. verglichen die TcPO2-Werte in Ruhe bei fünf Personen mit einer Unterschenkelamputation (vier aufgrund eines Traumas, eine aufgrund einer Infektion) mit und ohne Tragen eines Liners 33. Es ist nicht bekannt, ob die Teilnehmer Grunderkrankungen wie PAD hatten oder an RLP litten. TcPO2 wurde an der hinteren Wadenseite gemessen. Die TcPO2-Werte in Ruhe mit Liner (41,0 ± 10,4 mmHg) waren im Vergleich zu den TcPO2-Werten ohne Liner etwa 30 % geringer (57,8 ± 9,2 mmHg). In Kontrollmessungen bei Personen ohne Grunderkrankung war diese Verringerung sogar noch größer, was einem Rückgang von fast 50 % entspricht.
Bramley et al. verglichen die TcPO2-Werte zwischen der amputierten und der nicht amputierten Seite bei einer Person mit einer Unterschenkelamputation 34. Durch eine aufblasbare Manschette wurde Druck auf die nicht amputierte Seite ausgeübt, wobei die Druckgrößen dem Druck ähnelten, den eine pneumatische Mobilitätshilfe nach einer Amputation ausübt. Dies sollte den Druck simulieren, den der Stumpf durch eine Unterschenkelprothese erfährt. TcPO2 wurde an drei Stellen gemessen: an der Patellasehne, der seitlichen Wade und der hinteren Wade. Der Druck wurde kontinuierlich durch die aufblasbare Manschette erhöht, bis nach 50 Minuten 60 mmHg erreicht waren. Die TcPO2-Werte zeigten an allen drei Stellen eine Abnahme von mehr als 25 % gegenüber dem Ausgangswert, wobei die seitliche Wade und die Patellasehne mehr als 75 % Reduktion gegenüber dem Ausgangswert aufwiesen. Die visuell geschätzte Abnahmerate der TcPO2-Werte an der hinteren und seitlichen Wadenstelle schien am Stumpf größer zu sein als auf der kontralateralen, nicht amputierten Seite. Sobald der Druck abgelassen wurde, wurde eine reaktive Überkompensation von bis zu 25 % gegenüber dem Ausgangswert festgestellt. Zehn Minuten nach dem Entfernen der Manschette war keiner der Messwerte an den Messstellen auf das Ausgangsniveau zurückgekehrt. Leider wurden keine tatsächlichen TcPO2-Messwerte angegeben, und es ist nicht bekannt, ob der Teilnehmer RLP erfuhr.
Angesichts der vorgelegten Informationen bestand das primäre Studienziel darin, Veränderungen der TcPO2-Werte in Ruhe während der Verwendung von Linern in der Population zu bestimmen, die die Autoren am häufigsten sehen: Personen mit PAD und Personen mit anhaltendem RLP ohne somatische Pathologie als Ursache. Die sekundären Studienziele waren die Bewertungen möglicher Korrelationen von TcPO2-Werten in Ruhe mit Raucherstatus, Alter, Geschlecht, Mobilitätsniveau, täglicher Verwendungsdauer des Liners und Revisionsoperationen nach der Amputation.
Methoden
Klinisches Umfeld
Die Universitätsklinik Balgrist ist ein tertiäres Behandlungszentrum für orthopädische Chirurgie mit einer spezialisierten Abteilung für die Behandlung von diabetischen Füßen, orthopädischen Komplikationen bei PAD, Amputationen sowie für prothetische und orthetische Nachsorge. Die Einheit besteht aus drei Fachärzten für orthopädische Chirurgie, zwei Internisten, einem Spezialisten für Infektionskrankheiten und einem Team von mehr als zehn Orthopädietechnikern. Es bestehen Verbindungen zu den Abteilungen für Angiologie und Gefäßchirurgie des Universitätsspitals Zürich. Ein speziell auf die Bedürfnisse des einzelnen Patienten abgestimmtes Team untersucht die Situation des Patienten in interdisziplinärer Zusammenarbeit. Es sind immer mindestens ein orthopädischer Chirurg sowie ein Techniker für Prothetik und für Orthetik beteiligt.
Studienteilnehmer
Die Studie wurde genehmigt von der örtlichen Ethikkommission „Kantonale Ethikkommission Zürich, Stampfenbachstrasse 121, 8090 Zürich, Schweiz“ (BASEC-Nr. 2016–00395). Alle Studienteilnehmer gaben eine schriftliche Einverständniserklärung ab. Patienten, die zwischen 2007 und 2017 an unserer Einrichtung eine Unterschenkelamputation erhalten hatten, konnten an der Studie teilnehmen. Alle Unterschenkelamputationen wurden von oder unter der direkten Aufsicht eines leitenden orthopädischen Chirurgen durchgeführt. Die Amputationen wurden wie von Burgess und Zettl beschrieben durchgeführt 35.
Die Rekrutierung potenzieller Studienteilnehmer erfolgte zwischen März und September 2017. Einschlusskriterien waren: älter als 18 Jahre, Unterschenkelamputation, Ausstattung mit einer endgültigen Prothese, die ein Prothesenlinersystem enthält, tägliche Verwendung der Prothese mindestens zwei Stunden pro Tag und RLP länger als drei Stunden pro Tag. Ausschlusskriterien waren: somatische Ursachen für RLP (nach Tab. 1), Radikulopathie, Knochentumor als Amputationsindikation und Drogen- oder Alkoholmissbrauch.
Für alle Teilnehmer wurde eine standardisierte Anamnese durchgeführt, die Angaben zum Amputationsniveau beinhaltete, den Grund für die Amputation, Vorhandensein bzw. Nichtvorhandensein von PAD und/oder Diabetes mellitus, Raucheranamnese, Mobilitätsgrad (K‑Level) auf Grundlage des Amputee Mobility Predictor 36, Schmerzintensität bei Verwendung der Prothese (bewertet anhand des Fragebogens zur Prothesenevaluation, Gruppe 2, Frage I, in dem die Schmerzen mit einem visuellen Standardanalogwert [VAS] bewertet werden) 37 und die täglichen Zeiten des Prothesengebrauchs. Nach Aufnahme der standardisierten Krankengeschichte füllten die Teilnehmer den SF-36-Fragebogen aus.
TcPO2-Testaufbau
Das verwendete TcPO2-Messgerät (TCM4 Series ETX391-880R0263N0152014, Radiometer, Bronshoj, Dänemark, zuletzt gewartet am 27. Juli 2015) wurde 2006 von Groullier et al. validiert 38. Zur Messung von TcPO2 wurden Clark-Sensoren in das Gerät integriert 39.
Zu Standardisierungszwecken gaben die Orthopädietechniker allen Studienteilnehmern den Liner „Iceross Comfort Cushion“ (Össur, Reykjavik, Island) für die Dauer der Messung. Jeder Teilnehmer erhielt die richtige Linergröße für seinen Stumpf. Die Dicke des Liners an den Messpunkten betrug 7 mm.
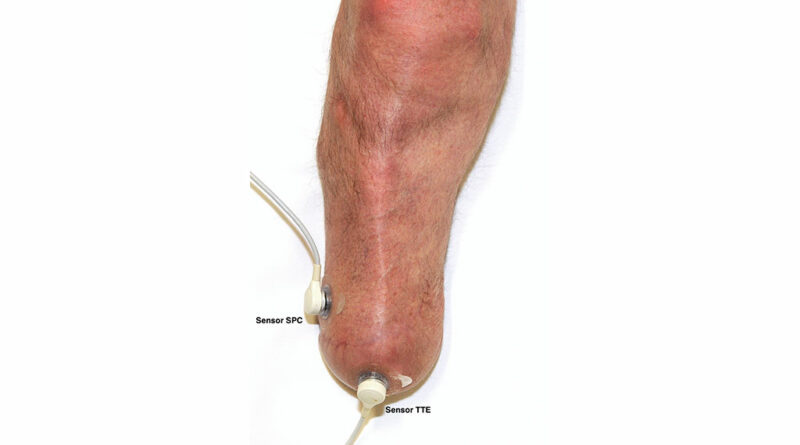
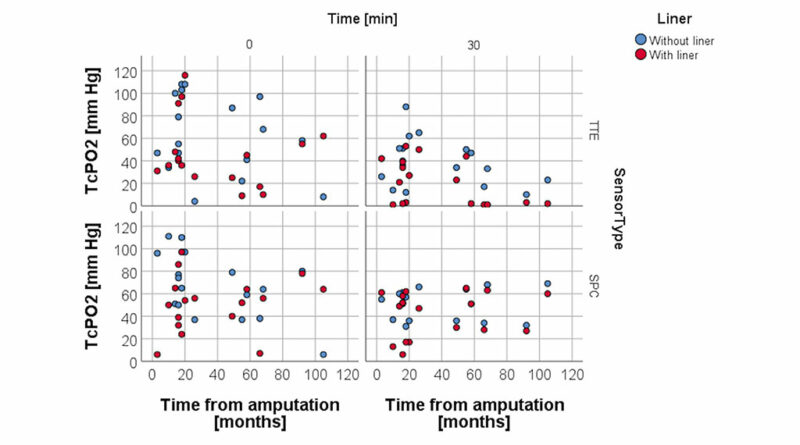
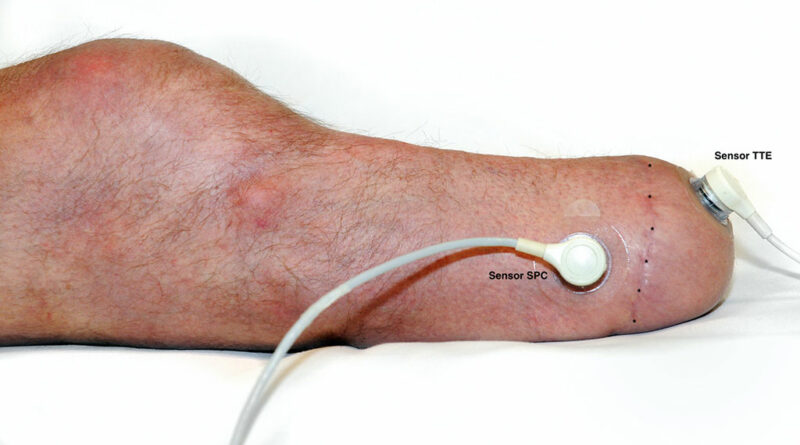
Zum Zweck der TcPO2-Messungen wurden die Studienteilnehmer in Rückenlage gebracht, die als beste Position für die Diskriminierung von Ischämien der Extremitäten beschrieben wird 40 41. Das Knie war während des gesamten Messvorgangs vollständig gestreckt. Alle Messungen wurden in Ruhe durchgeführt, d. h., vor der Testsitzung wurden keine Aktivitäten durchgeführt. Die Sensoren wurden vom TCM4-Messgerät automatisch kalibriert und erwärmt. Es wurden zwei Sensorelektroden verwendet, die direkt auf die Haut des Stumpfes platziert wurden, nachdem die Haut mit Alkohol gereinigt und mit einem Mulltupfer getrocknet worden war. Kontaktflüssigkeit (Radiometer, Bronshoj, Dänemark) wurde gemäß der Gebrauchsanleitung in den Raum zwischen Haut und Sensor eingefüllt. Ein Sensor wurde in der Horizontalebene über der Spitze des Tibiaendes (Sensor TTE) platziert, wo der verbleibende Gastrocnemiuslappen fixiert ist; der zweite Sensor wurde in der Sagittalebene distal über dem peronealen Kompartiment (Sensor SPC) platziert (Abb. 1 u. 2). Diese Stellen wurden gewählt, weil sie die distalsten Teile des hinteren Hautlappens (Sensor TTE) bzw. des vorderen Hautlappens (Sensor SPC) darstellen. An diesen Orten ist die Perfusion am stärksten eingeschränkt, und sie stellen das Worst-Case-Perfusionsszenario dar.
Die Messungen wurden für alle Teilnehmer in der gleichen Reihenfolge durchgeführt, d. h., es wurde das gleiche Protokoll für jeden Studienteilnehmer durchgeführt. Zu Beginn der Testsitzung lag die zu testende Person auf einer Liege auf dem Rücken, beide Beine gestreckt und mit freigelegtem Stumpf (keine Prothese und kein Liner). Nach einer 15-minütigen Akklimatisierungszeit, in der gemäß der Bedienungsanleitung die Kalibrierung, die Erwärmung der Sonden auf 44 °C und der Haut durch die Sensoren erfolgten, wurde die erste Basismessung (T0) ohne den Liner aufgezeichnet. Danach wurden drei weitere Messungen ohne den Liner nach 10, 20 und 30 Minuten durchgeführt, insgesamt also vier Messungen (T0, T10, T20, T30). Das gleiche Verfahren wurde wiederholt, diesmal aber mit angelegtem Liner. Um druckbedingte Messfehler sowie Druckgeschwüre zu vermeiden, wurden kleine Löcher entsprechend der Größe der Sensoren aus dem Liner ausgestanzt, sodass kein externer Druck auf die Sensoren ausgeübt wurde. Das Stanzen der Löcher in den Liner dauerte ungefähr eine Minute, während der Teilnehmer auf der Liege liegen blieb. Keiner der Sensoren wurde entfernt. Die TcPO2-Daten wurden visuell abgerufen.
Statistische Analysen
Die statistischen Analysen wurden mit SPSS (Version 23, IBM Corp., Chicago, Illinois, USA) durchgeführt. Eine Trennschärfeanalyse (Alpha-Fehler auf 0,05 eingestellt) ergab eine Mindeststichprobengröße von 13 Teilnehmern. Die entsprechende zugrunde liegende Annahme war ein TcPO2-Wert von 35 mmHg für Bedingung 1 (ohne Liner) und ein TcPO2-Wert von 50 mmHg für Bedingung 2 (mit Liner) mit einer Standardabweichung von 15 mmHg. Da die visuelle Datenprüfung eine Abweichung von der Normalverteilung der TcPO2-Werte sowohl für die Sensoren als auch für die Bedingungen zeigte, wurde ein Shapiro-Wilk-Test auf Normalverteilung angewendet, der diesen ersten Eindruck bestätigte. Somit wurden nichtparametrische statistische Tests durchgeführt. Wilcoxon-Vorzeichen-Rang-Tests wurden verwendet, um die TcPO2-Werte zwischen den beiden Bedingungen zu untersuchen, die zu den verschiedenen Zeitpunkten gemessen wurden. Um einen möglichen Zeiteffekt auf die beiden getesteten Bedingungen zu testen, wurde ein nichtparametrisches Modell mit wiederholten Messungen (Friedman-Test) verwendet, um die absoluten Unterschiede der TcPO2-Werte innerhalb der jeweiligen Bedingung zu untersuchen.
Mögliche unterschiedliche Auswirkungen der beiden Bedingungen auf die unterschiedlichen TcPO2-Werte für dichotome Variablen wurden unter Verwendung von Mann-Whitney-U-Tests bewertet. Spearman-Rangkorrelationsanalysen bewerteten die Assoziationen zwischen numerischen demografischen Parametern und TcPO2-Werten zu Studienbeginn.
Ergebnisse
Teilnehmer
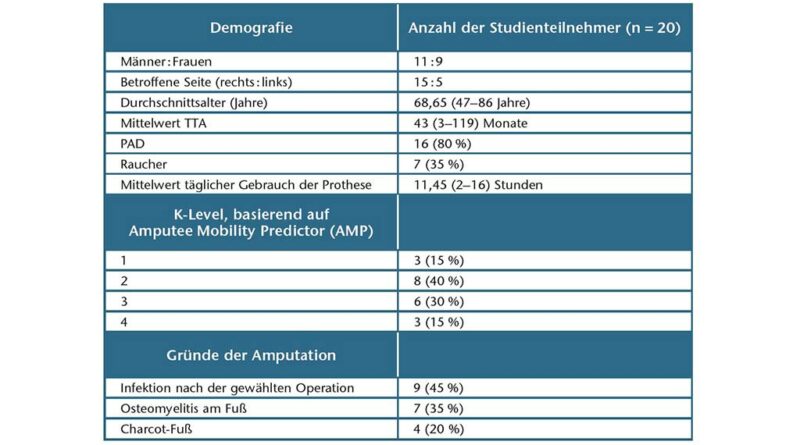
Zwanzig Teilnehmer (11 Männer, 9 Frauen) mit einem Durchschnittsalter von 68,65 Jahren (Spannbreite 47–86 Jahre) nahmen an der Studie teil. Die demografischen Daten der Teilnehmer werden in Tabelle 2 gezeigt. Die mittlere Zeit von der Amputation bis zu den TcPO2-Messungen betrug 43 (Spannbreite 3–119) Monate. Bei neun Teilnehmern waren Wundkomplikationen nach früheren chirurgischen Fußoperationen der Grund für die Amputation: vier Arthrodesen und fünf kleinere Fußamputationen. Weitere Gründe für eine Amputation waren Osteomyelitis aufgrund von Druckgeschwüren bei sieben Teilnehmern und Komplikationen der Charcot-Arthropathie (infizierte Druckgeschwüre mit nachfolgender Osteomyelitis) bei vier Teilnehmern. Vier Teilnehmer mussten zudem nach der Amputation einer Revisionsoperation unterzogen werden. Es waren keine Ulzerationen vorhanden, als die TcPO2-Messungen durchgeführt wurden.
SF-36
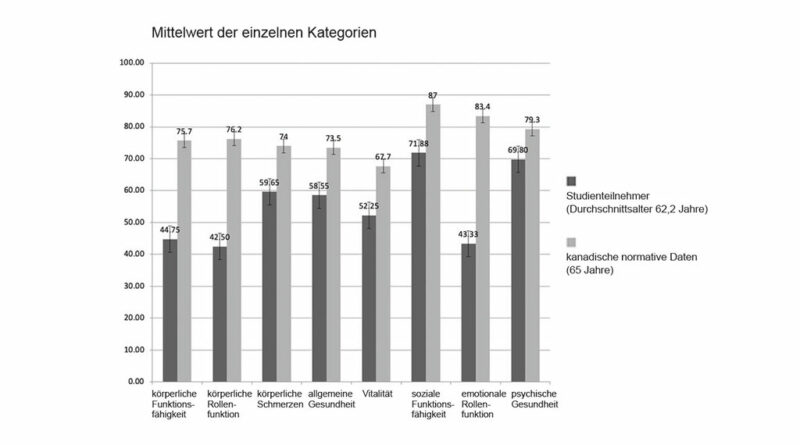
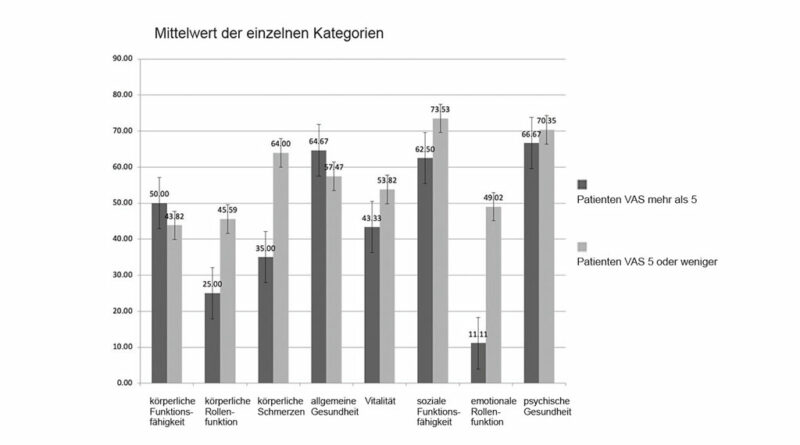
Alle SF-36-Ergebnisse sind in den Abbildungen 3 und 4 dargestellt. Im Vergleich zu altersbezogenen normativen Daten 42 erzielten die Studienteilnehmer in allen Teilwerten niedrigere Werte (Abb. 3). Darüber hinaus erzielten Teilnehmer, bei denen Schmerzen mit VAS ≥ 5 auftraten, höhere Werte bei körperlicher Funktionsfähigkeit und allgemeiner Gesundheit, geringere Werte hingegen in allen anderen SF-36-Teilbereichen (Abb. 4). Der Vergleich der SF-36-Ergebnisse mit den K‑Levels ergab, dass Teilnehmer mit einem K3-Level oder höher ihre körperliche und geistige Gesundheit niedriger bewerteten als Teilnehmer mit einem K2-Level oder weniger.
TcPO2 in Ruhe und Zeit
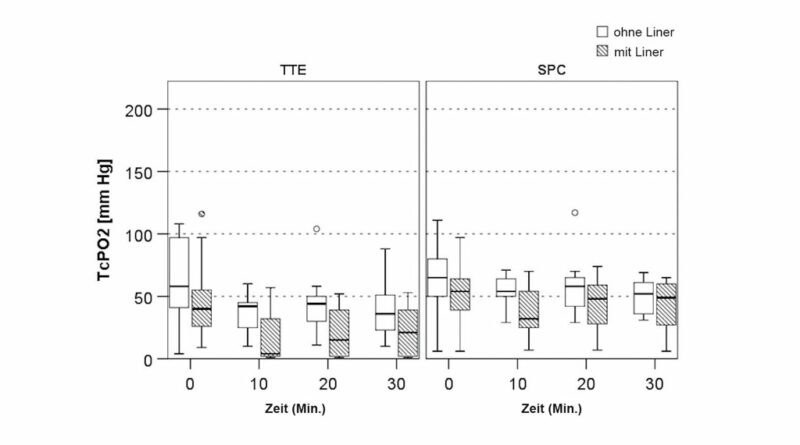
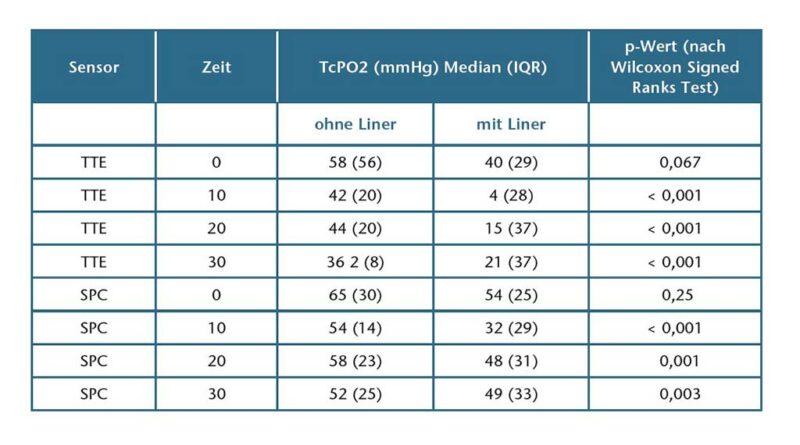
Bei der anfänglichen TcPO2-Messung T0 wurden für beide Sensoren keine statistisch signifikanten Unterschiede zwischen den Bedingungen 1 und 2 festgestellt, obwohl die TcPO2-Werte an beiden Sensorstellen mit Bedingung 2 niedriger waren. Alle TcPO2-Werte in Ruhe nahmen nach 10, 20 und 30 Minuten Tragen eines Liners signifikant ab (Abb. 3 u. 5).
Der Friedman-Test auf Zeit für die gepaarten Unterschiede bei TcPO2 in Ruhe war für beide Sensoren nicht signifikant: TTE (ꭓ 2(3) = 2,578; p = 0,461) und SPC (ꭓ 2(3) = 2,132; p = 0,545). Diese Ergebnisse deuten darauf hin, dass der mittlere TcPO2-Wert in Ruhe zwischen den beiden Bedingungen nicht unterschiedlich durch die Zeit beeinflusst wird.
TcPO2 in Ruhe und die Variablen Schmerz, Alter, tägliche Verwendung der Prothese und Zeit seit Amputation
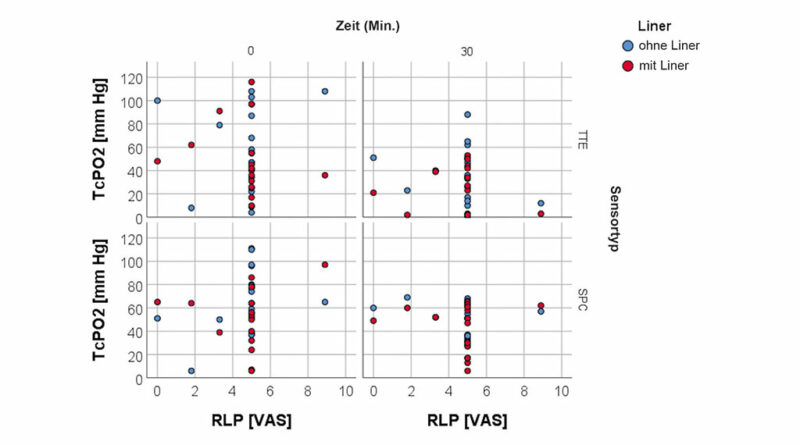
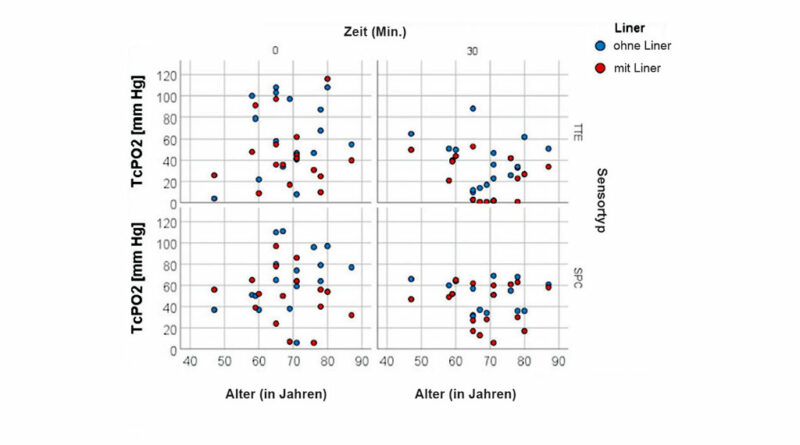
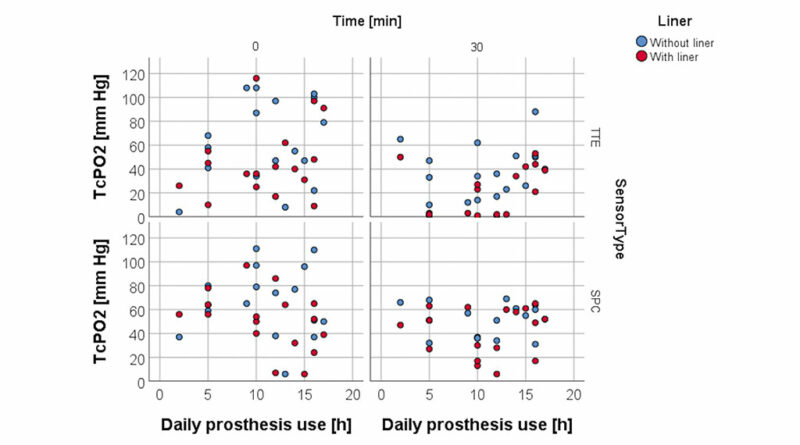
RLP wurde unter Verwendung einer VAS beurteilt, um die durchschnittliche Schmerzmenge innerhalb der letzten vier Wochen zu bewerten. Die Spearman-Rangkorrelationsanalyse für TcPO2 in Ruhe und die VAS-Ergebnisse für RLP (Abb. 6), die bei Studieneintritt erhoben wurden, waren für beide Sensoren unter beiden Bedingungen nicht signifikant, ebenso wie die Analyse für TcPO2 in Ruhe sowie Alter (Abb. 7), tägliche Verwendung der Prothese (Abb. 8) und für Zeit seit Amputation (Abb. 9).
TcPO2 in Ruhe und Geschlecht
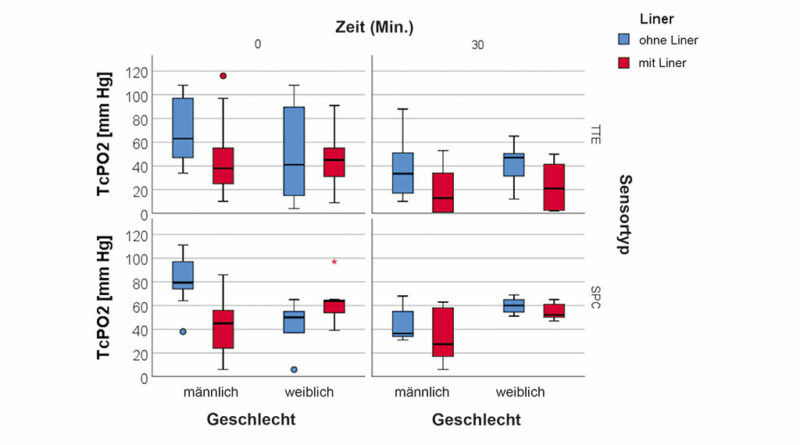
Mann-Whitney-U-Tests wurden verwendet, um die Assoziation von TcPO2-Werten und Geschlecht zu bewerten. Für Sensor TTE gab es keine statistisch signifikanten Unterschiede in TcPO2 zwischen Frauen und Männern, unabhängig davon, ob ein Liner getragen wurde oder nicht. Für Sensor SPC variierten die Ergebnisse jedoch: Ohne Liner hatten Frauen zu Studienbeginn einen signifikant höheren TcPO2-Wert (Medianunterschied = 29,5 mmHg, p = 0,003). Dieser Unterschied blieb bei T30 erhalten: Der Medianwert für Männer betrug 36,5 mmHg, während der Medianwert für Frauen 60,0mmHg betrug (p = 0,028). Beim Tragen eines Liners wurden jedoch bei T0 (Medianunterschied = 19,0 mmHg, p = 0,107) oder bei T30 (Medianunterschied = 24,5 mmHg, p = 0,051) keine Unterschiede zwischen Männern und Frauen beobachtet (Abb. 10; Tab. 3).
TcPO2 in Ruhe und die Variablen K‑Level und Revisionsoperation
Eine einfache ANOVA wurde durchgeführt, um die Auswirkungen von K‑Level und Revisionsoperation auf die TcPO2-Werte in Ruhe zu bewerten. Die Analysen zeigten keinen statistisch signifikanten Unterschied für TcPO2 zu Studienbeginn bei den verschiedenen Arten von K‑Level (mit Liner: TTE: p = 0,117, SPC: p = 0,453; kein Liner: TTE: p = 0,208, SPC: p = 0,906). Somit hatte das Aktivitätsniveau keinen Einfluss auf das TcPO2 in Ruhe. Auch eine bereits erfolgte Revisionsoperation zu Studienbeginn hatte keinen statistisch signifikanten Effekt auf die TcPO2-Werte in Ruhe (mit Liner: TTE: p = 0,257, SPC: p = 0,950; kein Liner: TTE: p = 0,528, SPC: p = 0,801).
Diskussion
Trotz eines interdisziplinären Ansatzes für jeden Patienten gibt es in der Klinik der Autoren eine beträchtliche Anzahl von Personen mit einer Unterschenkelamputation, bei denen RLP täglich länger als drei Stunden auftritt. Es liegt keine spezifische somatische Pathologie wie Osteitis, Osteomyelitis, Abszess oder schlechte Knochengestaltung als Ursache dieses Schmerzes vor. Häufige Probleme im Zusammenhang mit der Stumpfhaut, die RLP verursachen können, wie Weichteilüberschuss, Hautverletzungen, Geschwüre, Neurome, Hämatome oder Hautallergien, sind ebenfalls nicht die Ursache. Eine ungenügende Prothesenanpassung oder eine Degeneration benachbarter Gelenke sind für diese Fälle ebenfalls nicht verantwortlich. Viele dieser Patienten haben jedoch PAD. Zwei Fallberichte verknüpfen PAD mit RLP 43 44. Beide heben die Notwendigkeit einer stärkeren Fokussierung auf einen möglichen Gefäßverschluss (oder: eine mögliche Claudicatio) im Stumpf hervor. Wir waren daher daran interessiert, zu analysieren, ob eine verringerte lokale Mikroperfusion, die durch die von einem Liner selbst ausgeübte Kompression induziert wird, mit RLP zusammenhängt. Eine solche verringerte Mikroperfusion würde sich als verringerter TcPO2-Wert in Ruhe zeigen.
Diese Ergebnisse zeigten, dass die TcPO2-Werte in Ruhe tatsächlich signifikant abnahmen, wenn die Teilnehmer ihren Liner verwendeten, was auf eine verringerte Perfusion hinweist. Ein signifikanter Abfall der TcPO2-Werte in Ruhe wurde innerhalb der ersten 10 Minuten der Verwendung des Liners beobachtet, d. h. von T0, der Basismessung, bis T10. Nach diesem Abfall stabilisierten sich die TcPO2-Werte in Ruhe, und es konnten keine weiteren signifikanten Abnahmen festgestellt werden. Diese Ergebnisse bestätigen unsere Hypothese, dass die durch einen Liner allein induzierte Kompression die Mikroperfusion unmittelbar nach dem Anlegen des Liners verringert. Die Mikroperfusion ist möglicherweise in der Lage, sich an die erhöhte Kompression anzupassen, wie der leichte Anstieg der TcPO2-Werte zwischen T10 und T20 andeutet. Danach bleibt die Reduktion bei den Messungen bei T20 und T30 über den 30-Minuten-Zeitraum relativ konstant.
Ein ähnliches Muster bei der Abnahme der TcPO2-Werte in Ruhe wurde jedoch auch beobachtet, wenn die Teilnehmer ihren Liner nicht verwendeten. Diese Erkenntnis impliziert, dass unabhängig von der Verwendung des Liners ein Rückgang des TcPO2-Wertes in Rückenlage während der 30 Minuten, in denen Aufzeichnungen durchgeführt wurden, erfolgt, wobei der Rückgang mit einem angezogenen Liner größer war. Ähnliche Ergebnisse wurden von Rink et al. 45 dokumentiert. Sie waren an der Hautgesundheit von Personen mit einer Unterschenkelamputation interessiert und bewerteten die TcPO2-Werte in Ruhe, die Perfusion der Weichteile durch Laser-Doppler-Durchflussmessung sowie die Hauttemperatur. Alle drei Messungen wurden an der hinteren Seite des Stumpfes durchgeführt, wobei der TcPO2 am weitesten distal gemessen wurde. Der mittlere TcPO2-Wert in Ruhe für ihre 5 Teilnehmer betrug 57,8 mmHg ± 9,2, ein Wert, der nach einer Akkommodationszeit von 15 Minuten anhand einer 1‑minütigen kontinuierlichen Aufzeichnung gemittelt wurde. Da die Position des TcPO2-Sensors posterior war und die Werte aus einer kontinuierlichen Aufzeichnung gemittelt wurden, ist ein direkter Vergleich mit unseren Ergebnissen nicht möglich. Am nächsten an ihrer Messstelle lag der SPC-Sensor: Die TcPO2-Werte in Ruhe für den angelegten Liner bei T0, die Basismessung, die direkt nach einer Akkommodationszeit von 15 Minuten durchgeführt wurde, betrug 51,6mmHg ± 22,7. Dieses Ergebnis ist punktbasiert und wurde anhand von 20 Teilnehmern mit einer viel größeren Standardabweichung ermittelt. Die nächste Messung erfolgte zehn Minuten später bei T10 und zeigte einen stark reduzierten Wert von 40 mmHg ± 14,5. Die von Rink et al. verwendete Methode zur Ermittlung der TcPO2-Werte in Ruhe unterschied sich ebenfalls von der der Autoren. Um Sonden- und Sensorstörungen zu minimieren, entwickelten Rink et al. einen Silikonsondenhalter, in den die Sonde, die Sensoren und die entsprechenden elektrischen Kabel gleichmäßig eingebettet waren, um eine bündige Oberfläche gegenüber der Haut des Stumpfs zu erzeugen 46. Da die Außenseite des Sondenhalters ebenfalls glatt war, entstand eine etwas voluminösere Wade, was durch einen größeren Liner ausgeglichen werden konnte. Mit ihrem enganliegenden Aufbau kommt ihr Ansatz höchstwahrscheinlich einer „realen“ Situation, in der ein Liner angezogen wird, am nächsten.
Die TcPO2-Aufzeichnungen von Sensor SPC während des Tragens des Liners waren höher als die Aufzeichnungen bei gleicher Bedingung bei Sensor TTE. Der Messort beeinflusst die TcPO2-Werte erheblich. Das von Taylor und Palmer erstmals eingeführte Angiosomkonzept 47 liefert eine mögliche Erklärung: Während sich Sensor TTE im Gebiet der Arteria tibialis posterior befand, wurde Sensor SPC an der Verbindungsstelle der Arteria suralis und der Arteria descendens genucilaris platziert. Diese doppelte Blutversorgung kann zu den höheren TcPO2-Werten geführt haben, die mit Sensor SPC beobachtet wurden. Ferner könnten die verbleibenden peronealen Muskelbäuche dicker sein als das verbleibende Gastrocnemius-Muskelgewebe unter der Tibiaspitze, insbesondere bei Patienten mit PAD, bei denen viele Chirurgen den Musculus soleus entfernen.
Aufgrund der begrenzten Literatur, die zum Vergleich der Ergebnisse zur Verfügung steht, haben die Autoren Ergebnisse aus Thermografie-Daten verwendet, da sie gut mit Messungen von TcPO2 in Ruhe korrelieren 48. Thermografische Ergebnisse aus der Literatur zeigen ebenfalls eine hohe Abhängigkeit vom Messort, ähnlich wie die Ergebnisse der Autoren. Peery et al. zeigten einen allgemeinen Anstieg der Hauttemperatur nach einer Ruhezeit von 15 Minuten mit einer angelegten Prothese bei ihren Teilnehmern mit einer Unterschenkelamputation 49. Ein Vergleich ihrer Sensorposition und unserer Sensorplatzierung zeigt, dass sie an ähnlichen Stellen wie denen der Autoren einen Temperaturrückgang registriert haben 50 51. Der von Peery et al. beobachtete Temperaturanstieg scheint nicht mit der Durchblutung zu korrelieren, sondern könnte eine thermische Reaktion auf Druck durch Scherkräfte sein 52, da ihre Teilnehmer ihre Prothese anzogen, während Ruhemessungen durchgeführt wurden. Scherkräfte scheinen die TcPO2-Werte weiter zu senken, wenn sie zur normalen Belastung hinzukommen 53.
Leider konnten die Autoren keinen Zusammenhang zwischen TcPO2-Werten in Ruhe und RLP nachweisen. Eines der Einschlusskriterien für unsere Teilnehmer war, dass sie beim Tragen der Prothese mehr als drei Stunden pro Tag RLP hatten. Somit beeinträchtigt RLP unsere Studienpopulation erheblich. RLP, das aufgrund eines schlechtsitzenden Prothesenschafts ausgelöst wurde, kann ausgeschlossen werden, da alle Schäfte gut angepasst waren und für keinen der Teilnehmer ein Problem darstellten. RLP infolge der Ausrichtung der Prothese kann jedoch nicht ausgeschlossen werden. Kobayashi et al. zeigten einen signifikanten Zusammenhang zwischen selbst kleinen Fehlstellungen von 2° bei Abduktion und Adduktion und dem Reaktionsmoment des Schafts 54. Da der Druck innerhalb des Schaftes nicht gemessen wurde, ist nicht bekannt, ob das aufgezeichnete Reaktionsmoment des Schafts zu einem Anstieg des Schaftdrucks führte. Diese Drücke könnten gering sein und von den Linern so absorbiert werden, dass keine Druckspuren auf der Stumpfhaut sichtbar sind. Ein erhöhter Druck, der nicht als Druckspur auf der Haut in Erscheinung tritt, könnte jedoch einen Einfluss auf die Gewebeperfusion haben.
Dass keine Assoziation zwischen reduziertem TcPO2 in Ruhe und Schmerz gefunden wurde, ist kein Indikator dafür, dass kein Zusammenhang besteht. Das Verhältnis von Symptomintensität und Ischämie bei PAD ist komplex und oft sehr individuell. Beispielsweise zeigten TcPO2-Messungen, die beim Gehen auf dem Laufband aufgezeichnet wurden, dass schwere Ischämie und Schmerzen nicht gleichzeitig auftreten müssen und dass Schmerzen trotz anhaltender signifikanter Ischämie unabhängig vom Ort verschwinden können 55 56. Dennoch haben Schorr et al. berichtet, dass rund 69 % von 120 Laufband-Belastungstests wegen Schmerzen gestoppt werden mussten 57. Es fehlt Literatur darüber, wie TcPO2-Werte bei Aktivität sich auf die Schmerzen bei Personen mit einer Unterschenkelamputation auswirken, während diese gehen.
Das Ausmaß der täglichen Nutzung des Liners, das Mobilitätsniveau (K‑Level), das Alter, Revisionsoperationen und der Raucherstatus hatten keinen signifikanten Einfluss auf die TcPO2-Werte. Frauen hatten nach 30 Minuten Liner-Nutzung bei Sensor SPC signifikant höhere TcPO2-Werte als Männer, was bedeutet, dass ihre durch TcPO2 gemessene Gewebeperfusion an dieser Stelle besser war als bei den Männern. Da den Autoren geschlechtsspezifische Unterschiede im Angiosomkonzept nicht bekannt sind, könnte dieses Ergebnis entweder Zufall sein oder ein Hinweis auf ein unterschiedliches Maß an Weichteilschrumpfung bei Frauen. Bisher verzeichnet die Literatur keine Unterschiede im Ausmaß der Weichteilschrumpfung zwischen Männern und Frauen 58. Alternativ kann dieses Ergebnis tatsächlich ein Zeichen für Geschlechtsunterschiede bei Angiosomen sein.
Einschränkungen der Studie
Diese Studie weist mehrere Einschränkungen auf: Alle Tests wurden aus logistischen Gründen zwischen 13 und 17 Uhr durchgeführt. Die Teilnehmer wurden zwar aufgefordert, die Verwendung von Linern und Prothesen am Testtag bis nach Durchführung des Tests einzustellen, doch könnte eine mangelnde Einhaltung die TcPO2-Startwerte beeinflusst haben.
Alle Messungen wurden in Ruhe und mit den Teilnehmern in Rückenlage durchgeführt. Da mit den Teilnehmern keine Kontrollmessungen durchgeführt wurden, z. B. in sitzender Position, wobei sich der Stumpf eher in vertikaler als in horizontaler Position befindet, können wir nicht bestimmen, welchen Einfluss die Rückenlage auf die TcPO2-Werte hatte. Die Auswirkung des Stehens und Gehens auf die TcPO2-Werte während der Verwendung eines Liners bleibt unklar. Bei Personen ohne Amputation unterscheiden sich die TcPO2-Werte bei Aktivität von den TcPO2-Werten in Ruhe um bis zu 50 mmHg 59 60 61 62.
Die Methode der Autoren, Löcher in Sensorgröße in den Liner zu stanzen, um den durch den Liner verursachten Druck auf die Sensoren zu verringern, entspricht möglicherweise nicht der Situation eines nicht modifizierten Liners. Wie stark diese Löcher die Messwerte beeinflussen, ist schwer zu beurteilen. Lenz und Bush beschrieben in einer Fallstudie die Auswirkungen von Normal- und Scherkräften an der Schnittstelle zwischen Schaft und Liner einer getragenen Unterschenkelprothese 63. Es wurde mit größter Sorgfalt darauf geachtet, ein genaues Duplikat der aktuellen Prothese des Teilnehmers zu erstellen. In ihrer letzten Testbedingung (Bedingung 3) wurde ein großes Loch (> 4 cm Durchmesser) in den Liner aus Gel geschnitten, um Wägezellenmessungen direkt auf Hautebene zu ermöglichen. Beim Vergleich von Bedingung 3 mit Bedingung 1, bei der Kraftmessungen an der Prothesenwand durchgeführt wurden, zeigten ihre Ergebnisse eine signifikante Abnahme der Normal- und Scherkräfte während des gesamten Gangzyklus mit Bedingung 3. Bei Übertragung ihrer Ergebnisse auf unsere Situation würden Löcher im Liner die vom Liner auf den Stumpf ausgeübten Kräfte verringern, wodurch auch die Kompression verringert wird. Bei beiden Sensoren und zu allen Zeitpunkten außer bei der Ausgangsmessung wurde jedoch beim Tragen des Liners eine signifikante TcPO2-Reduktion beobachtet. Dies zeigt an, dass der Effekt des Liners trotz seiner kleinen Löcher immer noch vorhanden war. Trotzdem ist eine Untererfassung der in den Liner-Zustand der Autoren tatsächlich gemessenen Werte möglich. Vorsicht ist auch geboten, wenn die vorliegenden Ergebnisse auf andere Arten von Linern übertragen werden, da über unterschiedliche Linermaterialien und ihre Auswirkungen auf die Leistung in vivo nur wenig bekannt ist 64. Darüber hinaus sind die Linergrößen nicht durchgehend. Vielmehr werden unterschiedliche Stumpfumfänge in Größenkategorien gebündelt. Innerhalb einer bestimmten Kategorie kann der Druck variieren, je nachdem, ob sich der Stumpfumfang an der Grenze zur nächsten Kategorie befindet oder in der Mitte der Kategorie liegt. Somit ist die Linergröße eine potenzielle Störvariable, die möglicherweise zu der größeren Variabilität beigetragen hat, die bei der Bedingung mit angezogenem Liner beobachtet wurde.
Abschließend wurde der Schmerz nicht zu den Zeitpunkten T0, T10, T20 und T30 gemessen, sondern zu Studienbeginn. Mögliche Änderungen des RLP sollten in weiteren Studien bewertet werden, um mögliche Schmerzänderungen während der Messungen zu bestimmen.
Fazit
Im Vergleich zu TcPO2 in Ruhe ohne Silikonliner wurde ein signifikant reduzierter TcPO2 in Ruhe mit Liner innerhalb der hier untersuchten spezifischen Population überwiegend von PAD betroffener Personen beobachtet. Es konnte jedoch kein Zusammenhang zwischen TcPO2 in Ruhe und Schmerz gefunden werden. Von allen Variablen, die auf einen möglichen Einfluss auf die TcPO2-Werte in Ruhe getestet wurden (d. h. Rauchen, Alter, Geschlecht, Mobilitätsgrad, Dauer der täglichen Verwendung des Liners und Revisionsoperation), war nur das Geschlecht signifikant: Frauen hatten signifikant höhere TcPO2-Werte in Ruhe für Sensor SPC bei T0 und T30. Weitere Studien sind erforderlich, um zu untersuchen, ob dies auch bei der Messung der TcPO2-Werte in dynamischen Situationen gilt.
Danksagung
Die Autoren bedanken sich bei Frau Dagmar Gross für ihre Hilfe bei der Manuskripterstellung. Des Weiteren danken die Autoren den folgenden Orthopädietechnikern von Balgrist Tec, Zürich, Schweiz, für die technische Unterstützung: David Egger, Naemi Käser, Florian Müller und Sergio Stefanelli.
Hinweis
Bei diesem Artikel handelt es sich um eine ergänzte deutsche Übersetzung des folgenden Artikels: Berli MC, Jundt-Ecker M, Meier MR, Hofer M, Schöni M, Götschi T, et al. Resting TcPO2 levels decrease during liner wear in persons with a transtibial amputation. PLoS ONE, 2020; 15 (9): e0239930. https://doi.org/10.1371/journal.pone.0239930
Für die Autoren:
Dr. med. Martin Berli
Stellvertretender Leiter Technische
Orthopädie
Universitätsklinik Balgrist
Forchstrasse 340
CH-8008 Zürich
Schweiz
martin.berli@balgrist.ch
Begutachteter Beitrag/reviewed paper
Berli MC, Jundt-Ecker M, Meier MR, Hofer M, Schöni M, Götschi T, Uçkay I, Böni Th, Waibel FWA. Sinkende TcPO2-Werte während Ruhemessungen durch Tragen eines Liners bei Personen mit Unterschenkelamputation. Orthopädie Technik, 2021; 72 (8): 36–47
- Entwicklung eines zum physiologischen Gangbild kongruenten polyzentrischen Knieorthesengelenks – Zwischenstand eines Forschungsprojektes — 10. April 2026
- Mikroprozessorgesteuerte stand- und schwungphasenkontrollierte Ganzbeinorthesen (SSCO): Entwicklung, Systeme und Versorgungsrealität in der orthopädietechnischen Praxis — 9. April 2026
- Gips oder Orthese bei distalen Radiusfrakturen? — 8. April 2026
- Morgan SJ, Friedly JL, Amtmann D, Salem R, Hafner BJ. Cross-Sectional Assessment of Factors Related to Pain Intensity and Pain Interference in Lower Limb Prosthesis Users. Archives of Physical Medicine and Rehabilitation, 2017; 98 (1): 105–113. Epub 2016/10/16. https://doi.org/10.1016/j.apmr.2016.09.118. PMID: 27742450
- Ephraim PL, Wegener ST, MacKenzie EJ, Dillingham TR, Pezzin LE. Phantom pain, residual limb pain, and back pain in amputees: results of a national survey. Archives of Physical Medicine and Rehabilitation, 2005; 86 (10): 1910–1919. Epub 2005/10/11. https://doi.org/10.1016/j.apmr.2005.03.031.PMID: 16213230
- Hsu E, Cohen SP. Postamputation pain: epidemiology, mechanisms, and treatment. Journal of Pain Research, 2013; 6: 121–136. Epub 2013/02/22. https://doi.org/10.2147/JPR. S32299. PMID: 23426608
- Pereira MG, Ramos C, Lobarinhas A, Machado JC, Pedras S. Satisfaction with life in individuals with a lower limb amputation: The importance of active coping and acceptance. Scandinavian Journal of Psychology, 2018; 59 (4): 414–421. Epub 2018/04/24. https://doi.org/10.1111/sjop.12444. PMID: 29682756
- Jackson MA, Simpson KH. Pain after amputation. Continuing Education in Anaesthesia Critical Care & Pain, 2004; 4 (1):20–23. https://doi.org/10.1093/bjaceaccp/mkh007
- Dwornik G, Weiss T, Hofmann GO, Bruckner L. [Residual limb and phantom pain : Causes and therapeutic approaches]. Der Orthopäde, 2015; 44 (6): 435–444. Epub 2015/05/31. https://doi.org/10.1007/ s00132-015‑3122‑z. PMID: 26024778
- Uustal H, Meier RH 3rd. Pain issues and treatment of the person with an amputation. Physical Medicine and Rehabilitation Clinics of North America, 2014; 25 (1): 45–52. Epub 2013/11/30. https://doi.org/10. 1016/j.pmr.2013.09.008. PMID: 24287239
- Pereira MG, Ramos C, Lobarinhas A, Machado JC, Pedras S. Satisfaction with life in individuals with a lower limb amputation: The importance of active coping and acceptance. Scandinavian Journal of Psychology, 2018; 59 (4): 414–421. Epub 2018/04/24. https://doi.org/10.1111/sjop.12444. PMID: 29682756
- Dwornik G, Weiss T, Hofmann GO, Bruckner L. [Residual limb and phantom pain : Causes and therapeutic approaches]. Der Orthopäde, 2015; 44 (6): 435–444. Epub 2015/05/31. https://doi.org/10.1007/ s00132-015‑3122‑z. PMID: 26024778
- Dwornik G, Weiss T, Hofmann GO, Bruckner L. [Residual limb and phantom pain : Causes and therapeutic approaches]. Der Orthopäde, 2015; 44 (6): 435–444. Epub 2015/05/31. https://doi.org/10.1007/ s00132-015‑3122‑z. PMID: 26024778
- Dwornik G, Weiss T, Hofmann GO, Bruckner L. [Residual limb and phantom pain : Causes and therapeutic approaches]. Der Orthopäde, 2015; 44 (6): 435–444. Epub 2015/05/31. https://doi.org/10.1007/ s00132-015‑3122‑z. PMID: 26024778
- Murray AL, Morgenroth DC, Czerniecki JM. Residual limb claudication in a traumatic transtibial amputee. PM & R, 2013; 5 (2): 152–154. Epub 2013/02/19. https://doi.org/10.1016/j.pmrj.2012.08.003. PMID: 23415251
- de Boer RG, Paping MA, Kap B, Geertzen JH. Residual limb claudication after vascular transfemoral amputation. Prosthetics and Orthotics International, 2017; 41 (6): 601–604. Epub 2017/05/05. https://doi. org/10.1177/0309364617706747. PMID: 28470108
- Cochrane H, Orsi K, Reilly P. Lower limb amputation. Part 3: Prosthetics – a 10 year literature review. Prosthetics and Orthotics International, 2001; 25 (1): 21–28. Epub 2001/06/20. https://doi.org/10.1080/ 03093640108726564.PMID: 11411001
- Baars EC, Geertzen JH. Literature review of the possible advantages of silicon liner socket use in transtibial prostheses. Prosthetics and Orthotics International, 2005; 29 (1): 27–37. https://doi.org/10.1080/ 17461550500069612. PMID: 16180375
- Kristinsson O. The ICEROSS concept: a discussion of a philosophy. Prosthetics and Orthotics International, 1993; 17 (1): 49–55. Epub 1993/04/01. https://doi.org/10.3109/03093649309164354.PMID: 8337100
- Fergason J, Smith DG. Socket considerations for the patient with a transtibial amputation. Clin Orthop Relat Res, 1999; (361): 76–84. Epub 1999/04/23. https://doi.org/10.1097/00003086–199904000-00011. PMID: 10212599
- Baars EC, Geertzen JH. Literature review of the possible advantages of silicon liner socket use in transtibial prostheses. Prosthetics and Orthotics International, 2005; 29 (1): 27–37. https://doi.org/10.1080/ 17461550500069612. PMID: 16180375
- Kristinsson O. The ICEROSS concept: a discussion of a philosophy. Prosthetics and Orthotics International, 1993; 17 (1): 49–55. Epub 1993/04/01. https://doi.org/10.3109/03093649309164354. PMID: 8337100
- Ueno H, Fukumoto S, Koyama H, Tanaka S, Maeno T, Murayama M, et al. Regions of arterial stenosis and clinical factors determining transcutaneous oxygen tension in patients with peripheral arterial disease. J Atheroscler Thromb, 2010; 17 (8): 858–869. Epub 2010/03/31. https://doi.org/10.5551/jat.3723.PMID: 20351469
- Wimberley PD, Gronlund Pedersen K, Olsson J, Siggaard-Andersen O. Transcutaneous carbon dioxide and oxygen tension measured at different temperatures in healthy adults. Clin Chem, 1985; 31 (10): 1611–1615. Epub 1985/10/01.PMID: 3930089
- Andriessen A, Polignano R, Abel M. Monitoring the microcirculation to evaluate dressing performance in patients with venous leg ulcers. Journal of Wound Care, 2009; 18 (4): 145–150. Epub 2009/04/08. https://doi.org/10.12968/jowc.2009.18.4.41606. PMID: 19349934
- Moosa HH, Makaroun MS, Peitzman AB, Steed DL, Webster MW. TcPO2 values in limb ischemia: effects of blood_ow and arterial oxygen tension. The Journal of Surgical Research, 1986; 40 (5): 482–487.Epub 1986/05/01. https://doi.org/10.1016/0022–4804(86)90219–2. PMID: 3736032
- Poredos P, Rakovec S, Guzic-Salobir B. Determination of amputation level in ischaemic limbs using tcPO2 measurement.VASA Zeitschrift für Gefäßkrankheiten, 2005; 34 (2): 108–112. Epub 2005/06/23. https://doi.org/10.1024/0301–1526.34.2.108. PMID: 15968892
- Rooth G, Hedstrand U, Tyden H, Ogren C. The validity of the transcutaneous oxygen tension method in adults. Critical Care Medicine, 1976; 4 (3): 162–165. Epub 1976/05/01. https://doi.org/10.1097/00003246 197605000–00009. PMID: 939109
- Ruangsetakit C, Chinsakchai K, Mahawongkajit P, Wongwanit C, Mutirangura P. Transcutaneous oxygen tension: a useful predictor of ulcer healing in critical limb ischaemia. Journal of Wound Care, 2010; 19 (5): 202–206. https://doi.org/10.12968/jowc.2010.19.5.48048. PMID: 20505593
- Columbo JA, Nolan BW, Stucke RS, Rzucidlo EM, Walker KL, Powell RJ, et al. Below-Knee Amputation Failure and Poor Functional Outcomes Are Higher Than Predicted in Contemporary Practice. Vasc Endovascular Surg, 2016; 50 (8): 554–558. https://doi.org/10.1177/1538574416682159. PMID:27909207
- Nishio H, Minakata K, Kawaguchi A, Kumagai M, Ikeda T, Shimizu A, et al. Transcutaneous oxygen pressure as a surrogate index of lower limb amputation. International Angiology, 2016; 35 (6): 565–572. Epub 2016/10/22. PMID: 26871392
- Wang Z, Hasan R, Firwana B, Elraiyah T, Tsapas A, Prokop L, et al. A systematic review and metaanalysis of tests to predict wound healing in diabetic foot. J Vasc Surg, 2016; 63 (2 Suppl): 29S–36S e1–2. https://doi.org/10.1016/j.jvs.2015.10.004. PMID: 26804365
- Huang K, Ma Y, Wang J, Shi S, Fu L, Liu J, et al. The correlation between transcutaneous oxygen tension and microvascular complications in type 2 diabetic patients. J Diabetes Complications, 2017; 31 (5): 886–890. https://doi.org/10.1016/j.jdiacomp.2017.02.006. PMID:28242269
- Arsenault KA, Al-Otaibi A, Devereaux PJ, Thorlund K, Tittley JG, Whitlock RP. The use of anscutaneous oximetry to predict healing complications of lower limb amputations: a systematic review and metaanalysis. Eur J Vasc Endovasc Surg, 2012; 43 (3): 329–336. https://doi.org/10.1016/j.ejvs.2011.12.004. PMID: 22240334
- Ruangsetakit C, Chinsakchai K, Mahawongkajit P, Wongwanit C, Mutirangura P. Transcutaneous oxygen tension: a useful predictor of ulcer healing in critical limb ischaemia. Journal of Wound Care, 2010; 19 (5): 202–206. https://doi.org/10.12968/jowc.2010.19.5.48048. PMID: 20505593
- Rink CL, Wernke MM, Powell HM, Tornero M, Gnyawali SC, Schroeder RM, et al. Standardized Approach to Quantitatively Measure Residual Limb Skin Health in Individuals with Lower Limb Amputation. Adv Wound Care (New Rochelle), 2017; 6 (7): 225–232. Epub 2017/07/25. https://doi.org/10.1089/ wound.2017.0737. PMID: 28736682
- ISPO 17th World Congress Abstract Book. Prosthetics and Orthotics International, 2019; 43 (1_suppl): 1–600. https://doi.org/10.1177/0309364619883197
- Burgess EM, Zettl JH. Amputations below the knee. Arti_cial Limbs, 1969; 13 (1): 1–12. Epub 1969/01/01. PMID: 5363259
- Gailey RS, Roach KE, Applegate EB, Cho B, Cunniffe B, Licht S, et al. The amputee mobility predictor: an instrument to assess determinants of the lower-limb amputee’s ability to ambulate. Archives of Physical Medicine and Rehabilitation, 2002; 83 (5): 613–627. Epub 2002/05/08. https://doi.org/10.1053/ampr. 2002.32309. PMID: 11994800
- Legro MW, Reiber GD, Smith DG, del Aguila M, Larsen J, Boone D. Prosthesis evaluation questionnaire for persons with lower limb amputations: assessing prosthesis-related quality of life. Archives of Physical Medicine and Rehabilitation, 1998; 79 (8): 931–938. Epub 1998/08/26. https://doi. org/10.1016/s0003 9993(98)90090–9. PMID: 9710165
- Grouiller F, Jaquinandi V, Picquet J, Souday V, Saumet JL, Abraham P. Validation of a new device for transcutaneous oxygen pressure recordings in real and simulated exercise tests. International Angiology, 2006; 25 (2): 190–196. Epub 2006/06/10. PMID: 16763538
- Severinghaus JW, Astrup P, Murray JF. Blood gas analysis and critical care medicine. Am J Respir Crit Care Med, 1998; 157 (4 Pt 2): S114–122. Epub 1998/05/01. https://doi.org/10.1164/ajrccm.157.4.nhlb1‑9. PMID: 9563770
- Schef_er A, Rieger H. A comparative analysis of transcutaneous oximetry (tcPO2) during oxygen inhalation and leg dependency in severe peripheral arterial occlusive disease. J Vasc Surg, 1992; 16 (2): 218–224. Epub 1992/08/01. PMID: 1495145
- Schef_er A, Eggert S, Rieger H. In_uence of clinical _ndings, positional manoeuvres, and systolic ankle arterial pressure on transcutaneous oxygen tension in peripheral arterial occlusive disease. Eur J Clin Invest, 1992; 22 (6): 420–426. Epub 1992/06/01. https://doi.org/10.1111/j.1365–2362.1992.tb01484.x. PMID: 1633837
- Hopman WM, Towheed T, Anastassiades T, Tenenhouse A, Poliquin S, Berger C, et al. Canadian normative data for the SF-36 health survey. Canadian Medical Association Journal, 2000; 163 (3): 265–271. PMID: 10951722
- Murray AL, Morgenroth DC, Czerniecki JM. Residual limb claudication in a traumatic transtibial amputee. PM & R, 2013; 5 (2): 152–154. Epub 2013/02/19. https://doi.org/10.1016/j.pmrj.2012.08.003. PMID: 23415251
- de Boer RG, Paping MA, Kap B, Geertzen JH. Residual limb claudication after vascular transfemoral amputation. Prosthetics and Orthotics International, 2017; 41 (6): 601–604. Epub 2017/05/05. https://doi. org/10.1177/0309364617706747.PMID: 28470108
- Rink CL, Wernke MM, Powell HM, Tornero M, Gnyawali SC, Schroeder RM, et al. Standardized Approach to Quantitatively Measure Residual Limb Skin Health in Individuals with Lower Limb Amputation. Adv Wound Care (New Rochelle), 2017; 6 (7): 225–232. Epub 2017/07/25. https://doi.org/10.1089/ wound.2017.0737. PMID: 28736682
- Rink CL, Wernke MM, Powell HM, Tornero M, Gnyawali SC, Schroeder RM, et al. Standardized Approach to Quantitatively Measure Residual Limb Skin Health in Individuals with Lower Limb Amputation. Adv Wound Care (New Rochelle), 2017; 6 (7): 225–232. Epub 2017/07/25. https://doi.org/10.1089/ wound.2017.0737. PMID: 28736682
- Taylor GI, Palmer JH. The vascular territories (angiosomes) of the body: experimental study and clinical applications. British Journal of Plastic Surgery, 1987; 40 (2): 113–141. Epub 1987/03/01. https://doi.org/10. 1016/0007–1226(87)90185–8. PMID: 3567445
- Landsman AS, Barnhart D, Sowa M. Near-Infrared Spectroscopy Imaging for Assessing Skin and Wound Oxygen Perfusion. Clin Podiatr Med Surg, 2018; 35 (3): 343–355. Epub 2018/06/05. https://doi. org/10.1016/j.cpm.2018.02.005.PMID: 29861017
- Peery JT, Ledoux WR, Klute GK. Residual-limb skin temperature in transtibial sockets. Journal of Rehabilitation Research and Development, 2005; 42 (2): 147–154. Epub 2005/06/10. https://doi.org/10.1682/ jrrd.2004.01.0013. PMID: 15944879
- Peery JT, Ledoux WR, Klute GK. Residual-limb skin temperature in transtibial sockets. Journal of Rehabilitation Research and Development, 2005; 42 (2): 147–154. Epub 2005/06/10. https://doi.org/10.1682/ jrrd.2004.01.0013. PMID: 15944879
- Peery JT, Klute GK, Blevins JJ, Ledoux WR. A threedimensional finite element model of the transibial residual limb and prosthetic socket to predict skin temperatures. IEEE Transactions on Neural Systems and Rehabilitation Engineering, 2006; 14 (3): 336–343. Epub 2006/10/03. https://doi.org/10.1109/tnsre.2006.881532. PMID: 17009493
- Sanders JE. Thermal response of skin to cyclic pressure and pressure with shear: a technical note. Journal of Rehabilitation Research and Development, 2000; 37 (5): 511–515. Epub 2001/04/27. PMID: 11322149
- Manorama AA, Baek S, Vorro J, Sikorskii A, Bush TR. Blood perfusion and transcutaneous oxygen level characterizations in human skin with changes in normal and shear loads – implications for pressure ulcer formation. Clin Biomech (Bristol, Avon), 2010; 25 (8): 823–828. Epub 2010/07/29. https://doi.org/ 10.1016/j.clinbiomech.2010.06.003. PMID: 20663594
- Kobayashi T, Orendurff MS, Arabian AK, Rosenbaum-Chou TG, Boone DA. Effect of prosthetic alignment changes on socket reaction moment impulse during walking in transtibial amputees. J Biomech, 2014; 47 (6): 1315–1323. Epub 2014/03/13. https://doi.org/10.1016/j.jbiomech.2014.02.012.PMID: 24612718
- Fouasson-Chailloux A, Abraham P, Colas-Ribas C, Feuilloy M, Vielle B, Henni S. Simultaneous pain intensity rating and quanti_cation of ischemia throughout exercise and recovery in proximal versus distal arterial claudication. Vasc Med, 2017; 22 (6): 490–497. Epub 2017/10/08. https://doi.org/10.1177/ 1358863X17734304. PMID: 28985707
- Schorr EN, Treat-Jacobson D, Lindquist R. The Relationship Between Peripheral Artery Disease Symptomatology and Ischemia. Nurs Res, 2017; 66 (5): 378–387. Epub 2017/09/01. https://doi.org/10.1097/NNR.0000000000000230. PMID:28858146
- Schorr EN, Treat-Jacobson D, Lindquist R. The Relationship Between Peripheral Artery Disease Symptomatology and Ischemia. Nurs Res, 2017; 66 (5): 378–387. Epub 2017/09/01. https://doi.org/10.1097/NNR.0000000000000230. PMID:28858146
- Tantua A, Geertzen J, Dungen J, Breek J, Dijkstra P. Reduction of residual limb volume in people with transtibial amputation. Journal of Rehabilitation Research and Development, 2014; 51: 1119–1126. https://doi.org/10.1682/JRRD.2013.11.0243. PMID: 25437771
- Mahe G, Kalra M, Abraham P, Liedl DA, Wennberg PW. Application of exercise transcutaneous oxygen pressure measurements for detection of proximal lower extremity arterial disease: a case report. Vasc Med, 2015; 20 (3): 251–255. https://doi.org/10.1177/1358863X14567030. PMID: 25750011
- Henni S, Sempore YW, Le Meliner T, Ouedraogo N, Hamel JF, Abraham P. Intra-test and test-retest reliability of exercise oximetry in arterial claudication. Microvascular Research, 2018; 117: 44–49. Epub 2018/01/13. https://doi.org/10.1016/j.mvr.2018.01.003. PMID: 29325705
- Abraham P, Colas-Ribas C, Signolet I, Ammi M, Feuilloy M, Picquet J, et al. Transcutaneous Exercise Oximetry for Patients With Claudication – A Retrospective Review of Approximately 5,000 Consecutive Tests Over 15 Years. Circulation Journal, 2018; 82 (4): 1161–1167. Epub 2018/01/19. https://doi.org/10.1253/circj.CJ-17–0948. PMID: 29343673
- Holdich TA, Reddy PJ, Walker RT, Dormandy JA. Transcutaneous oxygen tension during exercise in patients with claudication. British Medical Journal (Clinical Research Ed), 1986; 292 (6536): 1625–1628. Epub 1986/06/21. https://doi.org/10.1136/bmj.292.6536.1625. PMID: 3087549
- Lenz AL, Bush TR. Evaluating shear and normal force with the use of an instrumented transtibial socket: A case study. Med Eng Phys, 2019; 71: 102–107. Epub 2019/07/25. https://doi.org/10.1016/j.medengphy. 2019.07.002. PMID: 31331756
- Klute GK, Glaister BC, Berge JS. Prosthetic liners for lower limb amputees: a review of the literature. Prosthetics and Orthotics International, 2010; 34 (2): 146–153. Epub 2010/04/14. https://doi.org/10.3109/ 03093641003645528. PMID: 20384553


![Gründe für Stumpfschmerzen und entsprechende Therapiemöglichkeiten, adaptiert von Dwornik et al. (Dwornik G, Weiss T, Hofmann GO, Bruckner L. [Residual limb and phantom pain : Causes and therapeutic approaches]. Der Orthopäde, 2015; 44 (6): 435–444. Epub 2015/05/31. https://doi.org/10.1007/ s00132-015-3122-z. PMID: 26024778).](https://360-ot.de/wp-content/uploads/2021/07/tab-1-800x445.jpg)