Einleitung
Kinder und Erwachsene mit chronischen Erkrankungen der Gehirnfunktion, wie beispielsweise nach Hirnentwicklungsstörungen, nach ischämischem oder hämorrhagischem Insult, nach Schädel-Hirn-Trauma oder Enzephalitis oder bei Multipler Sklerose, leben mit je nach Lokalisation und Ausdehnung der Schädigung unterschiedlich schweren Beeinträchtigungen ihrer Alltagsaktivitäten. Greif‑, Sprach‑, Seh‑, Hör‑, Sitz- Steh‑, Gehfunktion und kognitive, emotionale sowie psychosoziale Fähigkeiten können betroffen sein.
Körperhaltung, Stehen und Gehen sind komplexe sensomotorische Leistungen. Bei Einschränkungen der Leistungsfähigkeit des Zentralnervensystems sind Auffälligkeiten der Haltung, der Sprache, der Greiffähigkeit und des Gangbildes zu beobachten. Dieser motorischen Symptomatik liegen jedoch Störungen der motorischen UND sensorischen Funktionen zugrunde, wobei die Aufmerksamkeit besonders auf Letztere gelenkt werden soll.
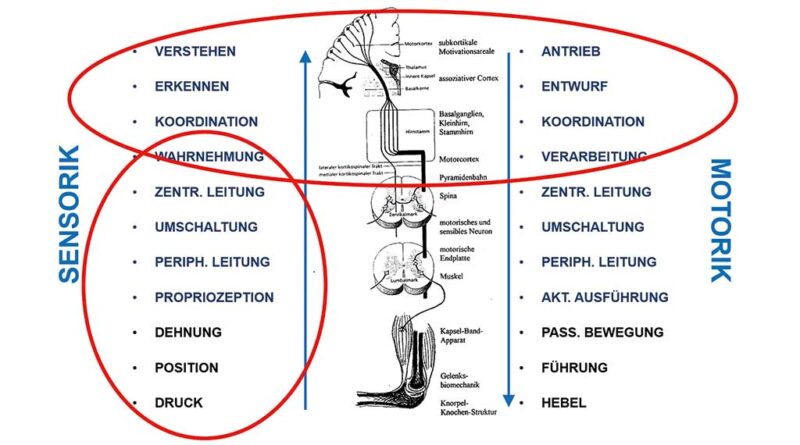
Beim gesunden Menschen werden exterozeptive Reize der Umwelt über Druck- und Temperatur-Rezeptoren bzw. ‑Sensoren in der Haut und dem Unterhautfettgewebe und den Dehnungsrezeptoren in Bindegewebe, Faszien und Muskeln aufgenommen und weitergeleitet. Sie werden mit propriozeptiven Reizen der Körperstellung über Positionsrezeptoren in Gleichgewichtsorganen, Faszien, Muskeln und Gelenkkapseln verknüpft und anhand von Assoziationen und Erfahrungen zur Wahrnehmung verarbeitet. Nun erkennen wir – in erster Linie unbewusst – die Ausgangsposition unseres Körpers. Dies ist die Voraussetzung dafür, dass die tonische Haltemuskulatur die Kopf‑, Rumpf- und Beinachsenstabilität unter den Bedingungen der Schwerkraft kontrolliert und durch die phasische Antriebsmuskulatur Bewegungen geplant und gesteuert werden können.
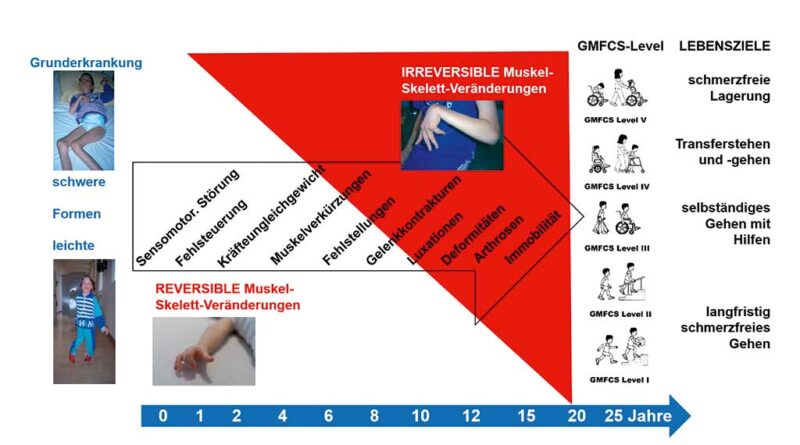
Bei Menschen mit zerebralen Bewegungsstörungen sind die Verarbeitung und Koordination dieser Informationen aus der Peripherie beeinträchtigt, die Informationen der Sensoren werden nicht oder falsch verarbeitet und können der Planung und Kontrolle der Motorik nicht ausreichend zur Verfügung stehen (Abb. 1). Die mangelnde Haltungs- und Bewegungskontrolle führt zu einer zusätzlichen sekundären Verschlechterung der Sensomotorik. Einerseits durch „Non-use“ (Nicht-Gebrauch) und andererseits durch Fehlstellungen von Körperabschnitten, die nicht als falsche Position wahrgenommen werden können, nehmen Muskel-Skelett-Veränderungen ihren Ausgang. Diese sind zunächst reversibel, jedoch fortschreitend schmerzhaft und entwickeln sich je nach Schweregrad zu irreversiblen Deformitäten der Stütz- und Bewegungsorgane (Abb. 2).
In den vergangenen Jahren konnten im Rahmen von dreidimensionalen Bewegungsanalysestudien autoregulative Mechanismen der Skelettmuskulatur entdeckt werden, die bei zerebralen Bewegungsstörungen versuchen, den Körper unter den Bedingungen der Schwerkraft durch eine Muskelüberaktivität zu stabilisieren. Die Schwäche der tonischen Haltemuskulatur scheint durch eine – als „Spastik“ zu beobachtende – Überaktivität der phasischen Bewegungsmuskulatur der Extremitäten kompensiert zu werden1.
Andererseits führen bei weniger aktiven, nicht gehfähigen Patienten die Inaktivität der Skelettmuskulatur, die fehlende Muskelmasse und der Mangel an Training zu einem Mangel an entzündungshemmenden Substanzen. Die somit bei Reizung nozizeptiver Nervenfasern ungehemmt erzeugte Neuroinflammation schaltet den Schmerzverstärker ein und schwächt die körpereigene Schmerzabwehr2. Dies wird mit als Ursache für die Entwicklung unterschätzter chronischer Schmerzen bei Menschen auch mit schweren zerebralen Bewegungsstörungen vermutet.
Bei Kindern muss zusätzlich die Dimension der Reifung und Entwicklung berücksichtigt werden. Das erstmalige Erreichen des Stehens und Gehens ist ein Meilenstein der kindlichen Entwicklung und hängt unmittelbar mit der Entwicklung der Psyche und des Selbstbewusstseins zusammen.
Schwere neuromotorische Störungen führen zu mangelnder Reifung der Sensomotorik und bei Ausbleiben eines ausreichenden Trainings in weiterer Folge zu Störungen der Bewegungsorgane und anderer Organfunktionen. Studien zeigen, dass alle Kinder mit Zerebralparesen, unabhängig vom Alter, mit muskuloskelettalen Schmerzen leben, die umso stärker sind, je weniger mobil die Kinder sind3 4.
Ziel der vorliegenden Arbeit ist es, die praktischen Erfahrungen mit verschiedenen afferenz-stimulierenden „Senso-Orthesen“ bei Kindern und Erwachsenen mit zerebralen Bewegungsstörungen mit der bisher publizierten Literatur abzugleichen und dem Behandlungsteam einen Überblick über den derzeitigen Wissenstand zur Verfügung zu stellen. Suchkriterien für die systematische Literaturrecherche zur Wirkungsweise, zu klinischen Erfahrungen, Indikationen und Outcome der verschiedenen Orthesentypen in der Datenbank Pubmed waren die Begriffe cerebral disorders, stroke, cerebral palsy AND sensory orthoses, sensory input orthoses, pressure input orthoses, electrostimulation orthoses, compression suits, electrostimulation suits.
Entwicklung von Senso-Orthesen zur Verbesserung der Haltungs- und Bewegungskontrolle
Ziel jeder Hilfsmittelversorgung bei Menschen mit zerebralen Bewegungsstörungen und neuromuskulären Erkrankungen ist der Ausgleich der sensomotorischen Fehlfunktion, um physiologische Aktivität zu ermöglichen und Schmerzen sowie Sekundärschäden des Körpers zu vermeiden. Es ist daher naheliegend, bei der Entwicklung von wirksamen Orthesen die sensorischen Restfunktionen bestmöglich zu nutzen, die funktionstüchtigen peripheren extero- und propriozeptiven Rezeptoren zu stimulieren und somit die unbewusste Wahrnehmung durch Mechanismen der Neuroplastizität zu trainieren, um die Voraussetzungen für eine adäquate Reaktion des motorischen Systems, der tonischen Halte- und phasischen Bewegungsaktivität zu schaffen.
Senso-Orthesen wären somit in der Lage, einerseits den „Non-use“ der neuronalen Afferenzen und andererseits – durch ihre zusätzlichen mechanisch-stabilisierenden Eigenschaften – die Entwicklung von Fehlstellungen von Körperabschnitten, Schmerzen und Muskel-Skelett-Veränderungen positiv zu beeinflussen.
Die Ziele der Senso-Orthetik können wie folgt zusammengefasst werden:
- Schmerzfreiheit
- Verbesserung der Kraft der tonischen „Anti-Schwerkraft-Muskulatur“ mit Kräftigung der Kopf‑, Rumpf- und Haltungskontrolle und erleichterter Aktivierung der oberen Extremitäten
- Verbesserung der Sensorik und der Perzeption mit Beeinflussung des Muskeltonus und Hemmung spastischer Muskelüberaktivität
- Verbesserung der Sprachmotorik und damit der Kommunikation und Nahrungsaufnahme
- Vergrößern des Bewegungsausmaßes der Muskeln und Gelenke mit Vorbeugen von Sekundärschäden durch Erhalt der Dehnfähigkeit der Muskeln und damit Vermeidung von Kontrakturen und konsekutiven knöchernen Deformitäten sowie Vermeidung häufig unterschätzter muskuloskelettaler Schmerzen
- Normalisierung der Hebelarme, um Krafttraining der Muskulatur zu ermöglichen
- Beeinflussung des Knorpelwachstums und der Gelenksentwicklung
- Belastung der unteren Extremitäten und Wirbelsäule zur Vermeidung einer Inaktivitätsosteoporose
- im Wachstumsalter Stimulation der Wachstumsfugen
- durch Verbesserung der Muskelkraft und Mobilität bessere kardiopulmonale Leistungsfähigkeit und bessere Funktion innerer Organe und des Stoffwechsels
- durch Vertikalisierung Normalisierung des Serotonin-Stoffwechsels und Verbesserung der zerebralen Leistungsfähigkeit
- Reduktion psychologischer Probleme durch Steigerung des Selbstbewusstseins
- Erreichen von sozialer Teilhabe
Die derzeit entwickelten und Kindern und Erwachsenen mit zerebralen Bewegungsstörungen klinisch zur Verfügung stehenden Senso-Orthesen bzw. sensorisch wirksamen Hilfsmittel können in fünf Gruppen mit unterschiedlichem Ansatz ihrer Wirkungsweise unterteilt werden:
- Wärme
- Kompression (und Vertikalisierung)
- Lokomotion5
- Vibration
- Elektrostimulation
Hilfsmittel nutzen durch diese spezifischen physikalischen Mechanismen und die damit verbundene exterozeptive und propriozeptive Stimulation zentrale sensorische Restfunktionen, trainieren die unbewusste Wahrnehmung durch Mechanismen der Neuroplastizität und schaffen damit die Voraussetzungen für eine physiologische Motorik. Somit können diese auf fünf unterschiedlichen Wegen einerseits den „Non-use“ der neuronalen Afferenzen und andererseits die Entwicklung von Fehlstellungen, Schmerzen und Muskel-Skelett-Veränderungen vermeiden helfen.
Wie wirken Senso-Orthesen durch Kompression?
Anders als bei der Kompressionstherapie zur Verbesserung der Fließeigenschaften der Blut- und Lymphgefäße wirkt der Druck nicht auf das Bindegewebe, um den Tonus der Gefäßwände zu erhöhen, sondern auf die neuralen Mechanorezeptoren, die als primäre Druck- und Dehnungs-Sensoren für die Extero- und Propriozeption verantwortlich sind. Proprio- und exterozeptiver Input ermöglichen ein Training des afferenten Systems mit Verbesserung der Tiefenwahrnehmung und damit eine Aktivierung und Kräftigung der tonischen Haltemuskulatur.
Aus zahlreichen Studien der Raumforschung ist bekannt, dass propriozeptive und taktile Reize bei fehlender Schwerkraft über längere Zeiträume wiederkehrend appliziert werden müssen, um die Haltungskontrolle aufrechtzuerhalten und den Astronauten bzw. Kosmonauten nach der Rückkehr auf die Erde eine raschere Adaptation an die Schwerkraft zu erlauben6. Dieses Grundprinzip der dauerhaften sensorischen Reizapplikation greift die komplexe Methode der „Propriozeptiven Korrektur“ auf und ermöglicht im Rahmen der Neurorehabilitation die Behandlung von Menschen mit schweren Hirnschädigungen und Bewegungsstörungen7.
Entwicklung von Kompressionsorthesen bei zerebralen Bewegungsstörungen
Erstmals wurde ein beweglicher Korrekturanzug aus der Raumfahrt für die Behandlung von Kindern mit zerebralen Bewegungsstörungen in den 1990er Jahren von Kozijavkin an der Internationalen Rehabilitationsklinik Truskawez in der Ukraine eingesetzt. Eigene Beobachtungen vor Ort und ein im Lancet publizierter Erfahrungsbericht konnten eine Verbesserung der Haltung und Bewegung und eine Reduktion der Spastik im Rahmen der multimodalen Intensiv-Rehabilitation feststellen8. Eine ähnlich aufgebaute Kompressionsorthese führt zu einer Verbesserung des Gangbildes im Rahmen der multimodalen Intensiv-Rehabilitation nach Adeli9.
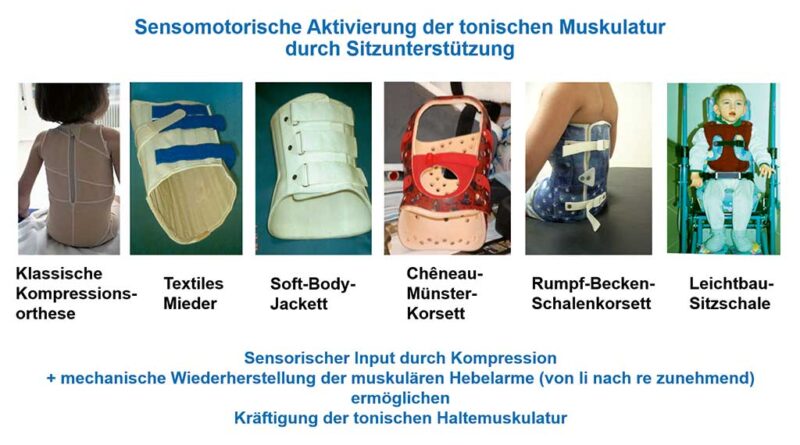
Weiterentwickelt wurden die Korrekturanzüge als elastische, hauteng anliegende Ganzkörper-Kompressionsorthesen für den Rumpf bzw. einzelne Körperteile, wie den Beckengürtel10. Eine Studie zur Rumpforthese „Spio“ („Stabilizing Pressure Input Orthosis“) zeigte in Kombination mit einer multimodalen ambulanten oder stationären Behandlung Verbesserungen von kyphotischen Fehlhaltungen, aber nicht von Skoliosen und Hüftluxationen11. Ähnlich aufgebaut sind die am Markt erhältlichen Kompressionsorthesen, wie beispielsweise die „Dynamic GPS Soft-Orthese“, „Flexa Barbieri SLR-Orthese“ und „Protheseus TLSO Weste“ (Abb. 3).
Qualitätskriterien erleichtern die Beurteilung der Wirksamkeit und des Stellenwerts im Gesamtbehandlungskonzept: Kompressionsrumpforthesen sollen in Verbindung mit konventioneller Therapie und Alltagsaktivitäten eine subjektiv und objektiv messbare verbesserte Rumpfstabilität und Handfunktion ermöglichen. In der Praxis ist sehr oft eine orthopädietechnische Nachbesserung durch zusätzliche elastische Zügel und partielle Versteifungen notwendig.
Evidenz gibt es für die Verbesserung der aktiven Sitzfunktion, Verbesserung der Handmotorik und Kopfkontrolle durch Stabilisierung des Rumpfes. Voraussetzung sind fehlende höhergradige Atmungs- oder Hautprobleme12 13. Die Indikation ist bei flexibler Wirbelsäuleninstabilität ohne strukturelle Deformitäten, wie Kyphose oder Skoliose, mit für die aktive Aufrichtung ausreichend kräftiger Rumpfmuskel-Restfunktion gegeben. Kontraindiziert sind eine ausgeprägte Rumpfmuskelschwäche und strukturelle Fehlstellungen. In einem systematischen Review aus 2021 wurden 12 Studien zu dynamischen Kompressionsorthesen (wie Therasuit, Theratog, Adeli und andere) inkludiert. Bei Kindern mit Zerebralparesen konnten signifikante Veränderungen der Ganggeschwindigkeit, Kadenz, Schrittlänge und Symmetrie in Verbindung mit Trainingsprogrammen festgestellt werden, sodass die Autoren 18–60 Sitzungen empfehlen, um optimale Resultate zu erzielen14.
Das Grundprinzip der „Dynamischen Stabilität“ bei der neuro-orthetischen Versorgung wurde bereits in den 1960–1970er Jahren von Adriano Ferrari, Neuro-Rehabilitationsmediziner und Schüler von Milani Comparetti, beschrieben, der feststellte, dass die beste Orthese durch Beweglichkeit aller Gelenke sensomotorisches Lernen durch neuronale Plastizität ermöglicht15.
Auch die dynamische Orthesenversorgung nutzt daher diese beschriebenen Mechanismen. Kompression entsteht durch die halbelastische, eng anliegende Bauweise und Belastung der Mechanorezeptoren im Rahmen der Vertikalisierung. Durch weitgehend freigegebene Gelenke können tonische wie phasische Muskeln durch die Sicherung physiologischer Ursprungs- und Ansatzpunkte sowie Hebelarme trotz zentraler Paresen maximal aktiviert und gekräftigt werden.
Dynamische Rumpforthesen (semirigide bis rigide Rumpfstützorthese, Kunststoff-Stützmieder, Chêneau-Münster-Korsett) sind stabiler als rein textil hergestellte Kompressionsorthesen, nutzen jedoch aufgrund ihrer dynamischen Stabilität neben ihrer mechanischen Stützfunktion ebenso das Behandlungsprinzip der extero- und propriozeptiven Stimulation der Mechanorezeptoren (Abb. 4). In der Literatur findet sich eine Evidenz für das Erreichen einer Sitzfunktion, eine Verbesserung der Handmotorik und Kopfkontrolle durch dynamische Stabilisierung des Rumpfes. Voraussetzung sind fehlende höhergradige Atmungs- oder Hautprobleme. Indikationen sind eine flexible oder strukturelle neuromuskuläre Wirbelsäulen-Instabilität, Kontraindikation ist die idiopathische Skoliose16 17 18.
Die einfachste Form einer durch Kompression afferenzstimulierenden Orthese ist die dynamische Einlage (sensomotorische, propriozeptive oder funktionelle Korrektureinlage), von der derzeit etwa 200 verschiedene Typen im Handel erhältlich sind (MBI, Derks, Podologische Einlagen, Spiraldynamische Einlagen, Jahrling, Pomarino etc.). Für Studien sollte die unterschiedliche Bauweise und Notwendigkeit einer Differenzierung beachtet werden19.
Die derzeitige Studienlage bestätigt eine Evidenz für die qualitative Verbesserung der Steh- und Gehfunktion und Muskeltonus-Regulation durch eine Aktivierung einzelner Muskeln durch propriozeptiv wirksame Reize an der Fußsohle. Signifikante quantitative Veränderungen gegenüber eines Kontrollkollektivs konnten in 3D-Ganganalyse-Studien bisher nicht gefunden werden. Voraussetzung ist eine ausreichende Funktion der Afferenzen ohne schwere strukturelle Fehlstellung. Indiziert sind dynamische Einlagen bei flexiblen Spitz‑, Platt‑, Hohl‑, Klumpfüßen, kontraindiziert bei fehlender Oberflächensensibilität oder schweren kontrakten Fußfehlstellungen20 21.
Für gehfähige Patienten mit zerebraler Bewegungsstörung wurden alternativ zur orthopädischen Schuhversorgung, entsprechend dem Prinzip der „Dynamischen Stabilität“, dynamische, das untere Sprunggelenk stabilisierende kurze Gehorthesen als Knöchel-Fuß-Orthesen (DAFO) mit flexibler ringförmiger Fassung entwickelt. Ihnen liegt der gleiche Wirkmechanismus wie bei der dynamischen Einlage in Kombination mit einer mechanischen Stabilisierung des unteren Sprunggelenkes zugrunde. Indikationen sind instabile, aber noch flexible Spitz‑, Platt‑, Hohl- und Klumpfüße, bei schweren flexiblen und strukturell fixierten Füßen oder Kontrakturen sind diese jedoch kontraindiziert22 23 (Abb. 5). Ebenso signifikant können dynamische Unterschenkel-Gehorthesen (Ankle Foot Orthosis, AFO) bei Patienten mit zerebralen Bewegungsstörungen und einer Instabilität oder (neuro-)muskulären Fehlfunktion des oberen Sprunggelenks (OSG)/Kniegelenkes ohne schwere strukturelle Fußfehlstellung zur Schmerzreduktion und Verbesserung der Steh- und Gehfunktion durch eine Stabilisierung des unteren Sprunggelenks (USG) und OSG und Rückverlagerung des Kniegelenkes der gesamten Beinachse beitragen. Indikationen sind Zehenballen‑, Stepper‑, Kauer‑, Hakengang mit/ohne leichten Fall‑, Spitz‑, Platt‑, Hohl‑, Klumpfüßen, Kontraindikationen sind strukturelle Fußfehlbildung oder ‑stellung und Kontrakturen. Interessant sind die positiven Ergebnisse der ersten familienzentrierten Studien24.
Bei nicht-gehfähigen Patienten kann sensomotorisches Lernen durch propriozeptiven Input mit dynamischen Ganzkörper-Stehorthesen (Trunk Hip Knee Ankle Foot Orthosis, THKAFO), erreicht werden. Bei ausreichender Kopfkontrolle kann bei Tetraparese oder Tetraplegie mit Instabilität oder neuromuskulärer Fehlfunktion der Rumpf-Becken-Beingelenke und gewichtsbedingt bis zum Alter von etwa 12 Jahren eine Kräftigung der tonischen Haltemuskulatur durch bewegliche Stabilisierung des Rumpfes und der Beinachsen erzielt werden (Abb. 6). Kontraindikationen sind auch hier schwere strukturelle Fehlstellungen und Kontrakturen. Neueste Studien zeigen eine auch nach 7 Jahren anhaltende Verbesserung der Hüftentwicklung bei 15–30° Abduktion und mind. 10 Stunden Stehtherapie pro Woche25 und Reduktion von operationsbedürftigen Hüftluxationen bei früher Versorgung in den ersten Lebensjahren26.
Auch für Senso-Orthesen auf der Basis der dynamischen Stabilität erleichtern Qualitätskriterien die Beurteilung der Wirksamkeit und des Stellenwerts im Gesamtbehandlungskonzept: Dynamische Einlagen, Knöchel-Fuß-Orthesen, dynamische Stehorthesen und Rumpforthesen, werden individuell modellgeformt gefertigt und sollen in Verbindung mit Therapie und Alltagsaktivitäten ein Training der Mechanorezeptoren und des afferenten Systems sowie eine ungestörte Mobilität mit Kräftigung der Muskulatur bei korrigierten Hebelarmen in Neutralstellung der Gelenke ermöglichen. Die berichtete Funktionsverbesserung und positive Aufnahme durch Patienten, die Beurteilung von ADL-Aufgaben, die visuelle und instrumentelle Messung von Haltungs- und Gangparametern und langfristige Entwicklung der Bewegungsorgane geben Hinweise auf die erwünschte Wirksamkeit.
Wie wirken Senso-Orthesen bei Elektrostimulation?
Im Gegensatz zur Kompression kann Elektrostimulation bei zerebralen Bewegungsstörungen mit einer noch stärkeren Reizapplikation der Rezeptoren therapeutisch genützt werden und multiple subjektiv und objektiv messbare Wirkungen auslösen. Elektrotherapie kann zur Schmerzdämpfung, Stimulation innervierter schwacher Muskeln, Steigerung der Neuroplastizität und Spastikreduktion eingesetzt werden.
Schmerzreduktion und damit eine Bewegungsverbesserung kann durch Schwellstrom mittels Oberflächenelektroden erzielt werden und wird z. B. bei einer Schulterluxation nach Insult verwendet.
Die Stimulation zentral gelähmter Muskeln und Muskelkräftigung schwacher Muskeln bei zentralen Paresen erfolgt durch Elektrostimulation mittels Schwellenwerttraining. Sie wird mit Hilfe von EMG-getriggerter Elektrostimulation z. B. für M. triceps brachii oder M. tibialis anterior klinisch eingesetzt.
Elektrostimulation ermöglicht auch die Tonussenkung bei spastischen Paresen. Periphere repetitive sub-sensorische Stimulation spricht propriozeptive Afferenzen an und wird mittels Handschuh oder Socken 2‑mal täglich 20–30 Min. 0,3 ms mit 30 Hz subsensorisch zur Spastikreduktion angewendet27 28.
Ebenso ermöglicht Elektrostimulation die Aktivierung des Gehirns und neuronale Vernetzung bei zerebralen Bewegungsstörungen. Sensorische afferente Stimulation wird zur Förderung der Neuroplastizität und Sensibilitätssteigerung verwendet29.
Hochtontherapie kann durch simultane Frequenz- und Amplituden-Modulation mit sinusförmigem, metallverträglichem Wechselstrom mit Frequenzen von 4000–33000 Hz und bis zu 300 mA eingesetzt werden. Indikationen sind Zerebralparesen nach Insult und bei Multipler Sklerose, wobei sich Heimgeräte zur täglichen Anwendung mit längerer Therapiedauer anbieten30.
Es ist wichtig zu beachten, dass die Wirkung von Senso-Orthesen durch Elektrostimulation von Person zu Person unterschiedlich sein kann und von verschiedenen Faktoren wie der Lokalisation und Ausdehnung der primären Schädigung, der Art der zerebralen Bewegungsstörung und Lähmung sowie dem individuellen Krankheitsverlauf abhängt.
Entwicklung von E‑Stimulationsorthesen bei zerebralen Bewegungsstörungen
Bisher wurden verschiedene Elektrostimulationsorthesen für zerebrale Bewegungsstörungen entwickelt. Am längsten klinisch angewendet wird die sogenannte funktionelle Elektrostimulation (FES), bei der elektrische Impulse verwendet werden, um geschwächte oder gelähmte Muskeln zu stimulieren. Diese Art von Orthesen kann bei Patienten mit zerebralen Bewegungsstörungen eingesetzt werden, um Bewegungen zu unterstützen und die Muskelkraft zu verbessern.
Funktionelle Elektrostimulation wird mit Stimulationsmanschetten am Unterarm, Ober- und Unterschenkel zur Aktivierung der langen Hand‑, Bein- und Fußmuskulatur erfolgreich eingesetzt. Indikationen sind eine Schwäche der Handgelenkstrecker, Kniestrecker, Kniebeuger, Pronatoren und Fußhebemuskulatur nach Insult, bei unilateraler Zerebralparese und Multipler Sklerose. Kontraindikationen sind strukturelle Fehlstellungen und fehlende subjektive Akzeptanz des Trägers bzw. der Trägerin.
Bei den Systemen für die unteren Extremitäten, wie beispielsweise „Bioness“, „Alfess“ und „WalkAide“, erfassen Bewegungssensoren die Position des Beins im Gangzyklus und triggern den richtigen Stimulationszeitpunkt. Die vollständig ersetzte Funktion kann in der 3D-Bewegungsanalyse dokumentiert werden.
Systeme für die oberen Extremitäten sind eher im therapeutischen Bereich verwendbar. „Bioness H200“ wird beispielsweise mit der kontralateralen Hand über eine Fernsteuerung getriggert, der „Regrasp-Bewegungssensor“ hinter der Ohrmuschel beim Nicken des Kopfes.
Die Wirksamkeit und der therapeutische Nutzen von Stimulationsorthesen31 32 und Neuroprothesen33 für Patienten mit zerebralen Bewegungsstörungen nach Insult wird bereits seit Jahrzehnten in zahlreichen Studien belegt. Die Systeme werden von in der klinischen Anwendung erfahrenen Zentren als nicht für alle Patienten geeignet beurteilt, eine ausgiebige Testung und korrekte Einstellung sind jedenfalls unabdingbar34.
Qualitätskriterien: Manschetten mit funktioneller Elektrostimulation sollen fehlende bzw. schwache Muskelfunktionen ersetzen, wobei der praktische Nutzen für Patienten das etwas aufwändige Tragen und Verwenden des instrumentellen Hilfsmittels im Alltag übertreffen sollte. Die Wirkung kann an der oberen Extremität mittels ADL-Aufgaben und für die unteren Extremitäten mittels klinischer bzw. instrumenteller Ganganalyse meist einfach beurteilt werden.
Eine weitere Art von Elektrostimulationsorthesen sind sensorische Orthesen, die speziell für die Behandlung von Sensibilitätsstörungen entwickelt wurden. Diese Orthesen verwenden elektrische Impulse, um die sensorische Wahrnehmung zu verbessern und die propriozeptiven Fähigkeiten zu fördern. Sie können bei Patienten mit zerebralen Bewegungsstörungen eingesetzt werden, um die Körperwahrnehmung und das Gleichgewicht zu verbessern.
Die sub-sensorische Stimulation, die durch das Adressieren propriozeptiver Afferenzen zur Tonusregulation und Spastikreduktion führt, wird von der Neuromodulations-Ganzkörper-Kompressions- und E‑Stimulations-Orthese „Exopulse Mollii Suit“ angewendet. Diese Form der elektrischen Stimulation durch Oberflächenelektroden ist eine nicht-invasive therapeutische Technik zur Verbesserung der willkürlichen motorischen Kontrolle und zur Verringerung von Schmerzen und Spastizität bei Patienten mit zerebralen Bewegungsstörungen. Ein Vorteil ist die bessere Compliance, da Patienten die Impulse im Gegensatz zur FES nicht spüren. Bei diesem System handelt es sich um einen eng anliegenden Ganzkörperanzug mit integrierten Elektroden, der für die selbst verabreichte elektrische Stimulation zur Verringerung von Spastizität und zur Förderung der Beweglichkeit entwickelt wurde. 58 eingebettete Elektroden stimulieren mit 20 Hz und steuern über Dermatome 40 Myotome bzw. Muskelgruppen an (Abb. 7).
Die Wirkungsweise dieser Senso-Orthese, bei der niedrige Frequenzen mit niedriger Intensität einen sensorischen Input hervorrufen, aber keine Muskelkontraktionen auslösen, ist nicht vollständig geklärt. Der theoretische Hintergrund dieser Methode bezieht sich in erster Linie auf das Konzept der reziproken Hemmung, d. h., dass der sensorische Input eines Muskels die Aktivierung eines antagonistischen Muskels durch Aktivierung disynaptischer reziproker Ia-Afferenzen hemmen kann. Beim neurophysiologischen Mechanismus der Antagonisten-Hemmung erreichen daher unterschwellige elektrische Impulse über taktile Hautnerven ohne Beteiligung der motorischen Anteile die entsprechenden spinalen Segmente, werden verschaltet und lösen im Renshaw-Interneuron eine Hemmung des Antagonisten aus, ohne eine Muskelkontraktion auszulösen.
Das Ziel dieser Senso-Orthese ist somit die Stimulation eines antagonistischen Muskels (z. B. Fußhebers), um die reflexvermittelte Überaktivität eines antagonistischen Muskels (z. B. Plantarflexots) zu reduzieren, indem eine reziproke Hemmung induziert wird. Wie bei der herkömmlichen TENS niedriger Intensität, könnten jedoch auch andere Mechanismen eine Rolle spielen35.
Der „Exopulse Mollii Suit“ wurde in mehreren klinischen Erfahrungsberichten mit positiven Ergebnissen bewertet, was auf sein Potenzial für die Rehabilitation hinweist. In einer rezenten Übersichtsarbeit36 wurde die Wirksamkeit für die Rehabilitation und Akzeptanz durch Patienten untersucht, wobei sich zeigte, dass die positiven Auswirkungen der Neuromodulations-Ganzkörper-Kompressionsorthese auf die Verbesserung der motorischen Funktionen und die Verringerung der Spastik mit der Dauer der Verabreichung und der Dosierung der Behandlung zusammenhängen, die wiederum vom Schweregrad der Beeinträchtigung des Patienten und seinen Behandlungszielen abhängen37.
Die überwiegende Anzahl der Patienten berichten über positive Effekte, die spontan oder nach wenigen Stunden eintreten. Sie beobachteten eine verbesserte Bewegungskoordination, besseren Schlaf und eine Entspannung der Muskulatur. Bisher wurden vonseiten der Behandelten und Behandler keine negativen Auswirkungen berichtet38.
Da nicht bei allen Patienten diese subjektiven und objektiven Verbesserungen beobachtet werden, sind weitere Studien notwendig, um Indikationen und Kontraindikationen exakt definieren zu können.
Derzeit kann die Testung bei Kindern und Erwachsenen mit zerebralen Bewegungsstörungen nach Insult, Schädel-Hirn-Trauma, bei Zerebralparesen und Multipler Sklerose empfohlen werden. Als Kontraindikationen werden vom Hersteller elektronische Implantate, lebenserhaltende Geräte, Geräte, die im Hochfrequenzbereich betrieben werden, zusammen mit EKG-Geräten und dem Vorliegen einer Schwangerschaft angegeben. Relativ kontraindiziert wäre die Orthese bei Epilepsie, Herz-Kreislauf‑, onkologischen, Haut- und Infektionskrankheiten sowie nach chirurgischen Eingriffen.
Erfahrungen mit der Anwendung von Senso-Orthesen und Ausblick
Der Indikationsbereich der Senso-Orthesen umfasst prinzipiell Kleinkinder, Kinder, Jugendliche und auch Erwachsene mit zerebralen Bewegungsstörungen aller grobmotorischen Funktionsstufen. Sie können im Therapiesetting oder auch für Aktivitäten im Alltag eingesetzt werden. Voraussetzung für die Verwendung sind eine ausreichende Kopfkontrolle und Oberflächensensibilität, eine ausreichende Aktivierbarkeit und Kraft der tonischen und/oder phasischen Muskulatur sowie fehlende oder nur wenig fortgeschrittene strukturelle Veränderungen des Bewegungsapparates, um eine weitgehende Neutralstellung der Wirbelsäulen- und Extremitätengelenke mit physiologischen Hebelarmen der Muskulatur in der Orthese erreichen zu können.
In Zentren, die Kinder und Jugendliche mit Zerebralparesen betreuen, konnten bereits über Jahrzehnte Erfahrungen mit Senso-Orthesen während der Therapie und in der Verwendung zuhause gesammelt werden. Im Rahmen der Physiotherapie und bei den neuroorthopädischen Teambesprechungen wird die zusätzliche Verwendung nach einer ausführlichen Anamnese zu den regelmäßigen Aktivitäten und nach einer klinischen Untersuchung zunächst gemeinsam diskutiert. Der erwartete Nutzen, wie verbesserte Kraftentwicklung, mehr Selbstständigkeit, größere Mobilität, wird gegen mögliche Probleme, wie Einschränkungen und Aufwand im Familienalltag, abgewogen.
Senso-Orthesen nach dem Prinzip der dynamischen Stabilität, wie Fuß‑, Rumpf- und Ganzkörperorthesen, werden anschließend verordnet und individuell gefertigt und im Rahmen von Hilfsmittelkontrollterminen im Team übernommen, die Passform, Akzeptanz und Wirksamkeit beurteilt und im weiteren Verlauf im Abstand von etwa 3–4 Monaten evaluiert.
Kompressionsorthesen und E‑Stimulationsorthesen werden nach Maß bestellt oder gefertigt und sollten vorab getestet werden. Von orthopädietechnischer Seite werden dazu Termine zur Austestung im Rahmen der Therapie und/oder zuhause angeboten. Idealerweise werden die Senso-Orthesen im Behandlungsteam auf Passform und Akzeptanz überprüft, die Wirkung nach etwa 30- bis 60-minütiger Verwendung gemeinsam anhand quantitativer Parameter, wie Gehstrecke, Ganggeschwindigkeit, Wirbelsäulenaufrichtung und Fingerfertigkeit, und qualitativer Parameter, wie Gangbild, Haltung und Handfunktion, beurteilt. Foto- bzw. Filmaufnahmen von Gangbild, Alltagsaktivitäten und/oder Greiffunktion werden vor und nach Austestung in Frontal- und Sagittalebene angefertigt und mit dem Behandlungsteam geteilt. Bei positiver objektiver und subjektiver Beurteilung erfolgen dann die Verordnung, Anpassung und Übernahme der Senso-Orthese.
Fazit
Im Gegensatz zu den zahlreichen Anwenderberichten sind wissenschaftliche Studien zu Senso-Orthesen noch selten. Diese beschreiben bei einem hohen Prozentsatz an Patienten Verbesserungen von verschiedenen Mobilitäts-Scores, von Verhalten, Motivation und Teilhabe. Nachteile oder ungünstige Effekte der Verwendung von Senso-Orthesen werden nicht berichtet. Dies entspricht auch den Erfahrungen unserer Klinik und betreuten Einrichtungen mit allen genannten Modellen. Wir sehen durchweg eine gute Akzeptanz der Kompressions- und Elektrostimulationsorthesen durch die Patienten und deren Familien nach einer kurzen Probezeit von wenigen Tagen. Bei regelmäßiger Verwendung von Kompressionsorthesen von mindestens täglich 30–60 Minuten konnten wir bei den meisten Patienten Verbesserungen der Gelenkbeweglichkeit, Gelenkentwicklung, Motorik und Alltagsaktivitäten abhängig von der motorischen Erkrankung, aber unabhängig vom verwendeten Modell feststellen. Bei Elektrostimulationsorthesen konnten wir diese Verbesserungen ebenfalls bei einem Teil der Patienten beobachten. Jedoch halten wir eine Austestung vor der konkreten Behandlungsindikation unbedingt für erforderlich.
Exakte Angaben zu Indikationen können, speziell für Orthesen mit Elektrostimulation, zum derzeitigen Stand der wissenschaftlichen Literatur und klinischen Erfahrungen noch nicht gegeben werden. Weitere Studien zur Funktion des sensomotorischen Systems sind notwendig, um zu verstehen, wie extero- und propriozeptiver Input zentral verarbeitet werden und unter physiologischen und pathologischen Bedingungen zur Haltungs- und Bewegungssteuerung beitragen. In der Zwischenzeit könnten mehr Erfahrungsberichte mit einzelnen Senso-Orthesen und bei einzelnen Krankheitsbildern im Kindes- und Erwachsenenalter dazu beitragen, Indikationen und Kontraindikationen genauer einzugrenzen und dem Behandlungsteam bei der klinischen Entscheidung helfen, welche Kinder und Erwachsene mit zerebralen Bewegungsstörungen von welchen Senso-Orthesen am besten profitieren.
Der Autor
Prof. Dr. Walter Michael Strobl, MBA
Facharzt für Orthopädie und Unfallchirurgie
Schwerpunkte: Kinderorthopädie, Neuroorthopädie, Rehabilitation
Institut MOTIO für Kinder- und Neuroorthopädie
Schönlaterngasse 9/10b
1010 Wien
walter.strobl@motio.org
www.motio.org
Begutachteter Beitrag/reviewed paper
Strobl WM. Senso-Orthetik mit Kompression und Elektrostimulation bei zerebralen Bewegungsstörungen – was wissen wir zur Effektivität? Orthopädie Technik, 2023; 74 (11): 38–47
- Die orthopädietechnische Versorgung mit einer dynamischen Fingerstreckorthese als eigenständige Therapie bei der Dupuytren’schen Kontraktur — 26. März 2026
- Vergleichende Prüfung konventioneller und additiv gefertigter Prothesenschäfte in Anlehnung an DIN EN ISO 10328:2016 — 10. März 2026
- Easypreg – ein Faserverbundwerkstoff zum Tiefziehen — 9. März 2026
- Schweizer K, Romkes J, Coslovsky M, Brunner R. The influence of muscle strength on the gait profile score (GPS) across different patients. Gait Posture, 2014; 39 (1): 80–85
- Xanthos DN, Sandkühler J. Neurogenic neuroinflammation: inflammatory CNS reactions in response to neuronal activity. Nature Reviews Neuroscience, 2014; 15 (1): 43–53. doi: 10.1038/nrn3617
- Schmidt SM, Hägglund G, Alriksson-Schmidt AI. Bone and joint complications and reduced mobility are associated with pain in children with cerebral palsy. Acta Paediatrica, 2020; 109: 541–549. doi: 10.1111/apa.15006
- Østergaard C et al. Pain is frequent in children with cerebral palsy and negatively affects physical activity and participation. Acta Paediatrica, 2020; 110 (1), 301–306
- Strobl WM. Geräte zur selbstbestimmten Gehtherapie mit reziproker Beinführung – neuroorthopädische Empfehlungen. Orthopädie Technik, 2019; 70 (1): 27–33
- Macaulay et al. Developing Proprioceptive Countermeasures to Mitigate Postural and Locomotor Control Deficits After Long-Duration Spaceflight. Frontiers in Neuroscience, 2021; 15: 658985. doi: 10.3389/fnsys.2021.658985
- Motanova E et al. Application of Space Technologies Aimed at Proprioceptive Correction in Terrestrial Medicine in Russia. Frontiers in Physiology, 2022; 13: 921862. doi: 10.3389/fphys.2022.921862
- Aris B. The Kozijavkin method. Lancet, 2004; 364 (9449): 1927–1928. doi: 10.1016/S0140-6736(04)17497–7
- Ko M‑S, Lee J‑A, Kang S‑Y, Jeo H‑S. Effect of Adeli suit treatment on gait in a child with cerebral palsy: a single-subject report. Physiotherapy: Theory and Practice, 2015; 31 (4): 275–282. doi: 10.3109/09593985.2014.996307
- Hylton N, Allen C. The development and use of SPIO Lycra compression bracing in children with neuromotor deficits. Journal of Pediatric Rehabilitation Medicine, 1997; 1 (2): 109–116. doi: 10.3109/17518429709025853
- Giray E, Keniş-Coşkun Ö, Güngör S, Karadağ-Saygı E. Does stabilizing input pressure orthosis vest, lycra-based compression orthosis, improve trunk posture and prevent hip lateralization in children with cerebral palsy? Turkish Journal of Physical Medicine and Rehabilitation, 2017; 64 (2): 100–107. doi: 10.5606/tftrd.2018.1332
- Kokes S. Der Einfluss einer flexiblen Korsettversorgung auf die Atemfunktion von Kindern mit cerebraler Bewegungsstörung, GMFCS Level IV und V. Masterthesis. Neuroorthopädie-Lehrgang. Donau-Universität Krems. Vortrag beim 13. Internationalen Symposium für Neuroorthopädie 25.–27.01.2018 Wien
- Wunderlich, I. Die Auswirkung von Kompressionsrumpforthesen auf die Aufrichtung der Wirbelsäule zerebralgeschädigter Kinder. Masterthesis. Neuroorthopädie-Lehrgang. Donau-Universität Krems. Vortrag beim 13. Internat. Symposium für Neuroorthopädie 25.–27.01.2018 Wien
- Belizón-Bravo N et al. Effects of Dynamic Suit Orthoses on the Spatio-Temporal Gait Parameters in Children with Cerebral Palsy: A Systematic Review. Children (Basel), 2021; 8 (11): 1016. doi: 10.3390/children8111016
- Ferrari A. From movement to action: a new framework for cerebral palsy. European Journal of Physical and Rehabilitation Medicine, 2019; 55 (6): 852–861. doi: 10.23736/S1973-9087.19.05845–3
- Kajiura I et al. Concept and treatment outcomes of dynamic spinal brace for scoliosis in cerebral palsy. Journal of Pediatric Orthopaedics B, 2019; 28 (4): 351–355. doi: 10.1097/BPB.0000000000000580
- Rutz E, Brunner R. Management of spinal deformity in cerebral palsy: conservative treatment. Journal of Children’s Orthopaedics, 2013; 7(5): 415–418. doi: 10.1007/s11832-013‑0516‑5
- Strobl WM. Seating. Journal of Children’s Orthopaedics, 2013; 7 (5): 395–399. doi: 10.1007/s11832-013‑0513‑8
- Lastring L. „Sensomotorische“ Einlagenversorgung – kritische Diskussion des Begriffs. Orthopädie Technik, 2022; 73 (2): 40–46
- DGOOC-Beratungsausschuss Orthopädieschuhtechnik. Stellungnahme zu sensomotorisch wirkenden Fußorthesen (SMFO). Orthopädieschuhtechnik, 2016; 68 (4): 26–32
- MacFarlane C, Orr R, Hing W. Sensomotoric Orthoses, Ankle-Foot Orthoses, and Children with Cerebral Palsy: The Bigger Picture. Children (Basel), 2020; 7 (8): 82. doi: 10.3390/children7080082
- Morris C, Newdick H, Johnson A. Variations in the orthotic management of cerebral palsy. Child: Care, Health and Development, 2002; 28 (2): 139–147. doi: 10.1046/j.1365–2214.2002.00259.x
- Rogozinski BM et al. The efficacy of the floor-reaction ankle-foot orthosis in children with cerebral palsy. Journal of Bone & Joint Surgery, 2009; 91 (10): 2440–2447. doi: 10.2106/JBJS.H.00965
- Ribeiro Volpini Lana M et al. ‚What if it were like this?‘ Perception of mothers of children with cerebral palsy about the ankle-foot orthosis of their children: A qualitative study. Child: Care, Health and Development, 2021; 47 (2): 252–260. doi: 10.1111/cch.12840
- Martinsson C, Himmelmann K. Abducted Standing in Children with Cerebral Palsy: Effects on Hip Development After 7 Years. Pediatric Physical Therapy, 2021; 33 (2): 101–107. doi: 10.1097/PEP.0000000000000789
- Roupec J. Frühe Stehintervention und deren Einfluss auf die Notwendigkeit von Hüftoperationen bei Kindern mit Cerebralparese – eine retrospektive Langzeitanalyse einer Stichprobe in Ost-Österreich. Unveröffentlichte Masterthesis Neuroorthopädie – Disability Management. Donau-Universität für Weiterbildung Krems. Juni 2023
- Iyanaga T et al. Recumbent cycling with integrated volitional control electrical stimulation improves gait speed during the recovery stage in stroke patients. Journal of Exercise Rehabilitation, 2019; 25; 15 (1): 95–102. doi: 10.12965/jer.1836500.250
- Mahmood A, Veluswamy SK, Hombali A, Mullick A, N M, Solomon JM. Effect of Transcutaneous Electrical Nerve Stimulation on Spasticity in Adults With Stroke: A Systematic Review and Meta-analysis. Archives of Physical Medicine and Rehabilitation, 2019; 100 (4): 751–768. doi: 10.1016/j.apmr.2018.10.016
- Dimitrijević MM, Soroker N. Mesh-glove. 2. Modulation of residual upper limb motor control after stroke with whole-hand electric stimulation. Scandinavian Journal of Rehabilitation Medicine, 1994; 26 (4): 187–190
- Biowski P. Elektrotherapie bei cerebralen Bewegungsstörungen. Webinar zur Senso-Orthetik. Wien: Fortbildungsinstitut Motio, April 2023
- Hummelsheim H, Maier-Loth ML, Eickhof C. The functional value of electrical muscle stimulation for the rehabilitation of the hand in stroke patients. Scandinavian Journal of Rehabilitation Medicine, 1997; 29 (1): 3–10
- Alon G, Levitt AF, McCarthy PA. Functional electrical stimulation enhancement of upper extremity functional recovery during stroke rehabilitation: a pilot study. Neurorehabilitation & Neural Repair, 2007; 21 (3): 207–215. doi: 10.1177/1545968306297871
- Hausdorff JM, Ring H. Effects of a new radio frequency-controlled neuroprosthesis on gait symmetry and rhythmicity in patients with chronic hemiparesis. American Journal of Physical Medicine & Rehabilitation, 2008; 87 (1): 4–13. doi: 10.1097/PHM.0b013e31815e6680
- Sepin W. Erfahrungen in der klinischen Anwendung von Senso-Orthesen. Webinar zur Senso-Orthetik. Wien: Fortbildungsinstitut Motio, April 2023
- Tinazzi M et al. Long-lasting modulation of human motor cortex following prolonged transcutaneous electrical nerve stimulation (TENS) of forearm muscles: evidence of reciprocal inhibition and facilitation. Experimental Brain Research, 2005; 161 (4): 457–464. doi: 10.1007/s00221-004‑2091‑y
- Perpetuini D et al. Use and Effectiveness of Electrosuit in Neurological Disorders: A Systematic Review with Clinical Implications. Bioengineering (Basel), 2023; 10 (6): 680. doi: 10.3390/bioengineering10060680
- Pennati GV et al. Effects of 60 Min Electrostimulation With the EXOPULSE Mollii Suit on Objective Signs of Spasticity. Frontiers in Neurology, 2021; 12: 706610. doi: 10.3389/fneur.2021.706610
- Jonasson LL, Sörbo A, Ertzgaard P, Sandsjö L. Patients’ Experiences of Self-Administered Electrotherapy for Spasticity in Stroke and Cerebral Palsy: A Qualitative Study. Journal of Rehabilitation Medicine, 2022; 54: jrm00263. doi: 10.2340/jrm.v53.1131