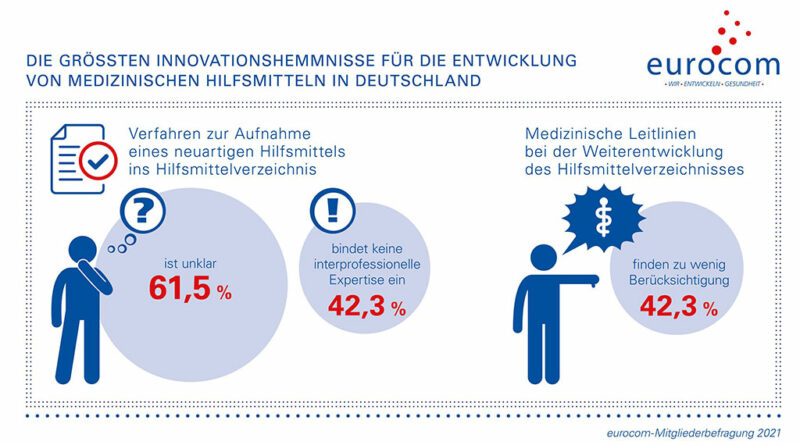
Die Hemmnisse für innovative und qualitätsorientierte Hilfsmittelversorgung müssen beseitigt werden, so das Fazit der Eurocom. Als schwerwiegendste Hemmnisse identifizierten die Eurocom-Unternehmen, die sich im Mai 2021 an der Mitgliederbefragung beteiligt hatten, demnach das unsichere Verfahren zur Aufnahme neuartiger Produkte in das Hilfsmittelverzeichnis (HMV) sowie die kostenintensiven regulatorischen Auswirkungen der Medical Device Regulation (MDR).
Im HMV-Verfahren sehen 61,5 Prozent der Befragten ein Risikopotenzial für die Aufrechterhaltung und Weiterentwicklung des Standards. Aufnahmeanträge wurden bislang bei 66 Prozent der Befragten abgelehnt, bei 59 Prozent war dies kein Einzelfall. Eurocom-Geschäftsführerin Oda Hagemeier erklärt dazu: „Wir brauchen ein klares und standardisiertes Verfahren zur Aufnahme neuartiger Produkte ins Hilfsmittelverzeichnis, insbesondere zur Anerkennung des medizinischen Nutzennachweises, unter stärkerer Berücksichtigung medizinischer Leitlinien.“ Die Eurocom fordert daher eine beratende Expertenkommission, die auf Antrag der zur Stellungnahme berechtigten Organisationen verpflichtend zum Einsatz kommt.
MDR als Kostentreiber
Als Markthemmnis werten 61,5 Prozent der Befragungsteilnehmer auch die MDR. Für 96 Prozent sind zusätzliche Kosten bei einer Gesamtkostensteigerung von bis zu 10 Prozent entstanden. Diese schlagen sich dabei vor allem in zusätzlichem Personal nieder, berichten 84,6 Prozent, sowie in klinischen Prüfungen (50 Prozent). Die Quintessenz für Geschäftsführerin Oda Hagemeier: eine konsequente EU-Marktüberwachung. „Der Marktzugang nicht-konformer Produkte der Freiverkaufslandschaft muss verhindert werden. Für fairen Wettbewerb und mehr Patientensicherheit.“
Auch eine positive Nachricht ergab die Mitgliederbefragung: Trotz Einbußen kommen die Eurocom-Mitgliedsbetriebe weitestgehend stabil durch die Corona-Krise. 88 Prozent der Befragten konnten alle Arbeitsplätze erhalten. Zwei weitere Forderungen ergeben sich dennoch für Oda Hagemeier aus den Erfahrungen aus der Corona-Pandemie: „Die Pandemie hat Verunsicherung in der Bevölkerung ausgelöst, Patienten haben aus Furcht vor Ansteckung mit dem Virus auch notwenige Untersuchungen und Behandlungen unterlassen, auch solche, auf die sie für eine dauerhafte Versorgung zur Linderung ihrer Beschwerden dringend angewiesen sind. Daher ist es erstens unerlässlich, dass Folgeverordnungen von zum Gebrauch bestimmten Hilfsmitteln in Pandemiezeiten kontaktlos möglich sind. Zweitens müssen ärztliche und nichtärztliche Leistungserbringer in einer Pandemie befähigt werden, einen sicheren Versorgungsalltag mit den gebotenen Hygiene- und Schutzmaßnahmen aufrechterhalten zu können.“ Ein gesundheitspolitisches Krisenmanagement müsse gewährleisten, dass Hersteller als versorgungsrelevant anerkannt und bevorzugt bei Schutzvorkehrungen (PSA, Impfung) berücksichtigt werden, so auch der Tenor von 53,8 Prozent der Befragten.
- Die orthopädietechnische Versorgung mit einer dynamischen Fingerstreckorthese als eigenständige Therapie bei der Dupuytren’schen Kontraktur — 26. März 2026
- Vergleichende Prüfung konventioneller und additiv gefertigter Prothesenschäfte in Anlehnung an DIN EN ISO 10328:2016 — 10. März 2026
- Easypreg – ein Faserverbundwerkstoff zum Tiefziehen — 9. März 2026