Einleitung
Nach der Amputation eines Körperteils nehmen bis zu 90 Prozent der Patienten diese fehlende Gliedmaße als noch vorhanden wahr 1. Dieser als Phantomgefühl bezeichnete Effekt reicht von einem einfachen Gefühl der Anwesenheit bis hin zur Wahrnehmung einer bestimmten Körperhaltung, Form oder sogar unwillkürlichen Bewegungen 2. Zusätzlich zu diesen Empfindungen leiden 45–85 Prozent der Patienten unter Phantomschmerzen, die sich als Kribbeln, Brennen oder Jucken, aber auch als starke Schmerzen wie Stechen, Schießen, Krämpfe oder Brennen äußern können 3. Phantomschmerz manifestiert sich in der Regel 24 Stunden bis eine Woche nach der Amputation und nimmt bei vielen Patienten im Laufe der Zeit an Intensität und Häufigkeit ab 4. Vor allem in den distalen Bereichen der fehlenden Gliedmaße halten Phantomempfindungen und ‑schmerzen länger an. Einige Patienten leiden jahrzehntelang unter diesen Schmerzen 5 6. Die zugrundeliegenden Mechanismen werden noch immer kontrovers diskutiert. Die derzeit vorherrschende Theorie ist das kortikale „Re-Mapping“, nach dem das Gehirn auf den Verlust einer Gliedmaße mit einer Reorganisation des somatosensorischen Kortex reagiert 7 8. Eine positive Korrelation zwischen Phantomschmerzen und der Wahrnehmung der Prothese als Fremdkörper konnte bereits nachgewiesen werden 9. Wenn die Prothese in das Selbstbild des Patienten eingebettet ist, dann spricht man von Embodiment 10. Embodiment fördert die Aktivität in den Hirnarealen, die für die Kontrolle der Extremitäten zuständig sind, und verringert so die kortikale Reorganisation, die typischerweise auf die Amputation folgt. Die Verringerung dieser Umstrukturierung scheint die Grundlage für die Verringerung von Phantomschmerzen zu sein 11.
Abbildung und Erfragung von Phantomwahrnehmung und ‑schmerzen
Da Phantomwahrnehmung eine schwer fassbare Entität darstellt, ist es nicht trivial, den Fortschritt dieser Veränderung im Verlauf der Behandlung zu verfolgen. Derzeit existiert weder ein standardisiertes Formular für die Dokumentation von Phantomempfindungen und Phantomschmerzen im Verlauf der Therapie noch für deren Visualisierung aus Sicht der Patienten. Beides ist jedoch von hoher klinischer Relevanz für die therapeutische Betreuung als auch für die orthopädietechnische Versorgung 12.
Die Dokumentation erfolgt in der Regel mit Schmerzfragebögen wie dem Kurzform-McGill-Schmerzfragebogen 13, der zum De-facto-Standard für die Beurteilung der Qualitäten von Phantomschmerzen geworden ist 14. Andere Schmerzfragebögen wie das Brief Pain Inventory (BPI) 15 bieten ein 2D-Körperdiagramm zur Lokalisierung des Schmerzes, doch die meisten Dokumentationen werden nach wie vor handschriftlich und in offener Form durchgeführt. Diese Form der Dokumentation hat den Nachteil, dass die Quantifizierung von Schmerzen kostspielig und ungenau ist.
Auf der Suche nach einer entsprechenden Softwarelösung wurden wir zwar fündig, was digitale Werkzeuge zum Einzeichnen von generellen Schmerzen betrifft 16, die teilweise auch das direkte Zeichnen auf einem 3D-Modell erlauben 17, jedoch ist keine dieser Lösungen spezifisch für die Erfassung von Phantomschmerzen ausgelegt und bietet auch keine Möglichkeit zur Visualisierung des Phantoms, so dass die Wahrnehmung und das Körperbild von Amputierten nicht abgebildet werden kann. Es gibt zwar Arbeiten, in denen Werkzeuge zur Erstellung eines veränderten Körperbildes vorgestellt wurden, diese beziehen sich jedoch auf das Thema Essstörungen 18. Da wir keine geeignete Software finden konnten, die eine vollständige Dokumentation der Phantomempfindungen und des veränderten Körperbildes ermöglicht, haben wir ein solches Programm selbst entwickelt. Im Folgenden wird die Funktionalität von C.A.L.A. und dessen Evaluierung im Bezug zur Funktionalität und Nutzerfreundlichkeit mit Therapeuten und Patienten beschrieben.
Dokumentation mit C.A.L.A.
Die Grundidee von C.A.L.A. besteht darin, einen virtuellen menschlichen 3D-Avatar so anzupassen, dass dieser das Körperbild der Patienten einschließlich des Phantomempfindens abbildet. Es sind verschiedene Level von Amputationen für die oberen und unteren Extremitäten bis zu den Fingern und Zehen darstellbar. Auch multiple Amputationen können dargestellt und dokumentiert werden. Visuell und funktionell erfolgt eine Trennung zwischen dem Stumpf und dem Phantom. In wiederholten Sitzungen können verschiedene Charakteristika des Phantomgliedes sowie der Empfindungen am Phantom und Stumpf erfasst werden.
Verformung des Phantoms
Manche Patienten berichten, dass sie ihr Phantomglied mit veränderten Proportionen wahrnehmen. Um diesen Umstand abzubilden, können Länge und Umfang einzelner Segmente der Extremitäten wie z. B. Oberarm, Unterarm oder Hand vergrößert oder verkleinert werden. Auch die einzelnen Fingerglieder, inklusive des Daumens, und die Zehen können derartig angepasst werden. Das Telescoping-Phänomen, bei dem bspw. der Unterarm im Ellenbogen verschwindet, kann mit dieser Funktion ebenfalls dargestellt werden.
Positionierung des Phantoms
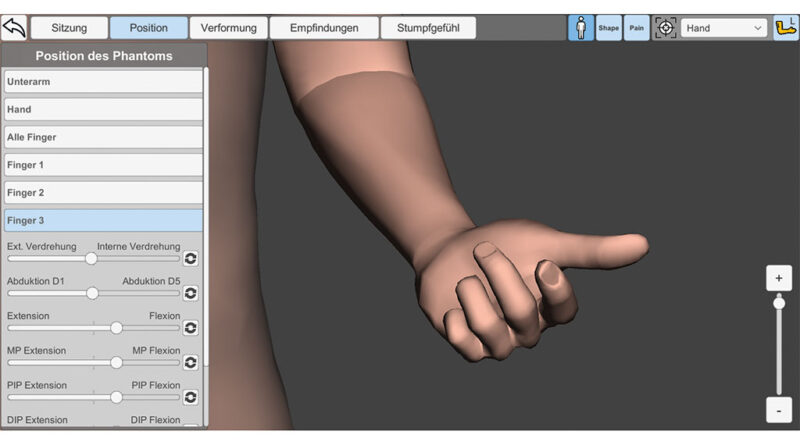
Das Gefühl, dass die Phantomgliedmaße in einer oder mehreren verdrehten oder unnatürlichen Positionen fixiert sind, kann abgebildet werden, indem die entsprechenden Gelenke des 3D-Avatars in die von den Patienten angegebene Position bewegt werden. Es können die Schulter‑, Ellbogen- und Handgelenke sowie die einzelnen Fingergelenke des 3D-Avatars eingestellt werden wie auch die Gelenke der unteren Extremitäten. Alle Gelenke können entlang ihrer natürlichen Achsen und auch um sich selbst uneingeschränkt gedreht werden. Dadurch können alle denkbaren und anatomisch unmöglichen Positionen der oberen und unteren Extremitäten dargestellt werden (siehe Abb. 1).
Einzeichnen von Schmerzen und Phantomempfindungen
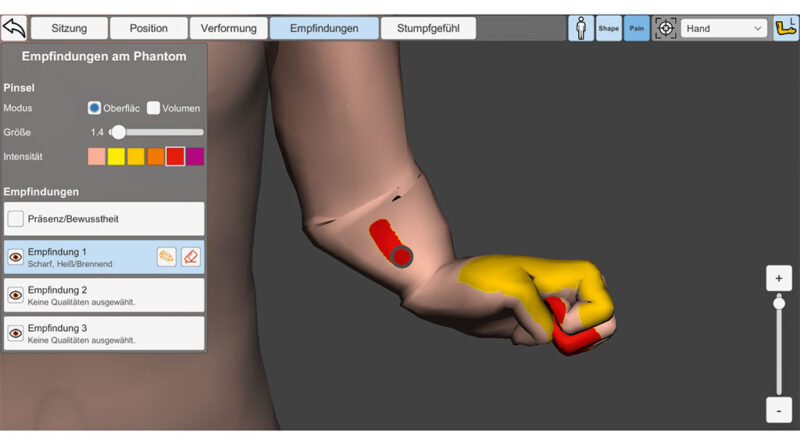
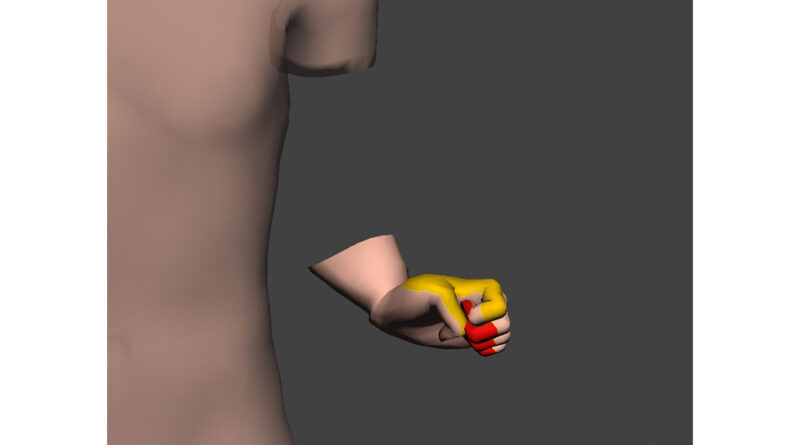
Schmerzen und Phantomempfindungen können in C.A.L.A. direkt auf dem 3D-Avatar eingezeichnet werden. Dazu wird der Mauszeiger oder Finger als Pinsel verwendet und die Schmerzen werden aufgemalt. Die Intensität der Empfindung wird anhand der Numerical Rating Scale (NRS) abgebildet. Die Werte zwischen 0 und 10 sind auf dem Avatar durch einen Farbverlauf von gelb (leicht) bis dunkelrot (sehr stark) dargestellt (siehe Abb. 2). Zusätzlich können der Empfindung mehrere Qualitäten zugeordnet werden, die teilweise aus dem Kurzform-McGill-Schmerzfragebogen übernommen wurden und teilweise auch selbst definiert wurden wie z. B.: oberflächlich, mittel, tief oder bei Ruhe, nachts. Schmerzen können sowohl am Phantom als auch am Stumpf aufgezeichnet werden. Bei Patienten, die berichten, dass sie Teile des Phantomgliedes nur verringert oder nicht wahrnehmen, kann diese empfundene Präsenz ebenfalls direkt auf das Phantom gezeichnet werden. Teile des Phantoms können damit auch visuell ausgeblendet werden (siehe Abb. 3).
Quantifizierung des Körperbildes
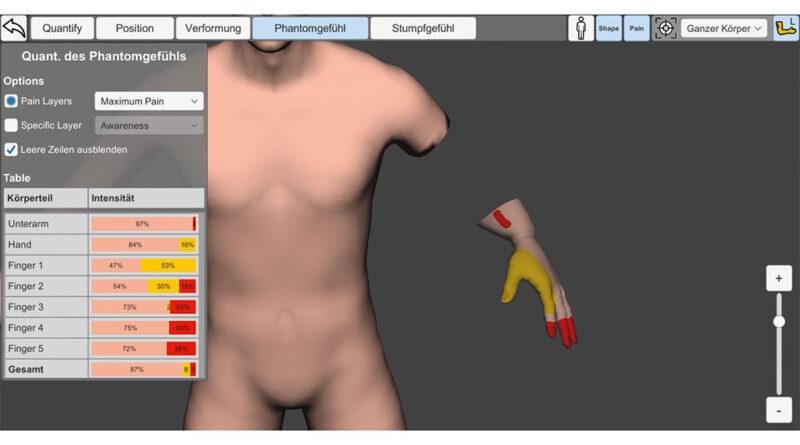
Alle Daten, die während des Dokumentationsprozesses erfasst werden, können abgespeichert und quantifiziert werden und ermöglichen eine Aussage über die Konstitution des Phantoms zum jeweiligen Zeitpunkt. Dies ermöglicht die Analyse der erfassten Aspekte Deformation, Position und Schmerz und deren Beobachtung im Verlauf der Behandlung. Die Quantifizierung der Verformung spiegelt die prozentuale Veränderung der Länge und des Umfangs der jeweiligen Gliedmaßen im Vergleich zum Basismodell wider. Ausgehend von den ursprünglich erfassten Körpermaßen der Patienten könnten diese Veränderungen damit auch absolut in Zentimetern berechnet werden. Die Quantifizierung der Position ergibt sich aus der Abweichung jeder Rotationsachse eines jeden Gelenks von der Grundposition des 3D-Avatars (Neutral-Null-Stellung). Schmerzen werden als Prozentsatz der Körperoberfläche quantifiziert, die mit der jeweiligen Intensität betroffen ist (siehe Abb. 4). Für eine separate Quantifizierung mehrerer Empfindungen können diese in bis zu 3 voneinander unabhängigen, Ebenen eingetragen werden.
Klinisch-therapeutischer Aspekt der Visualisierung
Der Patient zeichnet im engen Austausch mit dem Therapeuten (Physio-/Ergotherapeut) den Schmerz auf den 3D-Avatar ein (siehe Abb. 5). Die potenziell verändert empfundene Position bzw. Gestalt der Phantomextremität wird ebenfalls gemeinsam modelliert, sodass sowohl der Patient als auch der Therapeut eine sehr differenzierte und plastische Vorstellung von der aktuellen Phantomwahrnehmung bekommen.
Die exakte Erfassung und Quantifizierung der schmerzhaften Fläche und die Abgleichung mit Hautdermatomen ermöglichen dem behandelnden Arzt oder Therapeuten außerdem die Zuordnung zu peripher-neuralen Versorgungsgebieten. Darüber hinaus können mit C.A.L.A. neben dem Phantomschmerz auch die Stumpfschmerzen der Patienten erfasst werden, was nicht immer differenziert wird, aber im klinisch-therapeutischen Bereich hochrelevant ist.
Viele der mit C.A.L.A. befundeten Patienten melden uns in diesem Prozess zurück, dass sie sich bisher noch nicht so intensiv und detailliert mit der Wahrnehmung ihres Phantomglieds auseinandergesetzt haben. Diese meist von den Patienten nicht als unangenehm empfundene intensive Auseinandersetzung könnte möglicherweise auch zu einer verbesserten Akzeptanz der amputierten Extremität beitragen.
Es ist in der Physiotherapie üblich, verschiedene physikalische Methoden (z. B. segmentale TENS, Thermotherapie kontralateral) oder den Einsatz von Imaginationstherapien (z. B. Spiegeltherapie, Intentionstraining durch Bewegungsübungen mit dem Phantomglied) individuell bezüglich ihrer Schmerzwirksamkeit mit dem Patienten zu erproben. Eine regelmäßige, einmal wöchentliche Erfassung von Veränderungen im C.A.L.A.-Befund ermöglichen eine sehr differenzierte Verlaufsbeurteilung und Überprüfung der Effektivität eingesetzter Behandlungsmethoden.
Unsere Physiotherapeuten haben mit C.A.L.A. bereits über längere Zeiträume Befunddokumentationen erstellt. Nach ihrer Erfahrung hilft es den Patienten im mehrwöchigen Behandlungsverlauf bei der Schmerzbewältigung, wenn selbst kleine positive Veränderungen in den Schmerz- und Phantomglied-Parametern immer wieder gemeinsam visualisiert und bewertet werden können. Dadurch werden diese Verbesserungen (z. B. Schmerz gleichgeblieben, aber Medikation reduziert; oder Schmerz verringert bei gleicher Medikation) oft erst als Therapieerfolge bewusst gemacht und die Patienten-Adhärenz erhöht.
Hier kann mit C.A.L.A. regelmäßig der tagesaktuelle Zustand des Patienten im Austausch auf Augenhöhe erfasst, visualisiert und, auch im Verlauf, objektiv dokumentiert werden. Die Compliance steigt signifikant, die Patienten fühlen sich ernst- und angenommen. Neben der potenziellen Erhöhung der Therapie-Compliance bei den Patienten kann eine über die Zeit erfolgende Auswertung der Veränderungen in der Phantomglied-Stellung interessante Zusammenhänge zur Schmerzwahrnehmung objektivieren: Zum Beispiel könnte ein rückläufiges Telescoping-Phänomen mit einem verminderten Phantomschmerz erstmals mit einem Befundwerkzeug erfasst, quantifiziert und statistisch nach wissenschaftlichen Kriterien ausgewertet werden.
Orthopädietechnischer Aspekt der Dokumentation
Neben der Nutzung der C.A.L.A.-Applikation von Physio- und Ergotherapeuten könnte diese Anwendung ebenfalls die Arbeit von Orthopädietechnikern, die mit der Prothesenversorgung der Amputationspatienten beauftragt sind, sinnvoll ergänzen und bereichern. In der Orthopädietechnik werden bereits standardmäßig das Vorhandensein von Phantomgefühl und ‑schmerz, Stumpfschmerz, Lokalisation, Intensität sowie evtl. Medikation in den Anamnesebögen grob handschriftlich abgefragt und erfasst.
Für frischamputierte Patienten ist die Unterscheidung von Phantomgefühl und Schmerz, die Beschreibung der Stellung des Phantomgliedes im Raum und das Erleben von Gefühls- und Schmerzsensationen in einem nicht mehr vorhandenen Körperteil anfangs verwirrend, mit Scham behaftet und oft sehr quälend. Das Amputationstrauma muss bewältigt werden, Phantomschmerzen und Gefühle beeinträchtigen ohne entsprechendes sichtbares Korrelat die Lebens- und Schlafqualität. Schmerzende Stellen können nicht einfach gezeigt und berührt werden, die gängigen Schmerzmittel und spezielle Neuroleptika helfen eingeschränkt oder gar nicht. Dazu kommt das Erlernen des Umgangs mit einer Prothese und deren Reintegration in das massiv beeinträchtigte Körperschema.
Die in C.A.L.A. erfassten Phantom- und Stumpfschmerzen können sowohl Auswahl des Prothesen-Modells als auch die Anpassung der Prothese erleichtern (Passform, Druckstellen, Funktionalität versus Schmerzempfindung). Neben Video- und Fotodokumentation des Zustands vor und nach prothetischer Versorgung ist der Einsatz von C.A.L.A. auch für fundierte Begründungen individueller, bestgeeigneter Schaft-Bettungssysteme und Passteilauswahl gegenüber den Kostenträgern denkbar.
Mit C.A.L.A. könnten den betroffenen Patienten vor allem in der frühen Phase der Prothesenversorgung sehr gut die Zusammenhänge von Prothesennutzung und Schmerzwahrnehmung aufgezeigt werden. Dies könnte zu einem höheren Grad an Patienten-Adhärenz in der Prothesennutzung, einem verbesserten Embodiment der Prothese, einer Reduktion der Phantomschmerz-Beschwerden und letztlich einem höheren Maß an Lebensqualität beitragen.
Evaluierung der Funktionen und Anwenderfreundlichkeit von C.A.L.A.
Ein Prototyp von C.A.L.A. wurde im Rahmen einer Studie mit 33 Physio- und Ergotherapeuten und Orthopädietechnikern in Bezug auf Benutzerfreundlichkeit und Funktionsumfang evaluiert. Alle Teilnehmer mussten zwei vorgegebene Fälle fiktiver Patienten in C.A.L.A. dokumentieren und wurden danach befragt. Die funktionale Abdeckung des Prototyps wurde anhand von 22 Amputierten evaluiert, deren Amputationen mit C.A.L.A. dokumentiert wurden 19.
Die Benutzerfreundlichkeit, auf die bereits bei der Entwicklung des Prototyps viel Wert gelegt wurde, bewerteten die Befragten anhand des SUS (System Usability Scale)-Fragebogens 20 mit durchschnittlich 81 Prozent. Somit repräsentiert das Ergebnis eine hohe Benutzerfreundlichkeit. Aus den semistrukturierten Interviews mit den Teilnehmern konnten auch konkrete Anforderungen zur Erweiterung des Funktionsumfanges erhoben werden wie z. B. die detaillierte Modellierung der einzelnen Finger und Zehen, eine visuelle Unterscheidung von Phantom und Stumpf und eine umfangreichere Erfassung von Empfindungen und Schmerzen.
Limitierungen
Das komplexe Phänomen des Phantomschmerzes nach Extremitäten-Amputationen ist von multiplen individuellen Aspekten (z. B. Amputationsniveau, Schmerzen vor der Operation, emotionale Bewältigung, psychische Grundstimmung, soziale Belastungskomponenten) abhängig und wird von vielen Faktoren in der Nachbehandlung moduliert (u. a. Prothesenversorgung und ‑nutzungsfrequenz, Zeitraum nach der Amputation, individuell wirksame Therapiemethoden). Mit C.A.L.A. lassen sich nicht alle diese Einflussfaktoren detailliert erfassen und abbilden, doch die Applikation wird stetig weiterentwickelt, um sich dem Bedarf der Nutzer und Patienten anzupassen. Die bisher erhobenen Daten mit C.A.L.A.-Patienten lassen zwar Korrelationen erahnen, aber ermöglichen noch keine eindeutigen Aussagen über signifikante Zusammenhänge zur Phantomschmerz-Entwicklung im Therapieverlauf unter Einsatz spezifischer Behandlungsmethoden oder Schaftversorgungen. Um diese noch große wissenschaftliche Lücke zum Verständnis des Phantomschmerzes zu schließen, streben wir in den nächsten Jahren den Aufbau einer umfangreichen anonymisierten Patientendatenbank auf der Basis einer multizentrischen Nutzung der C.A.L.A.-Applikation an. Idealerweise können mit entsprechenden Datenbankeinträgen einige der oben angesprochenen Faktoren konkretisiert werden, sodass eine noch gezieltere Therapie für betroffene Patienten mit Phantomschmerzen möglich ist.
Fazit und Ausblick
C.A.L.A. (Computer Assisted Limb Assessment) ist eine Anwendung, die die Dokumentation und Visualisierung von Phantomempfindungen und ‑schmerz sowie die Quantifizierung des sichtbaren und unsichtbaren Körperbildes von Patienten ermöglicht. Darüber hinaus kann es aufgrund der Modularität der Funktionen zur Dokumentation weiterer Patientenkohorten eingesetzt werden, wie bei CRPS oder neuropathischen Beschwerden. Da derzeit viele handschriftlich auf Bodycharts erfasste Pathologien nicht digitalisiert werden, ermöglicht C.A.L.A. eine dauerhaft verfügbare und jederzeit auch später abrufbare digitale Alternative. C.A.L.A. kann als deskriptive und quantifizierende Dokumentationsmethode verwendet werden; die Visualisierung des Körperbildes kann dabei helfen, die Lücke zwischen der Wahrnehmung des Patienten und der Vorstellung des Anwenders zu schließen und den weiteren Behandlungsverlauf beeinflussen.
Interessenskonflikt
Die Autoren haben keine Interessenskonflikte.
Für die Autoren:
Dr. Cosima Prahm, Msc BA
BG Klinik Tübingen
Schnarrenbergstr. 95
72076 Tübingen
cosima.prahm@med.uni-tuebingen.de
www.playbionic.org
Begutachteter Beitrag/reviewed paper
1 BG Unfallklinik Tübingen, Klinik für Hand‑, Plastische, Rekonstruktive und Verbrennungschirurgie, Universität Tübingen
2 Orthopädie Brillinger GmbH & Co. KG, Tübingen
Prahm C, Merk J, Wrede S, Kolbenschlag J, Bressler M. C.A.L.A.: Ein Software-Tool zur digitalen Erfassung, Visualisierung und Dokumentation des Körperbildes von Amputierten. Orthopädie Technik, 2023; 74 (2): 36–40
- Die orthopädietechnische Versorgung mit einer dynamischen Fingerstreckorthese als eigenständige Therapie bei der Dupuytren’schen Kontraktur — 26. März 2026
- Vergleichende Prüfung konventioneller und additiv gefertigter Prothesenschäfte in Anlehnung an DIN EN ISO 10328:2016 — 10. März 2026
- Easypreg – ein Faserverbundwerkstoff zum Tiefziehen — 9. März 2026
- Jensen T. S., Krebs B., Nielsen J., Rasmussen P. Non-painful phantom limb phenomena in amputees: incidence, clinical characterstics and temporal course. Acta Neurologica Scandinavica 1984; 70 (6): 407–414. doi: 10.1111/j.1600–0404.1984.tb00845.x
- Flor H. Phantom-limb pain: Characteristics, causes, and treatment. Lancet Neurology 2002; 1(3): 182–189
- Richardson C., Kulkarni J. A review of the management of phantom limb pain: challenges and solutions. Journal of Pain Research 2017; 10: 1861–1870. doi: 10.2147/jpr.s124664
- Collins K. L. et al. A review of current theories and treatments for phantom limb pain. The Journal of clinical Investigation 2018; 128 (6): 2168–2176
- Flor H. Phantom-limb pain: Characteristics, causes, and treatment. Lancet Neurology 2002; 1(3): 182–189
- Aternali A., Katz J. Recent advances in understanding and managing phantom limb pain. F1000Research 2019; 8: 1167. doi: 10.12688/f1000research.19355.1
- Collins K. L. et al. A review of current theories and treatments for phantom limb pain. The Journal of clinical Investigation 2018; 128 (6): 2168–2176
- Flor H., Nikolajsen L., Jensen, T. S. Phantom limb pain: A case of maladaptive CNS plasticity? Nature Reviews Neuroscience 2006; 7 (11): 873–881. doi: 10.1038/nrn1991
- Kern U., Busch V., Rockland M., Kohl M., Birklein F. Prävalenz und Risikofaktoren von Phantomschmerzen und Phantomwahrnehmungen in Deutschland. Der Schmerz 2009; 23 (5): 479–488. doi: 10.1007/s00482-009‑0786‑5
- Bekrater-Bodmann, R. Perceptual correlates of successful body—prosthesis interaction in lower limb amputees: psychometric characterisation and development of the Prosthesis Embodiment Scale. Scientific Reports 2020; 10 (1): 14203. doi: 10.1038/s41598-020–70828‑y
- Flor H., Nikolajsen L., Jensen, T. S. Phantom limb pain: A case of maladaptive CNS plasticity? Nature Reviews Neuroscience 2006; 7 (11): 873–881. doi: 10.1038/nrn1991
- Kehl I., Bekrater-Bodmann R. Prothesenverkörperung und Phantomschmerz, Orthopädie Technik 2021; 72 (5): 44–48
- Melzack, R. The McGill Pain Questionnaire: Major properties and scoring methods. Pain 1975; 1 (3): 277–299
- Flor H., Nikolajsen L., Jensen, T. S. Phantom limb pain: A case of maladaptive CNS plasticity? Nature Reviews Neuroscience 2006; 7 (11): 873–881. doi: 10.1038/nrn1991
- Crawford C. S. From pleasure to pain: The role of the MPQ in the language of phantom limb pain. Social Sciene & Medizine 2009; 69 (5): 655–661. doi: 10.1016/j.socscimed.2009.02.022
- Shaballout N., Aloumar A., Neubert T. A., Dusch M., Beissner F. Digital Pain Drawings Can Improve Doctors’ Understanding of Acute Pain Patients: Survey and Pain Drawing Analysis. JMIR Mhealth Uhealth 2019; 21 (1): e11412. doi: 10.2196/11412
- F. Spyridonis F, Ghinea G. 2D vs. 3D pain visualization: User preferences in a spinal cord injury cohort. In: Marcus A. (Hrsg.). Design, User Experience, and Usability. Theory, Methods, Tools and Practice. DUXU 2011. Lecture Notes in Computer Science 6769. Berlin, Heidelberg: Springer, 2011. doi: 10.1007/978–3‑642–21675-6_37
- Alcañiz M. et al. A New Realistic 3D Body Representation in Virtual Environments for the Treatment of Disturbed Body Image in Eating Disorders. CyberPsychology & Behavior 2000; 3 (3): 433–439
- Bressler M. et al. Visualizing the Unseen: Illustrating and Documenting Phantom Limb Sensations and Phantom Limb Pain With C.A.L.A. Frontiers in Rehabilitation Sciences 2022; 3: 1–11
- Bangor, A., Kortum P. T., Miller J. T. An Empirical Evaluation of the System Usability Scale. International Journal of Human-Computer Interaction 2008; 24 (6): 574–594