Schmerz am Stumpf
Bei Stumpfschmerzen können verschiedene Quellen unterschieden werden: einerseits Druckprobleme und Schmerzen durch mangelnde Weichteilbedeckung des Knochens, ungünstige Form oder Länge insbesondere bei prothetischer Versorgung. Hier kommt es bspw. nach einer gewissen Zeit des Tragens einer Prothese zu Hautreaktionen, Schmerzen oder sogar Ulzerationen.
Andererseits gibt es von Nerven ausgehende Schmerzen, die einen völlig anderen Charakter haben: Es kommt zu einer extremen Berührungsüberempfindlichkeit, Brennen, Elektrisieren. Diese typischen „neuropathischen” Beschwerden weisen auf Probleme an den angeschnittenen Hautnerven hin. Diese enden im Bereich der Narbe. Nach dem Anschneiden kommt es immer zu einem Regenerationsversuch des Nervs. Die Nervenfasern sprossen aus. Da sie kein Gegenstück finden, kommt es zur Bildung einer keuligen Auftreibung aus dem Nervenende, dem sogenannten Neurom. Das Neurom verursacht besonders große Schmerzen, wenn es oberflächlich liegt und Druck ausgesetzt ist. Ein Stumpf mit dieser Art Beschwerden ist prothetisch schwierig versorgbar.
Obwohl bei jeder Amputation wie auch bei jeder anderen Art von Operation zahlreiche kleine und kleinste Hautnerven angeschnitten werden müssen, die nicht einzeln, wie unten geschildert, versorgt werden können, kommt es erstaunlicherweise in den meisten Fällen nicht zur Bildung eines schmerzhaften Neuroms. Neuromschmerzen können durch weiter proximal liegende Schäden, bspw. durch Nervenkompression, verschlimmert werden. Die Behandlung solcher Nervenkompressionen führt zur Verminderung der Neuromschmerzen 1. Daher wird auf Nervenkompressionen am Bein in diesem Artikel noch näher eingegangen.
Phantomschmerz
Ein Schmerz, der in ein nicht mehr vorhandenes Körpergebiet ausstrahlt, wird als bedrohlich empfunden, da keine gewohnten Schmerzreaktionen mit lokalen Maßnahmen wie Hinfassen, Reiben, Massieren, Kühlen etc. möglich sind. Dazu kommt der neuropathische Charakter, der besonders quälend ist. Diese Schmerzen gehen von langen, weiter nach distal reichenden, tiefliegenden Nerven aus, die durchtrennt wurden. Im Nervenende entstehen die schmerzhaften Signale, die vom Bewusstsein in der Region empfunden werden, für die der Nerv zuständig war.
Diagnostik
Klinische Untersuchung
Zunächst erfolgt die Abgrenzung zwischen Druckproblematik und von Nerven ausgehenden neuropathischen Beschwerden. Die Stumpfschmerzen werden genau lokalisiert und markiert. Die Neurome in der Haut werden den einzelnen Hautnerven zugeordnet. Durch Beklopfen der Haut nach proximal wandernd wird der proximalste Punkt ermittelt, an dem man ein Elektrisieren in das schmerzhafte Gebiet auslösen kann. Damit stellt man den Nerv dar, der in der Narbe des Stumpfes im schmerzhaften Neurom endet. Bei Phantomschmerzen erfolgt über die genaue Beschreibung des Empfindungsortes die Zuordnung zu den auslösenden Nerven. Mit diesem Wissen wird versucht, einen Auslösepunkt zu finden.
Da Nervenkompressionen zusätzliche Beschwerden auslösen und möglicherweise die Neuromproblematik verstärken können, wird auch danach gesucht. Zunächst werden die Engpassstellen am nicht betroffenen Bein untersucht. Obwohl dort keine Beschwerden bestehen, lassen sich häufig leichte Nervenkompressionen über die Druckempfindlichkeit an den Engstellen aufspüren. Die gleiche Untersuchung wird am betroffenen Bein durchgeführt und überprüft, ob Neuromverteilung oder Phantomschmerzen mit möglicherweise komprimierten Nerven zusammenpassen.
Obwohl die untere Extremität nicht wesentlich anders aufgebaut ist als die obere und zudem noch lebenslänglich durch das Körpergewicht belastet wird, werden Nervenkompressionssyndrome hier erstaunlicherweise als Raritäten eingestuft und sind wenig bekannt. Tunnel und Engstellen seien nicht vorstellbar 2. Aus Sicht des Autors sind die bekannten und weniger bekannten Kompressionsstellen wesentlich häufiger relevant als Ursache für neuropathische Symptome wie Schmerzen, Brennen, Kribbeln, Elektrisieren, Pelzigkeit, Taubheit, Verstärkung des Schweregrades beim Restless-Legs-Syndrom, Gangunsicherheit durch Schwanken (Taubheit der Fußsohle) oder Stolpern (Zehenheberschwäche) und ein Kofaktor bei der Bildung von Ulzerationen beim Diabetischen Fußsyndrom, wie es auch von Dellon beschrieben wurde 3.
Daher werden im Folgenden kursorisch die Prädilektionsstellen vorgestellt:
N. cutaneus femoris lateralis
Die Kompression dieses Nervs führt zur sogenannten Meralgie. Der Nerv tritt normalerweise unter dem Leistenband direkt medial der Spina iliaca anterior superior aus. Problematisch ist ein starker Richtungswechsel aus der Horizontalen im kleinen Becken in die Senkrechte auf den Oberschenkel. An dieser Knickstelle liegt der Nerv auf einer Schwelle durch die dicke Faszie des M. iliacus. Gleichzeitig drückt von cranial her das Leistenband den Nerv auf diese Schwelle 4. Bei Varianten kann es zu einem sehr weit medial liegenden Austritt mit entsprechenden mehrfachen Umlenkungen kommen. Hier ist eine Beteiligung bei chronischen Leistenschmerzen durch Schwellung nach Herniotomie möglich.
Neuropathische Symptome: Oberschenkel Vorder- und Außenseite (Abb. 1 u. 2)
N. saphenus
Dieser Nerv kann im Adductorenkanal eingeengt sein. Auch distal des Kanals können einzelne Faszienstreifen Schnürfurchen verursachen. Kompression bringen sowohl die Faszie des M. vastus medialis ventral als auch die zum Teil bereits sehnige Faszienplatte des M. adductor magnus. An gleicher Stelle ist auch die Kompression des R. muscularis n. femoralis unter der Faszie des Vastus medialis möglich (mögliche Beteiligung an Zuckungen beim RLS). Medial oberhalb des Knies kann der Durchtritt des N. saphenus und seines Astes (Ramus infrapatellaris) durch die Faszie problematisch sein.
Neuropathische Symptome: mediales Knie, Schienbein, medialer Unterschenkel, medialer Fußrand (Abb. 3)
N. tibialis
Die proximale Tibialiskompression unter der Soleusschlinge (Arcus tendinosus) direkt unterhalb der Kniekehle wurde anatomisch erst 2009 untersucht 5. 2012 erschien die erste Veröffentlichung klinischer Fälle 6 (Abb. 4). Unter den beschriebenen Fällen waren auch Versager nach Tarsaltunnel-Dekompression. Die distale Kompression, der sog. Tarsaltunnel (TTS), muss nach Dellon 7 eigentlich als 4 tarsale Tunnel verstanden und entsprechend operiert werden. Die alleinige Spaltung des Retinaculum flexorum reicht nicht aus. Es müssen neben den Calcaneusästen auch die Tunnel für N. plantaris medialis und lateralis weit in die Sohle hinein eröffnet werden, und zwar mit Exzision des zwischen den beiden Tunneln liegenden Septums.
Neuropathische Symptome: Wade, Ferse, Fußsohle (proximale Kompression) bzw. Ferse, Fußsohle (TTS), Zehenunterseite
N. peroneus communis, peroneus superficialis, peroneus profundus
Der Peroneus communis kann durch die Bizepssehne bedrängt, von strammen Faszien gegen den Fibulakopf gedrückt werden oder direkt über den Kopf verlaufen. Kritisch ist der Eintritt in die Muskulatur unter demM. peroneus longus (dorsal). Zieht sich dessen Faszie über die Außenseite hinaus in den Spalt zwischen die Muskulatur, kann hier eine Schnürung entstehen (Abb. 5). Je nach Verlauf des Nervs kann eine Kompression gegen den Hals der Fibula auftreten. Der Superficialis kann oberhalb vom Außenknöchel beim Fasziendurchtritt oder jenseits des Durchtrittes durch quer verlaufende Faszienzüge abgeschnürt werden (Abb. 6). Cranial davon ist ein langer subfaszialer Verlauf meist am Septum entlang ungünstiger als ein langer Verlauf zwischen den Muskeln. Der Profundus ist in der Tat selten symptomatisch unter dem Retinaculum extensorum (seltenes sog. vorderes Tarsaltunnel-Syndrom) als vielmehr distal der MT-Basen I/II, wo er von der Sehne des M. extensor hallucis brevis überkreuzt wird 8. Unter den knapp 2000 vom Autor dekomprimierten Nerven an der unteren Extremität finden sich hier am Profundus die stärksten makroskopisch sichtbaren Zerquetschungen (Abb. 7).
Neuropathische Symptome: Unterschenkel Außenseite, Sprunggelenk außen, Fußrücken, Zehenoberseite
N. suralis
Ähnlich wie beim Peroneus superficialis kann sowohl ein Fasziendurchtritt in Wadenmitte als auch ein langer „ungepolsterter” Verlauf subfaszial zwischen dem Übergang zur Achillessehne und der Faszie problematisch sein.
Nn. digitales plantares
Diese Endäste aus N. tibialis, dann N. plantaris medialis und lateralis werden z. B. bei Senk-Spreizfuß zwischen den Metatarsaleköpfchen gequetscht und von Bändern in belasteten Zonen gehalten. Sie verursachen die Metatarsalgie (z. B. Morton-Pseudoneurom), die zwischen allen Metatarsalia auftreten kann 9.
Unter Umständen kann eine Messung der Berührungsempfindlichkeit (Berührungsschwellen) mit einem speziellen Sensibilitätstestgerät (Pressure-Specified Sensory DeviceTM, PSSD, Abb. 8) noch mehr Informationen über den Zustand der Nerven erbringen.
Diagnostische Betäubung
Nachdem Neurome, Hautnerven, Auslösepunkte für Phantomschmerzen und Nervenkompressionspunkte lokalisiert sind, wird durch gezielte Einspritzungen örtlicher Betäubung versucht, eine deutliche Schmerzreduktion zu erreichen. Dabei wird nicht am Neurom in der Narbe eingespritzt, sondern weiter proximal versucht, den zuständigen Nerv auszuschalten (Nervenblock).
Therapie
Ist es nach einem oder mehreren Nervenblöcken zu einer deutlichen Besserung der Beschwerden gekommen, gibt es noch konservative Möglichkeiten. Schmerztherapeuten versuchen mit wiederholten Nervenblöcken das Schmerzniveau zu senken. Gelingt dies nicht dauerhaft, kommt abhängig vom allgemeinen Gesundheitszustand eine operative Behandlung in Frage.
Oft wird versucht, ein Neurom durch direktes Ausschneiden in der Narbe zu behandeln. Meist kann ein Neurom im Narbengewebe aber nicht dargestellt werden. Die Operation führt zwar zu einer kurzzeitigen Besserung der Situation; wie oben geschildert kommt es zur Nervenregeneration, die im Unterhautgewebe besonders stark ist. Es kann sich aber erneut ein Neurom in der Narbe bilden, am selben Ort mit derselben Problematik. Zudem befindet sich im alten Narbengebiet nun eine neue Narbe, nicht selten in der Belastungszone. Nach ursprünglich problematischer Wundheilung am Stumpf ist ein solcher Eingriff sehr risikoreich.
Vielmehr sollten die für die Neurome und Phantomschmerzen zuständigen Nerven weiter proximal aufgesucht werden. Dort werden sie durchtrennt und die Nervenstümpfe speziell versorgt, indem sie in die Muskulatur versenkt werden. Damit wird das empfindliche Nervenende in die Tiefe gelegt. Des Weiteren hat das Nervenende im Muskel weniger Aussprossungen.
Zusätzlich werden etwaig vorhandene Nervenkompressionen durch Nervenentlastung behandelt, was der Behandlung eines Karpaltunnelsyndroms am Handgelenk entspricht.
Fallbeispiel
Bei einer 50-jährigen Patientin wird im Februar 2011 wegen einer Durchblutungsstörung am linken Bein eine operative Gefäßsäuberung mit anschließender Stent-Einlage durchgeführt. Im Mai erfolgt nach kritischer Durchblutungsminderung eine Unterschenkel-Amputation mit anschließender Wundheilungsstörung. Die Diagnose: Panarteriitis nodosa, eine entzündliche Veränderung der Gefäßwände, die zum Gefäßverschluss führt. Im November 2011 erfolgen eine Vakuumtherapie (VAC) sowie eine Kniegelenksexartikulation mit erneuter Wundheilungsstörung; eine Wundreinigung wird vorgenommen.
Im August wird eine Oberschenkel-Amputation durchgeführt; wiederum ergibt sich eine Wundheilungsstörung, die per VAC behandelt wird. Im September 2011 wird der Oberschenkel-Stumpf gekürzt, nach erneuter Wundheilungsstörung erfolgt die Abheilung.
Die Patientin wird am 13. Juli 2012 aus der Schmerztherapie beim Autor vorgestellt. Sie hat seit einem Jahr stärkste Schmerzen und ist mit multiplen stärksten Schmerzmedikamenten (Opioiden) versorgt. Eine prothetische Versorgung ist wegen chronischen Stumpf- und Phantomschmerzes nicht möglich; die Patientin sitzt im Rollstuhl und hat an Gewicht zugenommen.
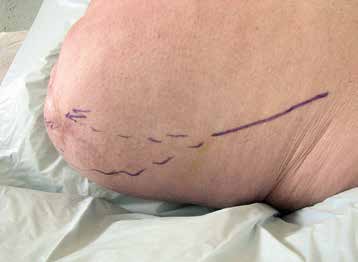
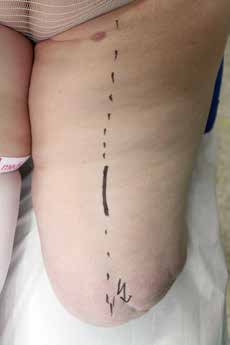
Bei der klinischen Untersuchung wird eine leicht überpigmentierte Narbenumgebung nach Wundheilungsstörungen festgestellt, des Weiteren starker Stumpfschmerz mit Neuromschmerz an der Narbe innen und unten. Die Patientin klagt über Phantomschmerzen wie „Feuergarben” in die Wade innen und Schmerzen in die Großzehe, zudem über Druckschmerz an Engstellen des Nervus saphenus im Adduktorenschlitz und an der Beinrückseite.
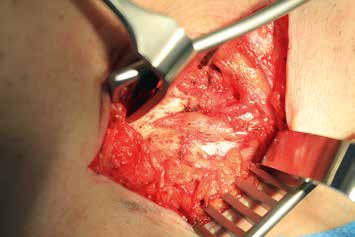
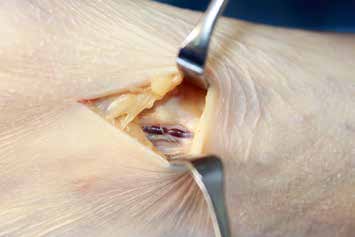
Damit lassen sich die Beschwerden zwei Nerven zuordnen: Es zeigen sich mehrere Neurome im Versorgungsgebiet des Nervus saphenus. Die Feuergarben in die mediale Wade entsprechen ebenfalls dem Versorgungsgebiet des N. saphenus. Derselbe Nerv ist weiter proximal im Adduktorenschlitz eingeengt. Weiter mittig am Stumpf bestehende Schmerzen von „unten” sowie die Phantomschmerzen in die Großzehe entsprechen dem N. ischiadicus. Es erfolgt der Nervenblock ca. 12 cm proximal des Stumpfes am N. saphenus. Damit ist der gesamte mediale Stumpf fast schmerzfrei (Abb. 9).
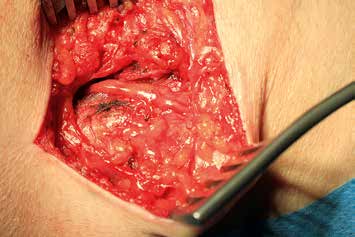
Aufgrund der Grunderkrankung mit der Gefäßerkrankung und der Vorgeschichte mit Wundheilungsstörungen wird vereinbart, zunächst nur einen Nerv zu behandeln. Es wird der für die medialen Neurome und den Waden-Phantomschmerz zuständige N. saphenus am Adduktorenschlitz dekomprimiert, verfolgt und distal abgesetzt. Der Nerv wird mit seinen Ästen in Muskulatur gepflanzt.
Anschließend erfolgt eine sofortige deutliche Schmerzminderung am Stumpf (70 %) sowie eine Reduktion des Phantomschmerzes in die Wade um 90 %. Die Wundheilung verläuft komplikationslos.
Nach 4 Monaten herrscht weiterhin ein stabiles Ergebnis. Interessanterweise ist aber in der Schmerzwahrnehmung der Patientin der verbliebene Schmerz aus dem Ischias-Bereich in den Vordergrund gerückt. Im ausführlichen Gespräch kann jedoch das Erreichte bestätigt und ins Bewusstsein gerückt werden.
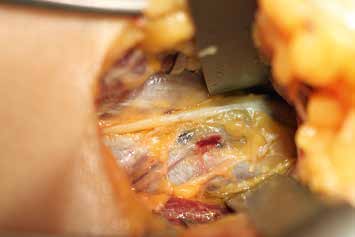
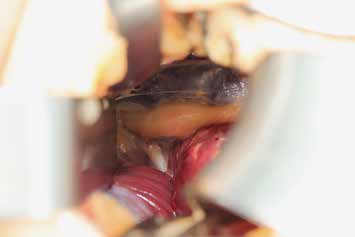
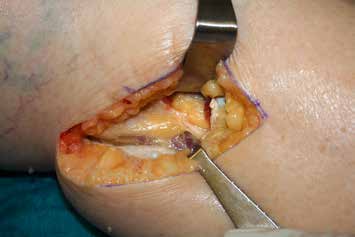
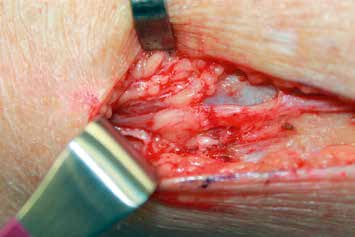
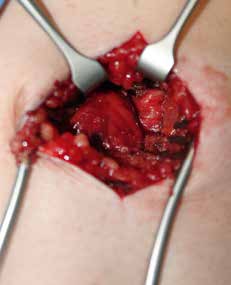
Es erfolgt eine Blockade des Ischias, die erneut eine Besserung im Zuständigkeitsbereich erbringt. Eine entsprechende Operation am Ischiadicus auf der Oberschenkelrückseite (Abb. 10) mit Herauslösen des Nervs aus der Narbe und Versenken in die Muskulatur (Abb. 11) führt zu weiterer Verbesserung der Berührungsempfindlichkeit am Stumpf. Zudem ergibt sich eine leichte Reduktion des Phantomschmerzes in die Großzehe. Das Ergebnis am Saphenus bleibt weiter stabil. Eine Reduktion der Schmerzmedikation ist dennoch nicht möglich. Insgesamt ist eine deutliche Schmerzreduktion erreicht worden; die Patientin kann nun mit einer Prothese versorgt werden.
Zusammenfassung
Bei Schmerzen nach Amputationen ist eine genaue Analyse des Schmerzcharakters und der Lokalisation notwendig. Mit einer entsprechenden klinischen Untersuchung erfolgt die Zuordnung der Beschwerden zu den jeweiligen Nerven, mit deren Blockade ermittelt wird, ob eine operative Herangehensweise erfolgversprechend ist. Das Fallbeispiel zeigt ein schrittweises Vorgehen, das zu einer deutlichen Verbesserung der Situation geführt hat. Es zeigt aber auch die Komplexität der Schmerzwahrnehmung auf, die auch im Zusammenhang mit dem erlittenen Schicksal und dem veränderten Körpergefühl gesehen werden muss.
Der Autor:
Dr. Martin Raghunath
Praxiszentrum Adickesallee Frankfurt
Adickesallee 51–53,
60322 Frankfurt
Arabella Klinik München
Arabellastraße 5, 81925 München
neurag@hotmail.de
Begutachteter Beitrag/Reviewed paper
Raghunath M. Diagnostik und therapeutisches Vorgehen bei Phantom- und Stumpfschmerz. Orthopädie Technik, 2014; 65 (3): 26–31
- Gips oder Orthese bei distalen Radiusfrakturen? — 8. April 2026
- Die orthopädietechnische Versorgung mit einer dynamischen Fingerstreckorthese als eigenständige Therapie bei der Dupuytren’schen Kontraktur — 26. März 2026
- Vergleichende Prüfung konventioneller und additiv gefertigter Prothesenschäfte in Anlehnung an DIN EN ISO 10328:2016 — 10. März 2026
- Wilhelm, A. Schmerzzustände im Bereich der oberen Extremitäten und ihre Behandlung. Chirurg, 1973; 44: 249–254
- Reiners, K. Internationaler Postgraduate Course Diabetic Foot, Rheine, persönliche Kommunikation
- Dellon, AL. The four medial ankle tunnels: A critical review of perceptions of tarsal tunnel syndrome and neuropathy. Neurosurg Clin N Amer, 2008; 19: 629–648
- Aszmann OC, Dellon ES, Dellon AL. Anatomical course of the lateral femoral cutaneous nerve and its susceptibility to compression and injury. Plast Reconstr Surg, 1997; 100: 600–604
- Williams EH, Williams CG, Rosson GD et al. Anatomic site for proximal tibial nerve compression: a cadaver study. Ann Plast Surg, 2009; 62: 322–325
- Williams EH, Rosson GD, Hagan RR et al. Soleal sling syndrome (proximal tibial nerve compression): results of surgical decompression. Plast Reconstr Surg, 2012; 129 (2): 454–462
- Dellon, AL. The four medial ankle tunnels: A critical review of perceptions of tarsal tunnel syndrome and neuropathy. Neurosurg Clin N Amer, 2008; 19: 629–648
- Dellon AL. Deep peroneal nerve entrapment on the dorsum of the foot. Foot Ankle, 1990; 11: 73–80
- Larson EE, Barrett SL, Battiston B et al. Accurate nomenclature for forefoot nerve entrapment, J Am Podiatr Med Assoc, 2005; 95: 298–305