Vorrangig geben das Sturzrisiko und die Anfälligkeit gegenüber einer Gewebebeschädigung am Stumpf Anlass zur Sorge. Die verordnete Prothesentechnologie muss die Bedürfnisse dieser spezifischen demografischen Anwendergruppe berücksichtigen. Eine geeignete Kombination von Prothesentechnologie für ältere, dysvaskuläre Amputierte bestehend aus Prothesenfuß, Verbindungssystem und Linerkonzeption kann Veränderungen bewirken, die sich für ältere, vaskuläre Amputierte als vorteilhaft erweisen.
Einleitung
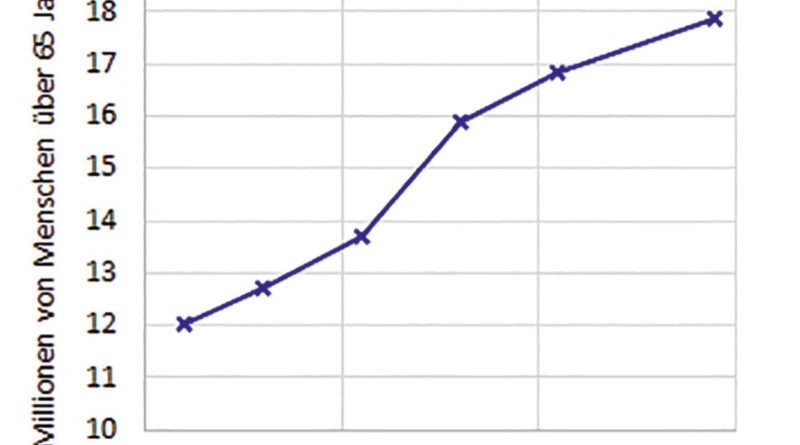
Wie die meisten Industrieländer weist auch Deutschland eine alternde Bevölkerung auf: Im Zeitraum von 1992 bis 2019 stieg der Anteil der Deutschen über 65 Jahre von 15 auf 22 % 1 (Abb. 1). Mehr ältere Menschen bewirken eine größere Belastung des Gesundheitswesens. Bei Gefäßerkrankungen und Diabetes besteht unter älteren Menschen eine erhöhte Prävalenz; sie sind zudem die Hauptursachen für Amputationen. Fünfundsiebzig Prozent aller Amputationen werden an Menschen über 65 Jahre vorgenommen, neunzig Prozent von ihnen weisen eine vaskuläre Ätiologie auf 2. Für das Design effektiver Prothesenkomponenten für ältere Amputierte ist es daher zwingend erforderlich, die sich verändernden biomechanischen Anforderungen älterer Menschen sowie die Auswirkungen der Disvaskularität auf Haut und Weichgewebe zu verstehen.
Biomechanische Anforderungen älterer Menschen
Mit zunehmendem Alter ändern sich die biomechanischen Anforderungen des Menschen 3: Die Beinmuskulatur wird schwächer und kann weniger Kraft erzeugen, was typischerweise einen verringerten Bewegungsradius der Gelenke, eine kürzere Schrittlänge, eine geringere Gehgeschwindigkeit und eine größere Variabilität im Gangbild bedingt. All diese Faktoren sind nachweislich mit einem erhöhten Sturzrisiko verbunden 4. Es ist aber nicht nur die Variabilität des Gangbildes, die das Sturzrisiko bei älteren Menschen erhöht: Geschwächte Muskeln, eine verminderte Sehkraft und eingeschränkte kognitive Fähigkeiten können ebenfalls dazu beitragen, ebenso einige Medikamente, die für ihre gleichgewichtsbeeinträchtigende Wirkung bekannt sind 5. All diese Faktoren werden durch die Amputation und den Verlust von sensorischer Rückmeldung und funktionaler Gelenkkontrolle verstärkt. Obwohl Stürze bei Amputierten allgemein häufig vorkommen, haben Studien gezeigt, dass bei älteren Amputierten ein erhöhtes Sturzrisiko besteht6.
Dysvaskuläre Amputationen
Bei gesunder Funktion strömt Blut durch den Körper, versorgt die Extremitäten mit Sauerstoff und Nährstoffen und entfernt Abfallstoffe. Bei Menschen mit Dysvaskularität ist die Durchblutung eingeschränkt, was bedeutet, dass nicht nur weniger Nährstoffe zugeführt werden, sondern auch, dass sich Abfallstoffe an der Arterienwand anzusammeln beginnen. Haut und Weichgewebe sind anfälliger gegen Schädigungen und Verletzungen; Durchblutungsstörungen haben zur Folge, dass das Gewebe mehr Zeit benötigt, um zu heilen7. Zeigt ein Patient zudem eine periphere Neuropathie oder Gefühlsstörungen in den Extremitäten, so können aus Hautverletzungen schnell schwerwiegendere Verletzungen werden, und es kann zu einer Infektion kommen, noch bevor sie sich feststellen lässt.
Nach der Amputation sind Haut und Weichgewebe des Stumpfes aufgrund der Narbenbildung und der zugrunde liegenden Probleme mit der Gewebeheilung anfällig, sodass eine erhöhte Wahrscheinlichkeit der Bildung von Dekubitalgeschwüren besteht. Studien zufolge ist bei 60,7 % der diabetesbedingt Amputierten innerhalb von fünf Jahren nach der Erstamputation eine zweite, höhere oder eine kontralaterale Amputation erforderlich 8.
Prothesendesign
Beim Prothesendesign ist es wichtig, die Anforderungen verschiedener demografischer Anwendergruppen zu berücksichtigen, damit die Prothesen adäquat an ihre spezifischen Mobilitäts- und gesundheitlichen Bedürfnisse angepasst sind. Bei älteren, vaskulären Amputierten steht die Verbesserung von Gangqualität und ‑komfort bei gleichzeitiger Verringerung des Sturzrisikos im Alltag und einem Schutz des verletzlichen Stumpfes im Mittelpunkt. In diesem Zusammenhang können Hydraulikknöchel eine Lösung bieten: Diese Technologie weist zahlreiche bewährte Vorteile für die genannte Altersgruppe auf 9 10 11.
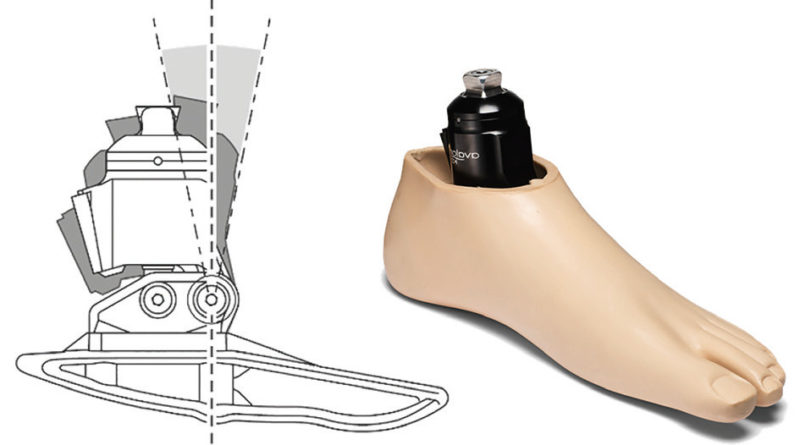
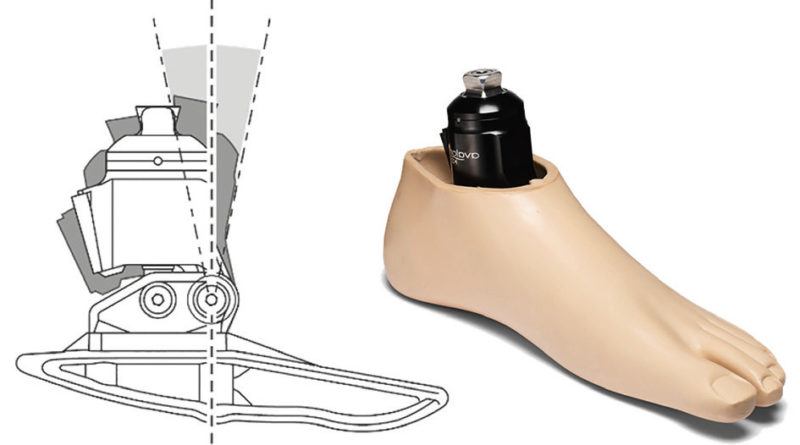
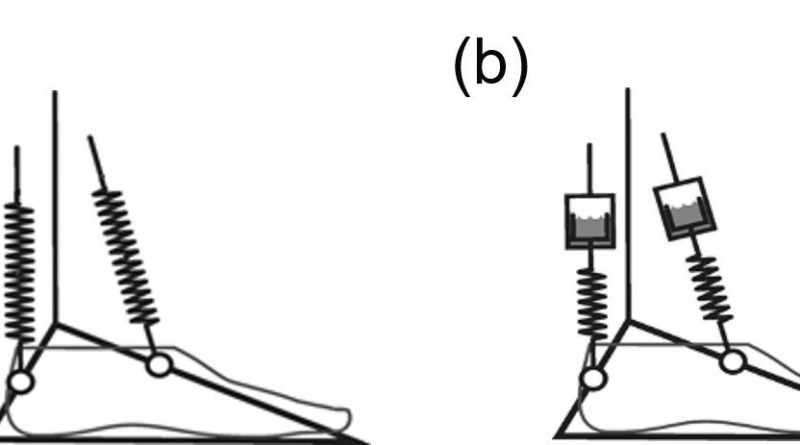
Der Aufbau einer geeigneten Prothese ist darauf ausgerichtet, den Körperschwerpunkt des Anwenders in Relation zu den Gelenken der unteren Extremitäten so zu platzieren, dass die Muskelkraft, die zur Aufrechterhaltung eines stabilen Standes und des Gleichgewichts des Anwenders erforderlich ist, minimiert wird. Gelenklose Carbonfederprothesenfüße verhalten sich elastisch und nutzen die Verformung der Carbonfedern, um eine Dorsalflexion und eine Plantarflexion zu erzielen. Das Problem bei einem solchen Konstruktionsansatz besteht allerdings darin, dass bei elastischer Bewegung der Prothese zur Krafterzeugung beim Gehen stets ein bestimmter Ausgangspunkt vorhanden ist, zu dem die Prothese bei Entlastung zurückkehrt (Abb. 2). Dies gestattet z. B. keine Anpassung an einen geneigten Untergrund, ohne dass dazu Ausgleichsbewegungen wie z. B. eine Beugung des Knies erforderlich sind. Bei dieser Bewegung wird die Position des Körperschwerpunkts des Anwenders in Relation zur Kniegelenkmitte verändert. Infolgedessen hat sich die Ausrichtung verändert, was eine erhöhte Muskelbeanspruchung und ein verringertes Gleichgewicht zur Folge hat. Hydraulikknöchelgelenke ermöglichen bis zu 12 Grad an viskoelastisch gedämpfter Knöchelbewegung. Das bedeutet, dass der Gleichgewichtspunkt unterschiedlich sein kann, was eine „Selbstausrichtung“ auf geneigtem Untergrund gestattet. Dadurch werden Kompensationsstrategien überflüssig, und es werden eine natürliche Körperhaltung und ein verbessertes Gleichgewicht gefördert 12.
Stürze sind nicht nur eine Folge von Gleichgewichtsverlust – das Stolpern beim Gehen ist ein weiterer Faktor, der dazu beiträgt. Amputierte haben sowohl das sensorische Bewusstsein für die Fußposition als auch die funktionale Kontrolle über die dorsalen Beuger des Sprunggelenks verloren und müssen daher alternative Methoden nutzen, um eine ausreichende Bodenfreiheit zu erzielen. Für einige Patienten bedeutet dies das Vollführen von Ausgleichsbewegungen wie z. B. Vaulting („Zehenwippen“). Hydraulikknöchelgelenke erreichen das Ende ihres Dorsalflexionsbereichs am Ende der Standphase und verbleiben in der Schwungphase in dieser Position (Abb. 3). Dadurch kann die Mindestbodenfreiheit im Vergleich zu starr befestigten herkömmlichen Prothesenfüßen um 18 % erhöht 13 und die Stolperwahrscheinlichkeit reduziert werden.
Hydraulikknöchel beeinflussen zudem die auf den Stumpf einwirkende Belastung: Wenn beim Gehen der Prothesenfuß den Boden berührt, übt der Boden eine gleich große Gegenkraft (Bodenreaktionskraft) auf die Prothese aus. Diese Kraft wird über die Prothese auf den Stumpf übertragen. Die Kontrolle der an der Schnittstelle zum Boden wirkenden Kraft kann dazu beitragen, die auf den Stumpf wirkende Belastung zu verringern und auf diese Weise eine Schädigung des Stumpfes zu vermeiden. Die Plantarflexion eines Hydraulikknöchelgelenkes zu Beginn der Standphase hilft dabei, die Stoßkraft zu absorbieren und den Zeitraum zu verlängern, über den die Kraft ausgeübt wird. Das bedeutet, dass der auf den Stumpf einwirkende Druckhöchstwert im Vergleich zu starren, herkömmlichen Füßen um bis zu 81 % geringer ist14. Des Weiteren wird der Belastungswert um bis zu 87 % reduziert [12]15. Diese Veränderungen können dazu beitragen, das empfindliche Stumpfgewebe vaskulärer Amputierter zu schützen.
Der hydraulische Fuß „Avalon“
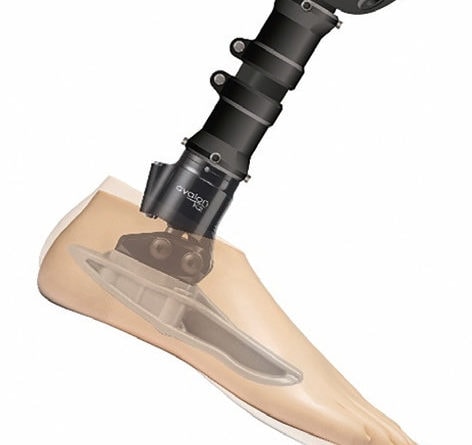
Der Avalon-Fuß (Blatchford, Basingstoke, Vereinigtes Königreich) besteht aus einem Hydraulikknöchelgelenk und einem Kunststoffinnenteil. Das hydraulische Knöchelgelenk bietet einen einstellbaren, viskoelastischen Bewegungsumfang von insgesamt 12° (6° PF und 6° DF); der speziell geformte „Kunststoffkiel“ wurde entwickelt, um ein leichteres Abrollen zu ermöglichen und den Anforderungen an Gangbild und Mobilität älterer Anwender oder von Anwendern mit geringerer Mobilität zu entsprechen (Abb. 4). Beim Gehen ermöglicht diese Kombination dem Anwender eine einfache Verlagerung seines Körperschwerpunkts über die Stützbasis hinaus nach vorn, um so die gewünschte Schrittlänge zu erzielen. Des Weiteren ermöglicht der Dorsalflexionsbereich, den Fuß einfacher nach hinten zu verlagern, um das Aufstehen von einem Stuhl zu erleichtern 16. Gehen und Aufstehen von einer Sitzgelegenheit mögen trivial erscheinen – für einen älteren Amputierten können sie die Aufrechterhaltung seiner sozialen Unabhängigkeit bedeuten.
In einer Studie aus dem Jahr 2016 wurde der Avalon-Fuß bei einseitig amputierten Anwendern der Mobilitätsklasse 2 mit einem herkömmlichen, nichthydraulischen Fußdesign verglichen 17. Bei Nutzung des Avalon-Fußes ließ sich die Asymmetrie in der Standphasendauer zwischen Prothese und gesunder Gliedmaße um durchschnittlich 34 % reduzieren (Abb. 5). Die Prothese wurde länger belastet, wodurch die Belastungszeit der gesunden Gliedmaße verringert wurde. Dieses Resultat verdeutlicht das Potenzial des getesteten Fußes hinsichtlich der Verringerung einer schädigenden Belastung der gesunden Gliedmaße. Im Rahmen einer weiteren Studie wurde ein einfacher Gehtest mit Zeiterfassung durchgeführt, um die verbesserte Mobilität von Amputierten der Mobilitätsklasse 2 mit dem Avalon-Fuß im Vergleich zu herkömmlichen Prothesenfüßen zu verdeutlichen 18. Das Resultat: Bei allen Probanden war die Gehgeschwindigkeit um durchschnittlich 6,5 % höher. Diese Verbesserungen erklären womöglich auch das Ergebnis einer weiteren Studie, bei der mit dem Avalon-Fuß eine Verbesserung des Gangs um 17,3 % und einen Anstieg der Anwenderzufriedenheit mit dem Gangbild um 21,9 % verzeichnet werden konnte, was mit Hilfe des Fragebogens zur Prothesenevaluierung (Prosthesis Evaluation Questionnaire, PEQ) zur Ergebnismessung festgestellt wurde 19.
Verbindung zwischen Stumpf und Schaft
Neben dem Prothesenfuß hat die Verbindung zwischen Stumpf und Schaft den unmittelbarsten Einfluss auf den Zustand des vaskulären Stumpfgewebes. Durch Befestigung der Prothese am Stumpf entsteht so ein zusätzliches „Gelenk“ an der unteren Gliedmaße. Dieses Gelenk kann Kraft in drei Achsrichtungen übertragen und in diese Richtungen rotieren; daher ist eine bestmögliche Verbindung sowohl zur Kontrolle als auch für einen komfortablen Sitz der Prothese unbedingt erforderlich 20 21.
Ein Vakuumsystem erzeugt durch eine luftundurchlässige Abdichtung, ein Einwegeventil am distalen Ende des Schaftes und eine mechanische Pumpe einen Unterdruck am gesamten Stumpf, der den Schaft sicher daran fixiert. Das Vakuum unterstützt zudem die Durchblutung des Stumpfes sowie die Stabilisierung des Stumpfvolumens 22 und verbessert die Sauerstoff- und Feuchtigkeitsversorgung des Gewebes 23. Somit wird die Relativbewegung zwischen Stumpf und Schaft reduziert 24 (ebenso eine damit verbundene reibungsbedingte Gewebeschädigung). Die sichere Verbindung verbessert die Prothesenkontrolle und die Eigenwahrnehmung (Propriozeption); die verbesserte Durchblutung fördert die Wundheilung am Stumpf 25.
Weitere wichtige Aspekte sind Temperatur und Feuchtigkeit an der Verbindung zwischen Stumpf und Schaft: Schweißablagerungen auf der Haut können eine Reihe von Hautproblemen nach sich ziehen 26, insbesondere dann, wenn ein Prothesenliner verwendet wird. Perforierte Liner wurden entwickelt, um eine Ableitung des Schweißes von der Haut zu ermöglichen und ein trockenes Stumpfklima zu schaffen 27. Durch die Ableitung des Schweißes von der Hautoberfläche wird das Risiko einer Hauterweichung und ‑mazeration gesenkt. Ein trockenerer Verbindungsbereich verbessert das Mikroklima und reduziert so Faktoren, die das Wachstum und die Ausbreitung von Bakterien im Schaft anregen. Dies kann sich aktiv auf die Förderung der Heilung und die Verbesserung des Gewebezustands auswirken 28. Die Kombination aus erhöhtem Vakuum und perforiertem Liner hat noch weitere Vorteile, da der Unterdruck direkt auf die Haut einwirken kann 29 und auf diese Weise Schweiß und Feuchtigkeit von der Hautoberfläche ableitet.
Fallstudie
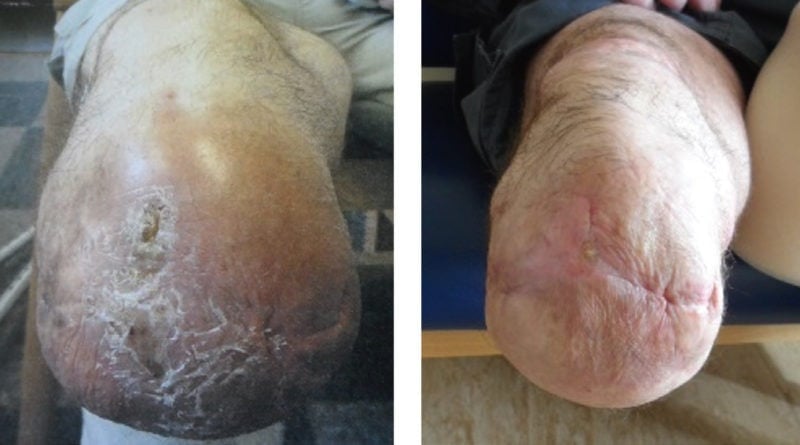
In einer kürzlich erschienenen wissenschaftlichen Publikation wurden die Auswirkungen einer Kombination aus fortschrittlichem Liner, einer Vakuumanbindung und der oben beschriebenen Knöchelgelenktechnologie auf einen transtibial vaskulär Amputierten der Mobilitätsklasse 2 aufgezeigt 30(Abb. 6). Der Betroffene litt seit ca. acht Jahren unter ständigen Hautproblemen, darunter Mazeration und Infektion der Haut, und hatte bereits einen Revisionseingriff in Erwägung gezogen, um diese Probleme zu beheben. Alternativ begann er mit der Anwendung eines perforierten Silcare-Breathe-Liners (Blatchford), um seine Haut trocken zu halten, und kombinierte diesen dann mit einem Avalon-Hydraulikknöchelgelenkfuß und einem Vakuumschaftsystem. Nach kontinuierlicher Anwendung dieser Kombination konnte durch das trockenere Stumpfklima – kombiniert mit verringertem Druck an der Stumpf-Schaft-Schnittstelle und einem Vakuum im Schaft – eine maßgebliche Verbesserung seines Hautzustands erzielt werden.
Schlussfolgerung
Ein fortgeschrittenes Alter sollte kein Hindernis für eine erfolgreiche prothetische Versorgung sein. Obwohl Stürze und Schädigungen des Weichgewebes eine besondere Herausforderung darstellen, verfügt die Prothesentechnologie über wissenschaftlich als geeignet erwiesene Methoden wie z. B. eine Vakuumanbindung und eine Hydraulikknöchelgelenktechnologie, um diese Risiken zu senken. Der Einsatz von geeigneter Prothesentechnologie für ältere Amputierte kann die genannten Probleme zum einen kurzfristig beheben und zum anderen langfristig durch Verhinderung von Stürzen, Gewebeverletzungen und häufigen Facharztbesuchen zu einer Senkung der Kosten für die Gesundheitsversorgung beitragen.
Für die Autoren:
Dr. Mike McGrath
Research Scientist Clinical Evidence Blatchford Limited
Unit D Antura, Bond Close
Basingstoke, RG24 8PZ
United Kingdom
Mike.mcgrath@blatchford.co.uk
Begutachteter Beitrag/reviewed paper
McGrath M, Moser D, Baier A. Anforderungen an eine geeignete Prothesentechnologie für ältere, dysvaskuläre Amputierte. Orthopädie Technik, 2010; 70 (11): 42–46
- Entwicklung eines zum physiologischen Gangbild kongruenten polyzentrischen Knieorthesengelenks – Zwischenstand eines Forschungsprojektes — 10. April 2026
- Mikroprozessorgesteuerte stand- und schwungphasenkontrollierte Ganzbeinorthesen (SSCO): Entwicklung, Systeme und Versorgungsrealität in der orthopädietechnischen Praxis — 9. April 2026
- Gips oder Orthese bei distalen Radiusfrakturen? — 8. April 2026
- GBE-Bund.de. Das Informationssystem der Gesundheitsberichterstattung des Bundes. http://www.gbe-bund.de/gbe10/pkg_isgbe5.prc_isgbe?p_uid=gast&p_aid=0&p_sprache=D (Zugriff am 08.08.2019)
- Fletcher DD, Andrews KL, Hallett Jr JW, Butters MA, Rowland CM, Jacobsen SJ. Trends in rehabilitation after amputation for geriatric patients with vascular disease: implications for future health resource allocation. Arch PhysMed Rehabil, 2002; 83 (10): 1389–1393
- Prince F, Corriveau H, Hébert R, Winter DA. Gait in the elderly. Gait Posture, 1997; 5 (2): 128–135
- Hunter SW, Batchelor F, Hill KD, Hill A‑M, Mackintosh S, Payne M. Risk factors for falls in people with a lower limb amputation: a systematic review. PM R, 2016; 9 (2): 170–180
- Hunter SW, Batchelor F, Hill KD, Hill A‑M, Mackintosh S, Payne M. Risk factors for falls in people with a lower limb amputation: a systematic review. PM R, 2016; 9 (2): 170–180
- Hunter SW, Batchelor F, Hill KD, Hill A‑M, Mackintosh S, Payne M. Risk factors for falls in people with a lower limb amputation: a systematic review. PM R, 2016; 9 (2): 170–180
- Greenhalgh DG. Wound healing and diabetes mellitus. Clin Plast Surg, 2003; 30 (1): 37–45
- Izumi Y, Satterfield K, Lee S, Harkless LB. Risk of reamputation in diabetic patients stratified by limb and level of amputation a 10-year observation. Diabetes Care, 2006; 29 (3): 566–570
- Moore R. Effect on Stance Phase Timing Asymmetry in Individuals with Amputation Using Hydraulic Ankle Units. JPO J Prosthet Orthot, 2016; 28 (1): 44–48
- Barnett CT, Brown OH, Bisele M, Brown MJ, De Asha AR, Strutzenberger G. Individuals with Unilateral Transtibial Amputation and Lower Activity Levels Walk More Quickly when Using a Hydraulically Articulating Versus Rigidly Attached Prosthetic Ankle-Foot Device. JPO J Prosthet Orthot, 2018; 30 (3): 158–164
- Moore R. Patient Evaluation of a Novel Prosthetic Foot with Hydraulic Ankle Aimed at Persons with Amputation with Lower Activity Levels. JPO J Prosthet Orthot, 2017; 29 (1): 44–47
- McGrath M, Laszczak P, Zahedi S, Moser D. Microprocessor knees with “standing support” and articulating, hydraulic ankles improve balance control and inter-limb loading during quiet standing. J Rehabil Assist Technol Eng, 2018; 5: 2055668318795396
- Johnson L, De Asha AR, Munjal R, Kulkarni J, Buckley JG. Toe clearance when walking in people with unilateral transtibial amputation: effects of passive hydraulic ankle. J Rehabil Res Dev, 2014; 51 (3): 429–437
- Portnoy S, Kristal A, Gefen A, Siev-Ner I. Outdoor dynamic subject-specific evaluation of internal stresses in the
residual limb: hydraulic energy-stored prosthetic foot compared to conventional energy-stored prosthetic feet. Gait Posture, 2012; 35 (1): 121–125 - Portnoy S, Kristal A, Gefen A, Siev-Ner I. Outdoor dynamic subject-specific evaluation of internal stresses in the residual limb: hydraulic energy-stored prosthetic foot compared to conventional energy-stored prosthetic feet. Gait.Posture, 2012; 35 (1): 121–125
- Shepherd RB, Koh HP. Some biomechanical consequences of varying foot placement in sit-to-stand in young women. Scand J Rehabil Med, 1996; 28 (2): 79–88
- Moore R. Effect on Stance Phase Timing Asymmetry in Individuals with Amputation Using Hydraulic Ankle Units. JPO J Prosthet Orthot, 2016; 28 (1): 44–48
- Barnett CT, Brown OH, Bisele M, Brown MJ, De Asha AR, Strutzenberger G. Individuals with Unilateral Transtibial Amputation and Lower Activity Levels Walk More Quickly
when Using a Hydraulically Articulating Versus Rigidly Attached Prosthetic Ankle-Foot Device. JPO J Prosthet Orthot, 2018; 30 (3): 158–164 - Moore R. Patient Evaluation of a Novel Prosthetic Foot with Hydraulic Ankle Aimed at Persons with Amputation with Lower Activity Levels. JPO J Prosthet Orthot, 2017; 29 (1): 44–47
- Tang J, McGrath M, Laszczak P, Jiang L, Bader DL, Moser D, Zahedi S. Characterisation of dynamic couplings at lower limb residuum/socket interface using 3D motion capture. Med Eng Phys, 2015; 37 (12): 1162–1168
- Tang J, McGrath M, Hale N, Jiang L, Bader D, Laszczak P, Moser D, Zahedi S. A combined kinematic and kinetic analysis at the residuum/socket interface of a knee-disarticulation amputee. Med Eng Phys, 2017;49: 131–139
- Sanders JE, Harrison DS, Myers TR, Allyn KJ. Effects of elevated vacuum on in-socket residual limb fluid volume: Case study results using bioimpedance analysis. J Rehabil Res Dev, 2011; 48 (10): 1231–1248
- Rink C, Wernke MM, Powell HM, Gynawali S, Schroeder RM, Kim JY, Denune JA, Gordillo GM, Colvin JM, et al. Elevated vacuum suspension preserves residual-limb skin health in people with lower-limb amputation: Randomized clinical trial. J Rehabil Res Dev, 2016; 53 (6): 1121–1132
- Darter BJ, Sinitski K, Wilken JM. Axial bone-socket displacement for persons with a traumatic transtibial amputation: The effect of elevated vacuum suspension at progressive body-weight loads. Prosthet Orthot Int, 2016; 40 (5): 552–557
- Brunelli S, Averna T, Delusso M, Traballesi M. Vacuum assisted socket system in transtibial amputees: Clinical report. Orthop Tech Quarterly (Engl. ed.), 2009; 2: 2–7D
- Dudek NL, Marks MB, Marshall SC, Chardon JP. Dermatologic conditions associated with use of a lower-extremity prosthesis. Arch Phys Med Rehabil, 2005; 86 (4): 659–663
- McGrath M, McCarthy J, Gallego A, Kercher A, Zahedi S, Moser D. The influence of perforated prosthetic liners on residual limb wound healing: a case report. Can Prosthet Orthot J, 2019; 2 (1): No. 3
- McGrath M, McCarthy J, Gallego A, Kercher A, Zahedi S, Moser D. The influence of perforated prosthetic liners on residual limb wound healing: a case report. Can Prosthet Orthot J, 2019; 2 (1): No. 3
- McGrath M, McCarthy J, Gallego A, Kercher A, Zahedi S, Moser D. The influence of perforated prosthetic liners on residual limb wound healing: a case report. Can Prosthet Orthot J, 2019; 2 (1): No. 3
- McGrath M, McCarthy J, Gallego A, Kercher A, Zahedi S, Moser D. The influence of perforated prosthetic liners on residual limb wound healing: a case report. Can Prosthet Orthot J, 2019; 2 (1): No. 3