Einleitung
Ausgedehnte Defekte der Extremitäten nach schweren mechanischen oder thermischen Traumata und nach Tumorresektionen werden heute meist in einem interdisziplinären Ansatz gelöst, um eine ideale, für den Patienten maßgeschneiderte Rekonstruktionslösung anbieten zu können. Frühzeitige Kommunikation, gemeinsame Planung und das Wissen um die Möglichkeiten und Limitationen der verschiedenen Verfahren der beteiligten Disziplinen sind dabei Voraussetzung.
Eine große Zahl der Defekte bedarf eines freien mikrovaskulären Gewebetransfers, da mit ortsständigem Gewebe oder avaskulären Transplantaten (z. B. Spalthaut) keine oder nur eine unbefriedigende Lösung zu erzielen ist. Die Grundprinzipien der eskalierenden Komplexität (sogenannte rekonstruktive Leiter 1) führen somit automatisch zu Verfahren, bei denen mehrere Gewebearten in zusammenhängender Form (Compound-Lappenplastiken) oder an verschiedenen Gefäßstielen (Chimärenlappenplastiken 2) transplantiert werden. Oft kann man mit diesen Transplantaten aus den drei klassischen Entnahmeregionen (Tab. 1) die rekonstruktiven Probleme suffizient lösen 3 4 5.
In besonderen Fällen sind die rekonstruktiven Anforderungen jedoch so hoch, dass sich die mikrochirurgische Konstruktion primär nicht zusammenhängender Gewebeteile anbietet. Diese sogenannten fabrizierten Chimärenlappen haben in folgenden Fällen Vorteile:
- wenn die einzelnen Gewebearten innerhalb eines vaskulären Stromgebietes nicht optimal zur Defektgeometrie und ‑größe passen,
- wenn der Defekt extrem groß ist,
- wenn eine Knappheit vorhandener oder präparierbarer Anschlussgefäße vorliegt,
- wenn es Probleme beim Hebestellenverschluss geben könnte, sofern alle Komponenten aus einer Region (s. Tab. 1) entnommen werden,
- wenn eine sekundäre weitere Lappentransplantation extrem schwierig oder unmöglich ist oder
- wenn die Einzelkomponenten möglichst unabhängig platziert werden müssen 6.
Im Folgenden werden vier Fallbeispiele zur Illustration dieser klinischen Strategie zur individualisierten Defektrekonstruktion dargestellt und die Erfahrungen der Verfasser diskutiert.
Fall 1
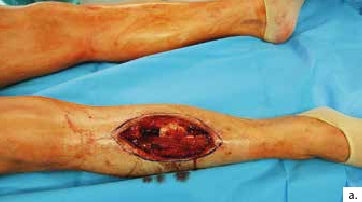
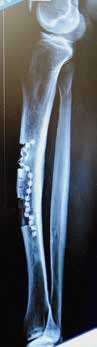
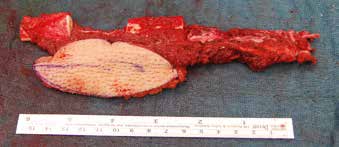
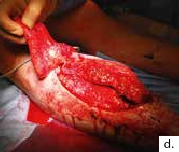
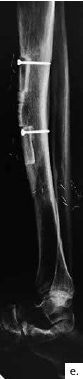
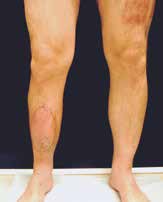
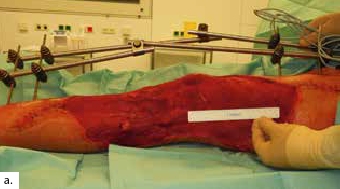
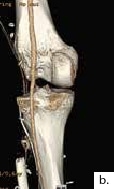
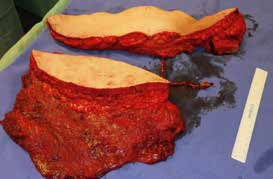
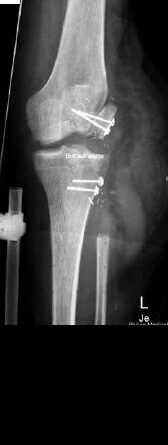
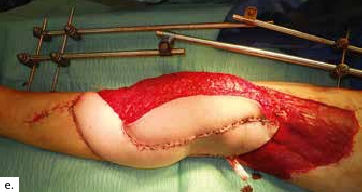
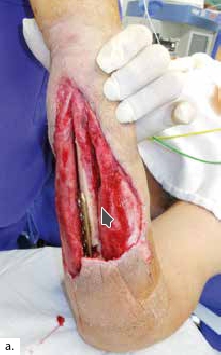
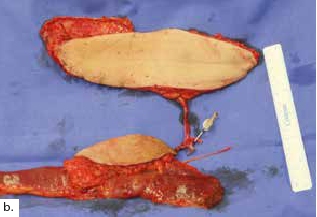
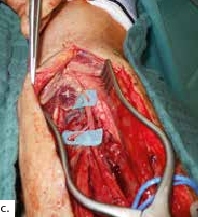
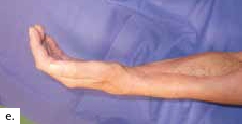
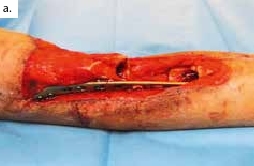
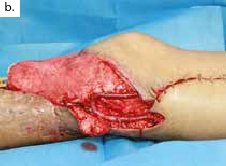
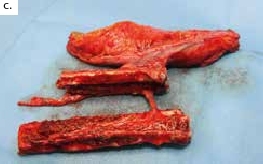
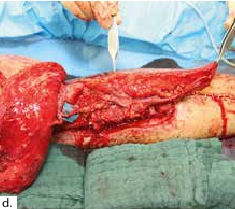
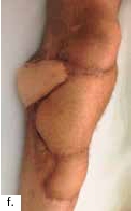
Nach einem kindlichen Trauma entwickelte ein 36-jähriger Mann eine chronische Tibiaschaftosteitis mit großer Defektwunde. Die Sanierung der Staphylococcus-aureus-positiven Osteitis erfolgte durch unfallchirurgische serielle Debridements der Knochen und Weichteile (Abb. 1a) und durch lokale und systemische Antibiotikagabe. Nach dreifach negativen Abstrichen wurden die durch die Markraumausfräsung entstandenen Tibiadefekte (Abb. 1b) mit einer an der A. tibialis posterior vaskularisierten, segmentierten Fibula (Abb. 1c) rekonstruiert. Um den Integumentdefekt neben der Fibulamonitorinsel und die freiliegende Tibia komplettierend zu decken, wurde an das distale Ende der A. fibularis des Knochentransplantats ein freier M.-gracilis-Muskellappen angeschlossen; die Fibula diente somit als Durchflusslappenplastik (Abb. 1d). Die Knochentransplantate wurden mit Einzelschraubenosteosynthesen gesichert und zeigen zehn Wochen postoperativ bereits Zeichen einer knöchernen Einheilung (Abb. 1e). Der Heilungsverlauf der Integumentrekonstruktion gestaltete sich ebenfalls unauffällig (Abb. 1f). Nach dreimonatiger Entlastung an Unterarmgehstützen und sechsmonatiger Kompressionsstrumpftherapie geht der Patient inzwischen volllastig ohne Gehhilfen.
Fall 2
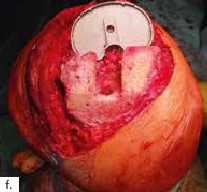
Ein 28-jähriger Motorradfahrer kollidierte mit einem Pkw und erlitt eine Defektfraktur der linken proximalen Fibula und einen Verlust der lateralen Femurkondyle inklusive des lateralen Bandapparates unter einem extrem großen Weichteildefekt (Abb. 2a u. b). Nach multiplen auswärtigen Debridements wurde nach Zuweisung ins eigene Haus interdisziplinär besprochen, die Extremität mit einer Kniegelenkprothese und einer plastisch-chirurgischen Defektdeckung zu erhalten. In einem ersten Schritt wurde ein kontralateraler Tensor-fasciae-latae-(TFL-) Lappen umschnitten („flap delay“), um ihn in seiner gesamten Länge vom Beckenkamm bis zum Knie heben zu können. Eine Woche später erfolgte die Konstruktion der fabrizierten Chimärlappenplastik durch Hebung des osteofasziokutanen TFL-Transplantats inklusive eines vaskularisierten Beckenkammblocks und der mikrovaskuläre Anschluss End-zu-End an den Serratusabgang der A. thoracodorsalis des rechten muskulokutanen M.-latissimus-dorsi-Lappens (Abb. 2c). Dieses sehr große zweiblättrige Lappenmodul wurde anschließend End-zu-End an die Vasa gastrocnemia lateralis anastomosiert und die vaskularisierten Einzelkomponenten wie folgt verteilt: Der Beckenkammblock fungierte als laterale Kondylenaugmentation, um den Sitz einer späteren Knieendoprothese zu optimieren; die Faszia lata wurde zur Stabilisierung von diesem Block transossär an die verbleibende Fibula und das laterale Tibiamassiv genäht (Abb. 2d). Die ausgedehnten Lappenplastiken dienten zum Defektverschluss, gemeinsam mit zusätzlichen Spalthauttransplantaten (Abb. 2e). Nach sechswöchiger Abheilung im Fixateur externe erfolgten der Umschulungsbeginn und die Mobilisation an Unterarmgehstützen mit Fußsohlenteilkontakt.
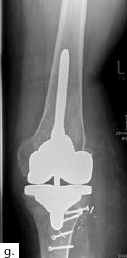
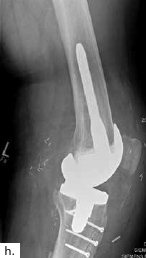
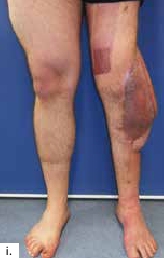
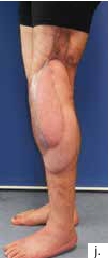
Sechs Monate später konnte bei solide eingeheiltem Knochenblock (Abb. 2f) eine teilgekoppelte Kniegelenkprothese implantiert werden, deren Bedeckung in der Folge durch die ausreichend dimensionierten Lappenplastiken unproblematisch war (Abb. 2g u. h). Der Patient erzielte nach Rehabilitationsmaßnahmen eine vollständige Belastungsfähigkeit bei freier Kniegelenkbeweglichkeit und solide verheiltem Integument (Abb. 2i u. j).
Fall 3
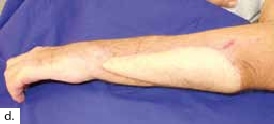
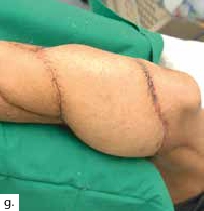
Ein polytraumatisierter Mann erlitt eine Ulnafraktur mit einem Kompartmentsyndrom an seinem linken Unterarm. Aufgrund der lebensbedrohlichen anderen Diagnosen und daher sekundär priorisierter Kompartmentspaltung verlor er sukzessive seine gesamte Beugemuskulatur an dieser Hand. Nach Stabilisierung der Klinik des Patienten resultierte schließlich ein ausgedehnter ulnarer Weichteildefekt mit inzwischen osteosynthetisierter, jedoch freiliegender Ulna und stark vernarbten Weichteilen (Abb. 3a). Die Gefäße am Unterarm waren technisch nicht mehr präparierbar. Dieses rekonstruktive Problem konnte nicht mit einem einzelnen Transplantat gelöst werden. Daher wurde ein fabrizierter Chimärenlappen aus einem großen Oberschenkellappen (ALT-Lappen) und einem funktionellen M.-gracilis-Lappen zusammengesetzt (Abb. 3b) und als Modul in der Ellenbeuge reanastomosiert. Der als Durchflusslappen dienende ALT-Lappen verschloss die Ulnarseite des Unterarms und bedeckte den Knochen. Der an die Gefäße des M. rectus femoris der A. circumflexa femoris lateralis anastomosierte muskulokutane Gracilislappen dagegen wurde in die Beugesehnen der Finger eingeflochten und mit seinem motorischen Nerv an den noch präparierbaren motorischen Nerv der absenten M.-flexor-digitorum-profundus-Muskulatur (Abb. 3c, ellenbogennahe blaue Markierung) koaptiert. Im Zeitraum eines Dreivierteljahres besserten sich Kraft und Beweglichkeit der Finger und des Daumens, sodass der Patient einen kraftvollen Hakengriff aller Finger entwickeln konnte (Abb. 3d). Intensive Physio- und Ergotherapie sowie angepasste dynamische Beuge- und Streckkorrekturschienen wurden stationär begonnen und ambulant fortgeführt. Ein voller Faustschluss war aufgrund der komplexen Vorgeschichte und des klinischen Gesamtbildes allerdings nicht mehr möglich. Das Ziel des funktionellen Extremitätenerhalts wurde jedoch erreicht (Abb. 3e).
Fall 4
Ein 21-jähriger Motorradfahrer erlitt eine komplexe drittgradige Unterschenkelfraktur mit einem 9 cm langen proximalen Tibiadefekt und großer Integumentwunde (Abb. 4a). Aufgrund multipler Voroperationen bis zur Keimfreiheit nach stark verschmutzter Wunde und der erheblichen vaskulären Kompromittierung des Unterschenkels nach dem Unfall konnte ein vaskulärer Anschluss für die Defektdeckung nur über eine intraoperativ angelegte temporäre AV-Schlinge an die Femoralisgefäße im Adduktorenkanal erfolgen (Abb. 4b). Nach Auftrennen dieser Schlinge in einen venösen und einen arteriellen Schenkel konnte ein lateraler Oberschenkellappen („anterolateral thigh“; ALT) mikrovaskulär angeschlossen werden. An das distale Ende des R. descendens der A. circumflexa femoris lateralis an ein versorgendes Gefäß des ALT-Lappens wurde eine segmentierte freie osteofasziokutane Fibula (Abb. 4c) angeschlossen und im Double-Strut-Prinzip in den knöchernen Defekt eingesetzt (Abb. 4d u. e). Eine Wundheilungsstörung im kraniolateralen Bereich wurde durch ein drittes freies Transplantat (Paraskapularlappen) bedeckt (Abb. 4f u. g). Der Anschluss erfolgte an die Poplitealgefäße. Der nachfolgende Heilungsverlauf war ungestört. Eine individualisierte Kompressionsbestrumpfung fand für sechs Monate statt.
Diskussion
Im Zuge einer individualisierten Extremitätenrekonstruktion ist auch die primäre Verwendung freier Lappenplastiken indiziert, wenn dadurch Operationen eingespart werden können und ein für den Patienten optimales Ergebnis erzielen werden kann. Da man die „einfacheren“ Operationsverfahren damit überspringt, spricht man in diesen Fällen vom „rekonstruktiven Fahrstuhl“ 7. Werden die Anforderungen noch komplexer, kann man mit der beschriebenen Technik der Chimärenlappenfabrikation sogar die Einzelkomponenten der Transplantate auswählen. Diese sehr spezielle Strategie wird auch als „reconstructive rocket“ bezeichnet, weil damit für den Patienten gleichsam sämtliche Register der modernen plastischen Chirurgie gezogen werden und sogar prothetische Komponenten mit in die Lappenplastiken eingebaut werden können 8.
Die in der Einleitung und in Tabelle 2 beschriebenen Vorteile dieser Technik sind allerdings mit inhärenten Risiken verbunden, die im Einzelfall sorgfältig abgewogen werden müssen:
- Bei der Entnahme der Transplantate an zwei oder mehr Stellen am Körper sind eine Hebestellenmorbidität und Narben an diesen Stellen zu bedenken. Oft jedoch ist der Hebestellenverschluss an separaten Regionen einfacher, als wenn an einer Region eine sehr große Lappenplastik entnommen werden würde.
- Die primäre Operation einer fabrizierten Chimärenlappenplastik kann länger dauern, da zwei Hebestellen vorliegen und die Einzellappen miteinander reanastomosiert werden müssen. Es ist jedoch auch möglich, dass dadurch letztendlich Folgeoperationen eingespart werden. Zudem ist oftmals die einzeitige Defektrekonstruktion einfacher und sicherer, als wenn z. B. unter einen bereits transplantierten Weichteillappen später ein freies Knochentransplantat gesetzt werden muss.
- Es besteht das Risiko einer Verletzung des Lappenpedikels des ersten Lappens, es liegen Vernarbungen vor, oder eine zweite Empfängergefäßregion ist gar nicht mehr vorhanden. In beengten Verhältnissen kann auch der häufige Vorteil der langen Gefäßstiele zwischen den Lappen problematisch sein, da diese kinking- und torsionsfrei „verlegt“ werden müssen 9.
Die mikrovaskuläre Verbindung der Chimärenlappenmodule kann entweder End-zu-End („sequential“) oder End-zu-Seit („internal“) erfolgen 10. In beiden Fällen besteht das Risiko einer thrombotischen Komplikation und damit eines Lappenverlustes: bei den sequenziellen Lappen für den nachgeschalteten Lappen, bei den End-zu-Seit-Konstrukten sogar für beide Lappen. Deshalb empfiehlt es sich, jeden Lappen einzeln zu überwachen, z. B. über eine Monitorinsel oder eine implantierbare Dopplersonde. Tatsächlich ist jedoch die Verlustrate fabrizierter Lappen vergleichbar mit Einzellappentransplantaten, sofern eine adäquate mikrochirurgische Routine vorliegt 11 12 13 14. Nach eigener Erfahrung der Verfasser ist bisher kein einziges Transplantat von 15 fabrizierten Chimärenlappensystemen, bestehend aus jeweils zwei Einzelkomponenten, verlorengegangen.
Fabrizierte Chimärenlappen sind aufgrund ihres Aufwandes definitiv kein Instrument für die meisten Extremitätenrekonstruktionen. Jedoch spielt gerade in der skelettalen Rekonstruktion die Auswahl eines geeigneten vaskularisierten Knochentransplantates eine entscheidende Rolle, um zu unfallchirurgischen bzw. orthopädischen Techniken kongruente oder zusätzliche Optionen anbieten zu können. Defektgröße und ‑geometrie, Verhältnis zu Spongiosa und Kortikalis, primäre Belastbarkeit und osteogene Potenz unterscheiden sich doch teilweise erheblich. Die Notwendigkeit einer interdisziplinären Kommunikation kann deshalb nicht oft genug betont werden, um beispielsweise sinnlose sekundäre avaskuläre Spongiosatransplantationen unter einen freien Lappen zu verhindern, der zusammen mit einem vaskularisierten Knochenspan das Rekonstruktionsproblem gleich primär und mit schneller einheilendem Knochen gelöst hätte. Insbesondere Fall 2 zeigt daher auch, dass bei gemeinsamer Planung ein hervorragendes Ergebnis für den Patienten erzielt werden kann.
Fazit
Mikrochirurgische Rekonstruktionsmethoden sind aus dem plastisch-chirurgischen Teil der interdisziplinären Extremitätenwiederherstellung nicht mehr wegzudenken. Die meisten Anforderungen können mit singulären Lappen‑, Compound- oder Chimärentransplantaten bewältigt werden. In Einzelfällen sind jedoch zusammengesetzte fabrizierte Lappenmodulsysteme von Vorteil, um mit einem Optimum an Gewebemenge und ‑art in maximaler Platzierungsfreiheit eine kompromisslose Defektrekonstruktion zu erzielen. Bei entsprechender mikrochirurgischer Routine sind die Komplikationsraten gegenüber „normalen“ mikrovaskulären Transplantaten zwar nicht erhöht, jedoch müssen zwei oder mehr Hebestellen in Kauf genommen werden. Einen besonderen Vorteil haben fabrizierte Chimärenlappen bei vaskulär kompromittierten und vernarbten Wunden, da nur eine vaskuläre Spenderregion für mehrere Transplantate benötigt wird.
Für die Autoren:
Prof. Dr. med. Goetz A. Giessler
Direktor der Klinik für Plastischrekonstruktive, Aesthetische
und Handchirurgie
Klinikum Kassel
Mönchebergstraße 41–43
34125 Kassel
goetz.giessler@klinikum-kassel.de
Begutachteter Beitrag/reviewed paper
Giessler GA, Engel H. Komplexe Extremitätenrekonstruktion mit fabrizierten Chimärenlappen. Orthopädie Technik. 2018; 69 (8): 42–47
| Vaskuläres Stromgebiet | Mögliche Lappenplastiken |
|---|---|
| A. subscapularis |
|
| A. circumflexa femoris lateralis |
|
| A. fibularis |
| Vorteile | Nachteile |
|---|---|
|
|
- Vergleichende Prüfung konventioneller und additiv gefertigter Prothesenschäfte in Anlehnung an DIN EN ISO 10328:2016 — 10. März 2026
- Easypreg – ein Faserverbundwerkstoff zum Tiefziehen — 9. März 2026
- Konservative Versorgung einer adulten Skoliose mit einem modularen Bausatz – ein Versorgungsbeispiel — 6. März 2026
- Levin LS. The reconstructive ladder. An orthoplastic approach. Orthop Clin North Am, 1993; 24: 393–409
- Hallock GG. Further clarification of the nomenclature for compound flaps. Plast Reconstr Surg, 2006; 117: 151e–160e
- Engel H, Lin CH, Wei FC. Role of microsurgery in lower extremity reconstruction. Plast Reconstr Surg, 2011; 127 Suppl 1: 228S–238S
- Ninkovic M, Schoeller T, Benedetto KP, Anderl H. Emergency free flap cover in complex injuries of the lower extremities. Scand J Plast Reconstr Surg Hand Surg, 1996; 30: 37–47
- Peek A, Giessler GA. Functional total and subtotal heel reconstruction with free composite osteofasciocutaneous groin flaps of the deep circumflex iliac vessels. Ann Plast Surg, 2006; 56: 628–634
- Giessler GA, Schmidt AB, Germann G, Pelzer M. The role of fabricated chimeric free flaps in reconstruction of devastating hand and forearm injuries. J Reconstr Microsurg, 2011; 27: 567–573
- Gottlieb LJ, Krieger LM. From the reconstructive ladder to the reconstructive elevator. Plast Reconstr Surg, 1994; 93: 1503–1504
- Giessler GA, Hendrich C. De Novo Reconstruction of a Hybrid Patella by Staged Fabrication of a Microvascular Bone Transplant with an Osteointegrated Prosthetic Socket. Plast Reconstr Surg Glob Open, 2017; 4: e1159
- Giessler GA, Schmidt AB, Germann G, Pelzer M. The role of fabricated chimeric free flaps in reconstruction of devastating hand and forearm injuries. J Reconstr Microsurg, 2011; 27: 567–573
- Hallock GG. Further clarification of the nomenclature for compound flaps. Plast Reconstr Surg, 2006; 117: 151e–160e
- Ceulemans P, Hofer SO. Flow-through anterolateral thigh flap for a free osteocutaneous fibula flap in secondary composite mandible reconstruction. Br J Plast Surg, 2004; 57: 358–361
- Chen HC, Demirkan F, Wei FC, Cheng SL, Cheng MH, Chen IH. Free fibula osteoseptocutaneous-pedicled pectoralis major myocutaneous flap combination in reconstruction of extensive composite mandibular defects. Plast Reconstr Surg, 1999; 103: 839–845
- Dzwierzynski WW, Sanger JR, Yousif NJ, Matloub HS. Case report: sequential vascular connection of free flaps in the upper extremity. Ann Plast Surg, 1997; 39: 303–307
- Wei FC, Demirkan F, Chen HC, Chen IH. Double free flaps in reconstruction of extensive composite mandibular defects in head and neck cancer. Plast Reconstr Surg, 1999; 103: 39–47