Es wurde die Anwendbarkeit und Praktikabilität eines myoelektrischen Steuersystems untersucht. Zudem wurde ermittelt, dass implantierte Elektroden ein robusteres Signal liefern und derzeit eine geeignetere myoelektrische Steuerung bieten als Systeme, die Oberflächenelektroden verwenden.
Einleitung
Vor- und Nachteile anpassungsfähiger Prothesen
Mikroprozessorgesteuerte Prothesen bieten die fortschrittlichste Steuerung unter den handelsüblichen Beinprothesen. Diese nutzen Informationen von kinetischen und kinematischen Sensoren, um sich der Bewegung des Anwenders anzupassen, und haben keine direkte Möglichkeit, die Absichten des Anwenders durch Messungen zu erkennen. Eine mikroprozessorgesteuerte Prothese kann sich bis zu einem gewissen Grad auf den Anwender einstellen, z. B. durch die Angleichung an verschiedene Gehgeschwindigkeiten. Es hat sich gezeigt, dass die wichtigsten Vorteile u. a. in einer Reduzierung des Stolperrisikos liegen, was zu einer erhöhten Sicherheit 1 führt, darüber hinaus einem natürlicheren Gangbild beim Hinauf- und Hinabgehen von Treppenstufen und schiefen Ebenen 2 3, einem geringeren metabolischen Energieverbrauch 4 und einer verbesserten Fortbewegung 5.
Die derzeitigen mikroprozessorgesteuerten Prothesen erfordern ein gewisses Training und sind nicht immer intuitiv für die Anwender. Sie haben zudem über mehrere Ebenen hinweg einen eingeschränkten Bewegungsumfang, bieten eine eingeschränkte oder keine aktive Kraftunterstützung und keine direkte willkürliche Steuerung. Mit anderen Worten weisen derzeitige Prothesen im Vergleich zur gesunden unteren Extremität zahlreiche Einschränkungen auf. Eine Mensch-Maschine-Schnittstelle, die sich des Gehirns bedient, kann einige dieser Einschränkungen überwinden, indem sie die leistungsfähigste Schaltzentrale der Welt anzapft, die in der Lage ist, komplexe Bewegungen zu steuern und gleichzeitig darüber nachzudenken, was es abends zu essen geben soll. Fortschrittliche Mensch-Maschine-Schnittstellen verwenden bioelektrische Signale, um eine direkte Verbindung zum Nervensystem aufzubauen und auf diese Weise das weltbeste Steuerzentrum zu nutzen – das Gehirn 6.
Die Nutzung elektrischer Muskelsignale
Elektromyographische Signale (EMG-Signale), die sich der elektrischen Aktivität von Muskeln bedienen, werden verwendet, um den Anwendern von Prothesen zugleich willkürliche und nichtwillkürliche Kontrolle zu ermöglichen. Myoelektrische Arm- und Handprothesen sind kommerziell erhältlich. Untersuchungen mittels Oberflächenelektroden weisen darauf hin, dass EMG-gesteuerte Prothesen eine verbesserte Funktion und Ausführung bieten und darüber hinaus Muskelschwund und Phantomschmerzen reduzieren 7 8 9 10. Dadurch, dass dem Amputierten die direkte Steuerung seiner Prothese auf eine intuitive Art ermöglicht wird, entwickelt er ein stärkeres Bewusstsein für seine Prothese und nimmt diese leichter als Teil seiner selbst an. Dies sollte den Anwender zudem in die Lage versetzen, schneller und angemessener in Situationen zu reagieren, die durch die Programme nicht vorhergesehen werden können.
Oberflächen- vs. implantierte Elektroden
Trotz der vielversprechenden Ergebnisse unter Laborbedingungen sind keine EMG-gesteuerten Beinprothesen auf dem Markt. Dies ist in hohem Maße auf die mit Oberflächenelektroden in Verbindung stehenden Einschränkungen und die Herausforderung zurückzuführen, eine geeignete und komfortable Oberflächen-EMG-Aufzeichnungsanordnung zu erreichen. Oberflächenelektroden reagieren empfindlich auf Umweltveränderungen wie hohe Kräfte im Schaft des Amputierten, durch Schweiß bedingte Störungen, Verschiebung der Elektrodenposition durch Anund Ausziehen des Schafts, Netzbrummen und Bewegungsartefakte 11 12. Diese Einschränkungen haben dazu geführt, dass ein umfassendes Training erforderlich ist und die Systeme häufig nur während des Sitzens oder Stillstehens Anwendung finden können 13.
Die Alfred Mann Foundation entwickelte die ersten vollständig implantierbaren myoelektrischen Sensoren (IMES), um die inhärenten Probleme von Oberflächenelektroden zu überwinden. Die Sensoren können durch einen kleinen (5–10 mm) Einschnitt in einen verbleibenden Muskel des Stumpfes eingepflanzt werden und dienen der Erfassung der Muskelaktivität 14. Sie werden durch eine magnetische Verbindung mit Energie versorgt, die auch dafür verwendet wird, drahtlos Informationen an die IMES zu übermitteln und von diesen zu empfangen. Die Sensoren können problemlos vom Anwender durch Abschalten der magnetischen Verbindung oder durch Ausziehen des Prothesenschafts ausgeschaltet werden. Diese Sensoren sorgen für eine robuste Aufzeichnungsanordnung, und die Umweltfaktoren, die bei Oberflächen-EMGs zu Beschwerden und Signalstörungen geführt haben, werden durch das Implantieren der Elektroden vollständig umgangen.
Ziel dieser Studie war der Vergleich der Erfassung myoelektrischer Signale mittels Oberflächenelektroden vs. IMES und die Umsetzbarkeit ihrer Verwendung für die Steuerung von Beinprothesen.
Equipment und Methode
Probanden und Eingriffe
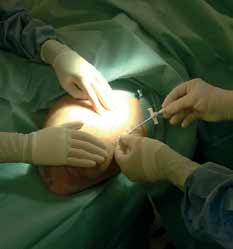
Zwei Beinamputierte wurden für eine IMES-Studie ausgewählt: ein Oberschenkelamputierter (TF = transfemoral) und ein Unterschenkelamputierter (TT = transtibial). Bei beiden Amputierten handelte es sich um erfahrene Anwender mit dem Aktivitätsgrad K3. Feine Drahtelektroden wurden verwendet, um zu überprüfen, dass von jedem Muskel bei einer willkürlich ausgelösten Kontraktion ein ausreichendes myoelektrisches Signal erfasst werden konnte. Zwei IMES-Sensoren wurden anschließend bei beiden Anwendern implantiert, beim oberschenkelamputierten Probanden in den Musculus biceps femoris und den Musculus vastus lateralis und beim unterschenkelamputierten Probanden in den Musculus tibialis anterior und den Musculus gastrocnemius. Jeder Eingriff dauerte etwa 30 Minuten und wurde unter lokaler Anästhesie und leichter Sedierung durchgeführt (Abb. 1). Beide Probanden wurden darum gebeten, bis zwei Wochen nach der Operation Unterarmgehstützen anstelle ihrer Prothesen zu verwenden, und es wurde ihnen eine vierwöchige Rehabilitationszeit gewährt, bevor mit den IMES-Tests begonnen wurde.
Das IMES-System
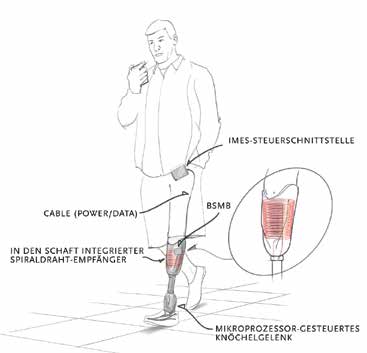
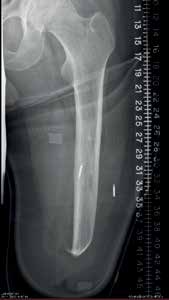
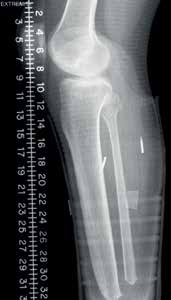
Jeder Sensor hat einen Durchmesser von etwa 2,5 mm und eine Länge von 16 mm, wobei die kundenspezifische Elektronik in einem Keramikzylinder untergebracht ist. Jedes Zylinderende ist aus leitfähigem Metall hergestellt, das als Elektrode dient (Abb. 2). Nach der Implantation wurden Röntgenbilder aufgenommen, um zu bestätigen, dass das Implantat an der richtigen Stelle sitzt, entsprechend der beabsichtigten Platzierung des Schafts (Abb. 3). Nachdem die Sensoren in die verbleibenden Muskeln des Stumpfes implantiert wurden, kann der im Prothesenschaft untergebrachte Spiral-Empfänger dazu verwendet werden, drahtlos über ein magnetisches Feld Energie und Informationen an die IMES zu übermitteln und von diesen zu empfangen. Der Spiraldraht-Empfänger wird mittels eines Spulentreibers gesteuert, der das magnetische Feld reguliert. Die IMES-Steuerschnittstelle versorgt den IMES mit Energie, sorgt für die Programmierung, empfängt Daten vom IMES und ist mit dem Message Broker für das bionische Signal (BSMB = „bionic signal message broker“) verbunden, der das IMES-System und die Prothesen von Össur miteinander verbindet (Abb. 4). Die IMES sind aufgrund von Stabilitätsproblemen nur in der Lage, gefilterte, gleichgerichtete und integrierte Signale zu versenden, und die Abtastrate des Sensors betrug 236 Abtastwerte pro Sekunde.
Oberflächenelektrodenanordnung
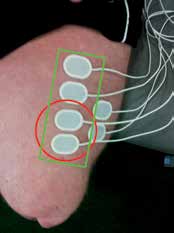
Es wurden vorausgehende Tests durchgeführt, um die passende Oberflächenelektrodenanordnung zu ermitteln. Ein Biosignalverstärker sowie ein Aufzeichnungssystem von Kine ehf wurden für die Erfassung des Oberflächen-EMG-Signals verwendet. Diese Verstärker haben eine Abtastfrequenz von 1600 Hz und können drahtlos EMG-Daten an einen Computer übermitteln. Es zeigte sich, dass die Passform des Schafts die Muskelaktivität des Stumpfes beeinflusst, und es war daher äußerst wichtig, denselben Schaft für die Erfassung der IMES und der Oberflächen-EMGs zu verwenden. Die Verstärker waren zu groß, um innerhalb des IMES-Schafts verwendet zu werden, und es wurden daher weiche Hydrogel-Elektroden auf der Haut angebracht und die Verbindungsdrähte proximal über den Schaftrand zu den auf dem Rücken des Probanden befindlichen Biosignalverstärkern geführt. Um die ideale Position für die Elektroden zu bestimmen, wurde der Stumpf während der Kontraktionen abgetastet und der Bereich von größtem Interesse ermittelt und gekennzeichnet. Es wurden im Anschluss iterative Messungen vorgenommen, um die Stelle mit der maximalen Signalstärke ausfindig zu machen. An der Stelle mit der maximalen Signalstärke sowie um den Bereich der durch Liner und Schaft zu erwartenden Verschiebung herum, d. h. nach proximal, wurden anschließend Elektroden platziert (Abb. 5).
Testphase
Muskelaktivitätsmuster variieren stärker zwischen den einzelnen Prothesenanwendern als zwischen nichtamputierten Menschen, was hauptsächlich auf anatomische Unterschiede zwischen Stümpfen und unterschiedliche Gehtechniken zurückzuführen ist 15. Aus diesem Grund wurden die natürlichen Muskelaktivitätsmuster und die willkürlich ausgelösten Kontraktionen zu Beginn mit dem Rheo Knee und dem Proprio Foot ohne EMG-Steuerung erfasst, um festzulegen, wann und wie die Steuerung umgesetzt werden soll.
Oberflächen-EMG-Signale wurden während des Sitzens mit und ohne den Liner und während des Stehens auf einer Prothese erfasst, um die Auswirkungen der prothetischen Schnittstelle auf das Signal auszuwerten. Der unterschenkelamputierte Anwender wurde darüber hinaus gebeten, seine Muskeln beim Gehen auf ebener Fläche willkürlich zu kontrahieren, um das Steuersignal für Dorsal- und Plantarflexion zu imitieren. Das Muskelaktivitätsmuster wurde dann mit den IMES und den Oberflächenelektroden beim Gehen, beim Herabgehen von Treppen sowie beim Hinsetzen und Aufstehen erfasst. Das Oberflächen-EMG konnte aufgrund des vom IMES-System erzeugten magnetischen Felds nicht erfasst werden, solange das System eingeschaltet war, daher wurden diese Messungen nicht gleichzeitig vorgenommen.
Unterschiede zwischen den IMES- und den EMG-Signalen wurden verglichen, wobei der Fokus auf Langzeitanwendung und Zuverlässigkeit gelegt wurde. Signalqualitäten wurden unter Verwendung von EMG-Profilen untersucht, wobei die mittlere Amplitude und die Standardabweichung des Signals während mehrerer Zyklen verglichen wurden. Die praktischen Einzelheiten der zwei Erfassungsmethoden wurden unter Berücksichtigung von Verbindungsausfällen und Anwenderkomfort bewertet.
Ergebnisse
Es traten während der Verfahren keine unerwünschten Ereignisse auf, und die Implantate sind auch drei Jahre nach der Implantation vollständig funktionsfähig. Die Sensoren haben bei den Probanden keinerlei Beschwerden verursacht, und sie konnten ihre Prothese uneingeschränkt nutzen.
Die Oberflächen-EMG-Aufzeichnungen von willkürlichen Kontraktionen beim Sitzen zeigten ein verbessertes Signal-Rausch-Verhältnis nach Anziehen des Liners. Das Signal war während der durch die Probanden willkürlich im Stehen auf ihrer Prothese ausgelösten Kontraktion am stärksten. Dies könnte darauf zurückzuführen sein, dass der zusätzliche Druck durch den Schaft die Elektroden nahe an der Signalquelle gehalten hat und/oder die Probanden im Stehen eine stärkere Kontraktion hervorrufen konnten. Die durch beide Probanden willkürlich ausgelösten Kontraktionen konnten mit den Oberflächenelektroden und den IMES in Situationen mit und ohne Belastung erfasst werden. Die Signalqualität der Oberflächen-EMG lag jedoch unter der Qualität der auf EMG-Profilen basierenden IMES-Signale.
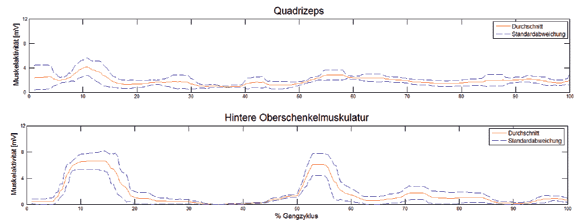
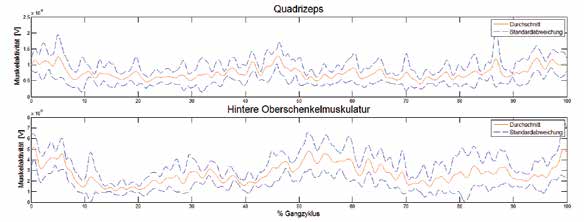
Die mittlere Amplitude der Signale war bei allen Belastungsübungen (z. B. Gehen, Herabgehen von Treppen sowie Aufstehen und Hinsetzen) bei beiden Muskeln höher und zeigte im Vergleich mit dem Oberflächen-EMG-Signal eine niedrigere Variabilität beim IMES-Signal. Dies ist in Abbildung 6 dargestellt, welche die mittlere und die Standardabweichung der IMES- und der Oberflächen-EMG-Signale zeigt, die beim Herabgehen einer Treppe aufgezeichnet wurden. Auf dieser Abbildung ist zu sehen, dass die hintere Oberschenkelmuskulatur beim Beugen des Knies und vor der anschließenden Schwungphasenextension aktiviert wird. Während des Gehens konnte ein ausgeprägtes Muskelaktivitätsmuster beim oberschenkelamputierten Probanden aufgezeichnet werden. Der oberschenkelamputierte Anwender hatte jedoch Schwierigkeiten bei der Durchführung einer willkürlichen Kontraktion einzelner Muskeln, wie das Oberflächen-EMG und die IMES-Messungen zeigten.
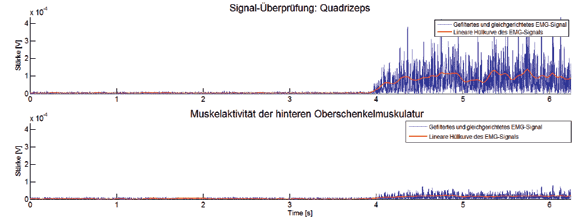
Ein Beispiel für die Prüfung des Oberflächen-EMG-Signals ist in Abbildung 7 zu sehen, wo der Proband darum gebeten wurde, 5 Sekunden lang zu entspannen und dann seinen Quadrizeps anzuspannen. Das Kontraktionssignal des untersuchten Muskels war immer stärker als die Signale der mitkontrahierenden Muskeln, die daher bei einem Kontrollschema mit einfachem Schwellenwert außer Acht gelassen werden können. Beim unterschenkelamputierten Probanden lagen keinerlei ausgeprägte Muskelaktivitätsmuster vor, die beim Gehen auf ebener Fläche mit einem der beiden Setups hätten erfasst werden können. Als der Proband jedoch dazu aufgefordert wurde, an das Heben seiner Zehen während des Gehens zu denken, konnte eine deutliche Aktivität festgestellt werden.
Die Messungen mit dem Oberflächen-EMG dauerten 6 Stunden, während die Aufzeichnungssitzung mit den IMES 3 Stunden in Anspruch nahm. Der zeitliche Unterschied kam dadurch zustande, dass es aufgrund von Schweiß und Bewegungsartefakten zu Verbindungsausfällen der Oberflächenelektroden kam, was zu häufigeren Aufzeichnungen führte. Die Probanden nahmen keine oder nur leichte Beschwerden während der Messung wahr. Die Elektroden und Drähte hinterließen jedoch in beiden Fällen sichtbare Abdrücke auf der Haut der Probanden. Beide Probanden berichteten, dass diese Abdrücke für den Rest des Tages blieben.
Diskussion
Die aufgezeichneten Oberflächen-EMG- und IMES-Signale wären beide bei Vorliegen des richtigen Kontrollschemas potenziell für die willkürliche Steuerung von Beinprothesen geeignet. Das ausgeprägte unwillkürliche Muskelaktivitätsmuster des oberschenkelamputierten Anwenders, das bei allen Übungen mit den IMES-Aufzeichnungen zu sehen war, könnte ebenfalls für die Steuerung verwendet werden, es muss jedoch auch bei der Umsetzung einer willkürlichen Steuerung Berücksichtigung finden. Als dem oberschenkelamputierten Anwender die direkte Steuerung seines Fußgelenks verliehen wurde, führte dies aufgrund der unwillkürlichen Muskelaktivität bei der Vorwärtsbewegung des Fußes zu einer sofortigen Dorsalextension im Knöchelgelenk.
Zwar waren Standard-Filtermethoden nicht immer in der Lage, das Rauschen des Oberflächen-EMG-Signals zu entfernen, doch die Merkmale der Artefakte und des Muskelsignals unterschieden sich, weshalb nützliche Informationen und brauchbare Steuersignale immer vom Oberflächen-EMG-Signal extrahiert werden konnten. Diese Ergebnisse weisen darauf hin, dass das Hauptproblem der Verwendung myoelektrischer Signale für die Steuerung von Beinprothesen nicht die Signalqualität ist, sondern die Gestaltung einer kommerziell akzeptablen prothetischen Schnittstelle, die ausreichend robust und komfortabel für den Anwender ist.
Diese Studie beschränkte sich auf lediglich zwei prothetische Schnittstellen, eine für jeden Probanden, doch Untersuchungen und Erfahrungen haben gezeigt, dass die Integration eines biologischen Verstärkers in die prothetische Schnittstelle zu einem komfortableren Setup mit weniger Artefakten führt F13]. Derzeit laufen weitere Forschungsarbeiten zur Entwicklung einer komfortablen und robusten prothetischen Schnittstelle mit Oberflächen-EMG, die zeigen, wie vielversprechend EMG-gesteuerte Beinprothesen sind 16 17 18 19 20. Diese Studien heben darüber hinaus jedoch auch die bereits erwähnten Nachteile von Oberflächenelektroden hervor, und es mangelt ihnen an Praktikabilität.
Beide myoelektrischen Signale, IMES und das der Oberfläche, können für die Steuerung verwendet werden, vorausgesetzt, dass ein geeignetes myoelektrisches Aufzeichnungssystem für die Oberflächenerfassung entwickelt wird. Oberflächensignale können ergänzend zur aktuellen Mikroprozessorsteuerung bionischer Prothesen verwendet werden.
Die IMES liefern ein robustes myoelektrisches Aufzeichnungssystem, das eine fortlaufende IMES-Erprobung ermöglicht. Die vorläufigen Ergebnisse dieser Tests sind vielversprechend, denn der Proband verfügt auf unterschiedlichen Terrains und in verschiedenen Situationen über eine zuverlässige direkte und intuitive Kontrolle über seine Prothese.
Manche menschlichen Aktivitäten und Bewegungen können nicht allein durch Algorithmen und mechanische Daten ausgedrückt werden. Durch eine Verbindung mit dem Nervensystem kann die prothetische Steuerung durch den Anwender über die bestehenden Möglichkeiten hinausgehen. Das Nervensystem kann bidirektionale Informationen für Sensorik und Steuerung liefern, indem es die Prothese mit Anwenderinformationen versorgt und dem Anwender Feedback über die Prothese gibt. Dies ist ein Blick in die Zukunft, aber in der Zwischenzeit muss der Fokus auf die Erzeugung eines praktischen, robusten und intuitiven Steuersystems mit einer komfortablen Schnittstelle gelegt werden.
Hinweis: Ein Video des Össur IMES-Prothesensystems ist auf der Webseite von Össur zu finden 21.
Für die Autoren:
Jona Sigrun Sigurdardottir
Ossur Iceland
Grjothals 1–5
110 Reykjavik, Island
jssigurdardottir@ossur.com
Begutachteter Beitrag/reviewed paper
Sigurdardottir JS, Sigurthorsson SP, Halldorsdottir G, Ludviksdottir GK, Helgason Th, Lechler K, Oddsson M, Ingvarsson Th, Kristjansson K. Oberflächenelektroden vs. implantierte Elektroden zur Steuerung von Beinprothesen. Orthopädie Technik, 2016; 67 (11): 34–38
- Die orthopädietechnische Versorgung mit einer dynamischen Fingerstreckorthese als eigenständige Therapie bei der Dupuytren’schen Kontraktur — 26. März 2026
- Vergleichende Prüfung konventioneller und additiv gefertigter Prothesenschäfte in Anlehnung an DIN EN ISO 10328:2016 — 10. März 2026
- Easypreg – ein Faserverbundwerkstoff zum Tiefziehen — 9. März 2026
- Kahle JT. Comparison of nonmicroprocessor knee mechanism versus C‑Leg on Prosthesis Evaluation Questionnaire, stumbles, falls, walking tests, stair descent, and knee preference. J Rehabil Res Dev, 2008; 45 (1): 1–14
- Alimusaj M, Fradet L, Braatz F, Gerner HJ, Wolf SI. Kinematics and kinetics with an adaptive ankle foot system during stair ambulation of transtibial amputees. Gait & Posture, 2009; 30 (3): 356–363
- Fradet L, Alimusaj M, Braatz F, Wolf SI. Biomechanical analysis of ramp ambulation of transtibial amputees with an adaptive ankle foot system. Gait & Posture, 2010; 32 (2): 191–198
- Delussu AS et al. Assessment of the effects of carbon fiber and bionic foot during overground and treadmill walking in transtibial amputees. Gait & Posture, 2013; 38 (4): 876–882
- Gailey RS et al. Application of self-report and performance-based outcome measures to determine functional differences between four categories of prosthetic feet. J Rehabil Res Dev, 2012; 49 (4): 597–612
- Zhang X, Liu Y, Zhang F, Ren J, Sun YL, Yang Q, Huang H. On Design and Implementation of Neural-Machine Interface for Artificial Legs. IEEE Trans Ind Inform, 2012; 8 (2): 418–429
- Zhang X, Liu Y, Zhang F, Ren J, Sun YL, Yang Q, Huang H. On Design and Implementation of Neural-Machine Interface for Artificial Legs. IEEE Trans Ind Inform, 2012; 8 (2): 418–429
- Wentink EC. Feasibility of Enhanced User Control and Feedback in Upper Leg Prostheses. Diss. University of Twente, Enschede, 2013
- Hargrove LJ et al. Robotic Leg Control with EMG Decoding in an Amputee with Nerve Transfers. New Engl J Med, 2013; 369 (13): 1237–1242
- Ortiz-Catalan M, Sander N, Kristoffersen MB, Håkansson B, Brånemark R. Treatment of phantom limb pain (PLP) based on augmented reality and gaming controlled by myoelectric pattern recognition: a case study of a chronic PLP patient. Front Neurosci, 2014; 8: 24
- Ortiz-Catalan M, Brånemark R, Håkansson B, Delbeke J. On the viability of implantable electrodes for the natural control of artificial limbs: Review and discussion. Biomed Eng Online, 2012; 11 (1): 33
- Oskoei MA, Hu H. Myoelectric control systems – A survey. Biomed Signal Process Control, 2007; 2 (4): 275–294
- Wentink EC. Feasibility of Enhanced User Control and Feedback in Upper Leg Prostheses. Diss. University of Twente, Enschede, 2013
- Weir RF, Troyk PR, DeMichele GA, Kerns DA, Schorsch JF, Maas H. Implantable Myoelectric Sensors (IMESs) for Intramuscular Electromyogram Recording. IEEE Trans Biomed Eng, 2009; 56 (1): 159–171
- Wentink EC. Feasibility of Enhanced User Control and Feedback in Upper Leg Prostheses. Diss. University of Twente, Enschede, 2013
- Zhang X, Liu Y, Zhang F, Ren J, Sun YL, Yang Q, Huang H. On Design and Implementation of Neural-Machine Interface for Artificial Legs. IEEE Trans Ind Inform, 2012; 8 (2): 418–429
- Wentink EC. Feasibility of Enhanced User Control and Feedback in Upper Leg Prostheses. Diss. University of Twente, Enschede, 2013
- Zhou P, Lowery MM, Englehart KB, Huang H, Li G, Hargrove L, Dewald JPA, Kuiken TA. Decoding a New Neural-Machine Interface for Control of Artificial Limbs. J Neurophysiol, 2007; 98 (5): 2974–2982
- Ha KH, Varol HA, Goldfarb M. Volitional control of a prosthetic knee using surface electromyography. IEEE Trans Biomed Eng, 2011; 58 (1): 144–151
- Lipschutz RD, Lock BA. A Novel Research And Clinical Approach To Using Gel Liners For Collection Of Surface Myoelectric Signals For Prosthetic Control. In: Proceedings of the MyoElectric Controls/Powered Prosthetics Symposium 2011, New Brunswick, Canada, 2011
- Össur. Össur Introduces First Mind-Controlled Bionic Prosthetic Lower Limbs for Amputees. http://www.ossur.com/about-ossur/news-from-ossur/1396-ossur-introduces-first-mind-controlled-bionic-prosthetic-lower-limbs-for-amputees (Zugriff am 04.10.2016)