Einleitung
Sprach‑, Atmungs- und Ergotherapeuten sind im ambulanten Bereich zunehmend mit Patienten konfrontiert, die nach invasiver Langzeitbeatmung mit einer geblockten Trachealkanüle (TK) versorgt sind und unter persistierenden Dysphagien leiden. Hierbei kann es zur Penetration von Speichel und Nahrung (wenn diese bis in den Kehlkopfeingang gelangen, jedoch oberhalb der Stimmlippen verbleiben) oder zur Aspiration kommen, bei der Material in die Luftwege unterhalb der Glottis eindringt – im schlimmsten Fall ohne Auslösung eines Hustenreflexes („stille Aspiration“). Eine Aspiration kann lebensbedrohlich sein und eine Pneumonie verursachen.
Mittlerweile wurden diverse praktikable Behandlungspfade zur Schlucktherapie und zur Dekanülierung entwickelt [1, 2], allerdings primär für den klinischen Bereich, in dem neben einer hohen Therapiedichte ein umfassendes 24-Stunden-Monitoring des Patienten möglich ist. Aber auch im außerklinischen Setting kann bei einer ausreichend hohen Therapiefrequenz und unter Einbezug der Pflegekräfte in das Trachealkanülenmanagement eine Dekanülierung und Oralisierung gelingen (wenn auch meist in einem etwas längeren Zeitraum).
Gründe für das Entstehen einer Dysphagie
Schluckstörungen sind eine häufige Kurz- und Langzeitkomplikation nach invasiver Beatmung und Tracheotomie. Vor allem eine länger liegende geblockte TK hat zahlreiche negative Auswirkungen auf den Schluckprozess: Sie vermehrt die Schleimproduktion und verhindert die natürliche Kehlkopfhebung während des Schluckens durch Fixierung der Trachea an der Halshaut (Ankereffekt), sodass der Kehldeckel während der Schluckreflexauslösung unter Umständen insuffizient schließt und Speichel und Nahrung dadurch leichter aspiriert werden können 1. Die Kehlkopfhebung kann dabei so stark eingeschränkt werden, dass der obere Speiseröhrensphinkter nicht mehr öffnet, sodass sich Speichel aufstaut und in die Trachea überlaufen kann. Daneben ist ein physiologischer Luftstrom durch Larynx, Pharynx, Nase und Mundraum ein wichtiger Anreiz zur Auslösung des Spontanschluckens; fehlt dieser Reiz aufgrund einer geblockten TK, sinkt die Schluckfrequenz rapide ab 2. Der fehlende Luftstrom führt außerdem zu teilweise massiven Sensibilitätsbeeinträchtigungen aufgrund mangelnder Stimulation von Chemo- und Druck rezeptoren in der Kehlkopfschleimhaut, sodass Schluck- und Hustenreflex sich zurückbilden können 3. Durch eine fehlende laryngeale Sprengung und einen unzureichenden intrathorakalen Druckaufbau kann aspiriertes Material zudem nicht effektiv abgehustet werden.
Therapeutisches Dilemma
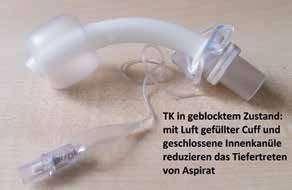
Durch die negativen Auswirkungen der TK auf den Schluckprozess entsteht häufig ein Teufelskreis: Einerseits benötigt der Patient aufgrund seiner reduzierten pharyngo-laryngealen Sensibilität eine geblockte TK, um den Tiefertritt von aspiriertem Material zu vermindern, andererseits führt eine dauergeblockte TK wiederum zu Sensibilitätsstörungen aufgrund des ständigen Speichelreizes auf die umgebende Schleimhaut und den fehlenden physiologischen laryngo-pharyngealen Luftstrom. Therapeuten befinden sich also in einem Dilemma: Zum einen soll der Patient aufgrund von Aspiration möglichst nicht entblockt werden, zum anderen wird sich die Sensibilität ohne physiologische Luftstromlenkung nicht signifikant verbessern 4. Dieser Konflikt ist letztlich nur zu lösen, indem Therapeuten mutig sind und unter (kalkuliertem!) Risiko mit kurzen Entblockungsphasen beginnen, da vor allem eine physiologische Luftstromlenkung durch den Kehlkopf die Sensibilität positiv beeinflusst und zum Anstieg der Schluckfrequenz führt 5. Um den Luftstrom entsprechend zu lenken, kann ein Sprechventil aufgesetzt werden, das als eine Art Rückschlagventil die Ausatmungsluft in Richtung Larynx lenkt (Abb. 1). Durch dieses entsteht ein ausreichend hoher subglottischer Druck, der eine Schlüsselkomponente des effektiven Schluckaktes ist. Zahlreiche Studien zeigen, dass der Aufsatz eines Sprechventils eine sofortige positive Wirkung auf die Biomechanik des Schluckprozesses hat und dass hierdurch schrittweise das Aspirationsausmaß verringert werden kann 67.
Allerdings kann nicht bei jedem Patienten so vorgegangen werden. Kontraindiziert ist eine Entblockung bei Patienten mit rezidivierendem starkem Erbrechen, akutem (antibiotisch behandeltem) pulmonalem Infekt, kontinuierlicher stiller Aspiration ohne Auslösung eines reflektorischen und/oder willkürlichen Hustenstoßes (endoskopischer und radiologischer Aspirationsgrad IV) und nach schweren Hirnstammschädigungen, wenn nicht nur Sensibilitätsstörungen aufgrund der dauergeblockten TK bestehen, sondern zudem noch neurologisch bedingte laryngo-pharyngeale Sensibilitätsbeeinträchtigungen vorliegen. Alle anderen Patienten können von einem kleinschrittigen Dekanülierungsmanagement meist gut profitieren.
Effektives Trachealkanülenmanagement
Erstes Therapieziel bei Patienten mit einer geblockten TK ist die Toleranz gegenüber zunehmenden Entblockungszeiten. Kurzzeitig entblockt (z. B. 10 bis 15 Minuten) werden sollte ab Grad III der endoskopischen Schweregradeinteilung der Aspiration nach Schröter- Morasch (2006), wenn bei permanenter Aspiration ohne Hustenreflex zumindest ein guter willkürlicher Hustenstoß initiiert werden kann, bzw. ab Grad III der radiologischen Schweregradeinteilung von Penetrationen/Aspirationen nach Hanning (1995), wenn trotz Aspiration > 10 % des Bolus ein reflektorischer Husten erfolgt 89.
Bei guter Toleranz und unter kontinuierlichem Monitoring können die Entblockungszeiten dann schrittweise ausgebaut werden. Voraussetzung für zunehmend längere Intervalle ist neben einem willkürlichen und/oder erhaltenen reflektorischen Husten ein ausreichend sicheres Abschlucken des Speichels 10. Treten bei Entblockungszeiten bis zu 24 Stunden über einen Zeitraum von mehreren Tagen keine Komplikationen (Infektionen, Ateminsuffizienz etc.) auf, kann eine ungeblockte TK eingesetzt werden, die dann wiederum in steigenden Intervallen abgestöpselt (d. h. mittels eines Verschlussstopfens komplett verschlossen) wird. Wenn auch das Abstöpseln ohne respiratorische Komplikationen gut toleriert wird, kann der Patient prinzipiell dekanüliert werden. Von Vorteil ist, dass hierbei auch komatöse und schwer bewusstseinsgestörte Patienten von der TK entwöhnt werden können – vorausgesetzt, dass ein reflektorischer Hustenstoß ausgelöst werden kann und dass die Spontanschluckrate ausreichend hoch ist.
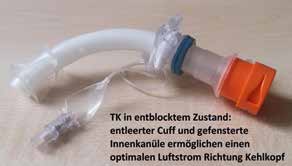
Empfehlenswert ist die Verwendung einer Kombinationskanüle (Abb. 2a–c), die über eine gefensterte und eine geschlossene Innenkanüle verfügt, sodass unter Blockung kaum Sekret von oben durch die TK laufen kann (geschlossene Innenkanüle), unter Entblockung aber eine maximale Luftmenge nach oben gelangen kann (gefensterte Innenkanüle). Auch der Umweg über eine ungeblockte TK ist bei einer Kombi-TK nicht zwingend erforderlich, da diese im entblockten Zustand auch abgestöpselt werden kann. Nahezu jede Firma hat mittlerweile entsprechende Kanülen im Angebot.
Dekanülierungsmanagement bei beatmeten außerklinischen Intensivpatienten
Bei beatmeten Patienten ist die Möglichkeit zur Entblockung der TK abhängig vom Beatmungsmodus und von der Strategie der Entwöhnung („Weaning“).
- Kontrollierte Beatmung: Wird ein Patient kontrolliert beatmet, ist eine Entblockung der TK nicht ratsam, da der Patient keine selbstständigen Atemzüge tätigt. Bei Entblockung würde der Atemhub vom Beatmungsgerät zwar oropharyngeal entweichen, allerdings würde der Patient dadurch ein zu geringes Luftvolumen einatmen, sodass eine adäquate Ventilation nicht gewährleistet wäre.
- Assistierte Beatmung: Hierbei löst der Patient seinen Atemzug am Beatmungsgerät selbstständig aus und erhält auf der Basis voreingestellter Parameter (z. B. Druckunterstützung bei der Einatmung) Hilfestellung vom Respirator. In diesem Modus kann unter Beatmung die TK ganz oder partiell entblockt werden 11. Fakultativ kann ein an das Schlauchsystem adaptierbares Sprechventil aufgesetzt werden – bspw. ein Passy-Muir®-Sprechventil, das zwischen TK und Beatmungsschlauch platziert wird 12. In beiden Fällen muss jedoch gewährleistet sein, dass die Beatmung weiterhin den individuellen Bedürfnissen des Patienten entspricht. Oft müssen hierzu diverse Geräteparameter erhöht und die Leckage-Alarmgrenzen reduziert werden. Die Anpassung der Parameter und die Entscheidung darüber, ob ein beatmeter Patient entblockt werden kann oder nicht, sollte grundsätzlich vom zuständigen Arzt getroffen werden.
- Kontinuierliches Weaning: Hierbei wird der maschinelle Atemanteil kontinuierlich reduziert und der Anteil der Spontanatmung entsprechend erhöht, d. h., die Invasivität der Beatmung wird schrittweise verringert. Da der Patient bis zum Beatmungsende nicht vom Gerät diskonnektiert wird, ist ein Entblocken mit Sprechventilaufsatz nur eingeschränkt möglich. Bei wachen Patienten kann unter Anpassung verschiedener Parameter und Alarmeinstellungen am Respirator im assistierten Beatmungsmodus ein Passy-Muir®-Sprechventil an das Beatmungssystem angeschlossen werden.
- Diskontinuierliches Weaning: Die Entwöhnung besteht hier aus Phasen der assistierten maschinellen Beatmung und Phasen der Spontanatmung ohne Beatmungsgerät (Freiatmungsphasen). Der Patient wird zunehmend länger in eine Freiatmung überführt, in der prinzipiell (in Abhängigkeit von der aktuellen medizinischen Situation) mit dem Entblocken der TK begonnen werden kann. Wichtig ist hierbei ein umfangreiches Wissen über Abbruchkriterien, sodass respiratorisch kritische Situationen rasch erkannt werden – z. B. Unruhe, Tachykardie, Agitiertheit, Kaltschweißigkeit, Angst, vegetativer Stress, Zyanose, eine Steigerung der Atemfrequenz > 35/min, eine insuffiziente Atmung (Sauerstoff-Abfall > 10 %, Tachypnoe, Dyspnoe), ein erhöhter Einsatz der Atemhilfsmuskulatur und/oder ein Anstieg der Herzfrequenz um mehr als 30 % des Ausgangswertes 13. Zeigt der Patient Symptome einer respiratorischen Insuffizienz, müssen Therapeuten das Notfallmanagement beherrschen und den Patienten wieder an das Beatmungsgerät anschließen können.
Kann ein Patient nicht von der Beatmung entwöhnt werden, hängt die weitere Therapie von der aktuellen Beatmungssituation ab, d. h., wie invasiv die Beatmung ist und ob Freiatmungsphasen möglich sind. Innerhalb dieser kann geprüft werden, ob eine Entblockung mit Sprechventil möglich ist – zum einen, um verbale Kommunikation zu ermöglichen und die Sensibilität durch physiologische Luftstromlenkung zu verbessern, zum anderen, um eine orale Ernährung diagnostisch abklären und unter weitestgehend physiologischen Bedingungen erfolgen lassen zu können. Ist eine Entblockung nicht möglich, gibt es seit geraumer Zeit eine TK, mit der ein Patient auch unter Beatmung und Blockung phonieren kann, und zwar mittels eines in die Innenkanüle integrierten Sprechventils (Blom® Tracheostomy Tube System von Pulmodyne®). Allerdings ist die Passform der TK (hinsichtlich Länge, Krümmung und Position der Fensterung) nicht für jeden Patienten optimal geeignet.
Oralisierung von außerklinischen Intensivpatienten
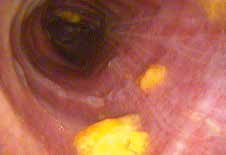
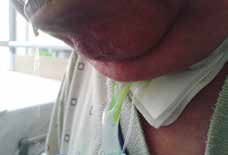
Da alle Patienten nach länger liegender geblockter TK aufgrund der sich daraus möglicherweise entwickelnden Sensibilitätsminderung ein sehr hohes Risiko für eine Dysphagie haben, sollte vor einer oralen Nahrungsgabe unbedingt eine apparative (fiberoptische endoskopische Evaluation) oder klinische Schluckdiagnostik (Speichel- und/oder Bolusfärbetest) erfolgen 14. Eine orale Nahrungsgabe ohne vorherige Evaluation des Schluckvermögens ist grob fahrlässig und kann zu Pneumonien führen (Abb. 3 sowie 4a u. b).
Generell sollte mit einer Oralisierung erst dann begonnen werden, wenn ein Patient ausreichend wach und kognitiv unbeeinträchtigt ist, reflektorisch und/ oder willkürlich abhusten kann, keine akuten pulmonalen Komplikationen bzw. Infekte bestehen und die TK entblockt werden kann. Auf eine Nahrungsgabe bei geblockter TK sollte wenn möglich verzichtet werden, da unter Blockung Aspiration nicht unmittelbar bemerkt wird, aspiriertes Material nicht abgehustet werden kann und der Patient unter Umständen häufiger abgesaugt werden muss, wodurch unnötige Mikroläsionen gesetzt werden, ohne dass das gesamte Aspirat entfernt werden kann 15. Eine dauergeblockte TK ist jedoch prinzipiell keine absolute Kontraindikation gegen eine orale Nahrungsaufnahme: Kann ein Patient aufgrund respiratorischer Probleme nicht vom Beatmungsgerät diskonnektiert oder entblockt werden, ist jedoch wach, kognitiv unbeeinträchtigt und aspiriert nicht, kann er durchaus oralisiert werden. Voraussetzung hierfür ist jedoch eine apparative oder klinische Schluckdiagnostik vor der oralen Nahrungsgabe.
Schlussfolgerungen
Um die Kurz- und Langzeitkomplikationen einer geblockten TK möglichst gering zu halten, sollte ein Dekanülierungsmanagement möglichst zügig begonnen werden. Entscheidend für die Wiedererlangung einer hinreichenden Sensibilität in Larynx und Trachea sowie einer ausreichend hohen Spontanschluckrate ist ein Luftstromstimulus, der durch Entblockung und Aufsatz eines Sprechventils in Richtung Kehlkopf gelenkt wird. Selbstverständlich darf dabei nicht leichtsinnig vorgegangen werden; mögliche negative Konsequenzen bei einem zu forschen Trachealkanülenmanagement (z. B. eine Pneumonie) sind unter kontinuierlichem Monitoring jedoch vermeidbar. Voraussetzung für ein effektives Dekanülierungsmanagement ist, dass alle Berufsgruppen (Therapeuten, Pflege, Arzt) involviert sind. Als Prozedere für den außerklinischen Bereich empfiehlt sich ein schrittweise längeres Entblocken der TK (z. B. beginnend mit 15 Minuten täglich über eine Woche, bei guter Toleranz 30 Minuten täglich, dann 2 Stunden usw.) ab Aspirationsgrad III der radiologischen und endoskopischen Schweregradeinteilung mit Hinnahme eines gewissen Aspirationsrisikos. Dieses besteht allerdings so oder so: Studien zeigen, dass auch eine korrekt geblockte TK nicht sicher vor Aspiration schützt 16. Da also immer Aspirationsgefahr besteht, spricht wenig gegen eine kurzzeitige Entblockung der TK, zumal der Patient erst dann effektiv abhusten und aspiriertes Sekret abgesaugt werden kann, welches sich über dem Cuff angesammelt hat.
Sprach‑, Atmungs- und Ergotherapeuten haben ein großes Spektrum an Optionen bei außerklinisch invasiv beatmeten oder geweanten tracheotomierten Patienten. Diese reichen von der Entblockung der TK in den Frei atmungsphasen beim diskontinuierlichen Weaning, der Entblockung unter Beatmung und dem Einsatz spezifischer Medizinprodukte für beatmete Patienten (Passy-Muir®-Sprechventil, Blom® Tracheostomy Tube System) über Dysphagiediagnostik (apparativ, klinisch) und die Entscheidung zur Oralisierung bis hin zur Erleichterung bzw. Ermöglichung von Kommunikation.
Fazit für die Praxis
Alle Patienten mit geblockter TK haben ein hohes Risiko für eine Schluckstörung mit meist stiller Aspiration, da sich aufgrund des fehlenden Luftstroms Schluck- und Hustenreflex durch mangelnde Stimulation von Chemo- und Druckrezeptoren der Kehlkopfschleimhaut abschwächen 17. Entscheidend für die Wiedererlangung der Sensibilität in Larynx und Pharynx sowie einer ausreichend hohen Spontanschluckrate ist daher ein Luftstromstimulus. Auch bei stiller Aspiration und vermindertem Hustenstoß sollte daher die TK (wenn zunächst auch nur kurz) entblockt werden, da eine spontane Rückbildung der Sensibilitätsstörung bei dauergeblockter TK nicht zu erwarten ist 18. Selbstverständlich darf dabei nicht leichtsinnig vorgegangen werden; mögliche negative Konsequenzen bei einem zu raschen Trachealkanülenmanagement (z. B. eine Pneumonie) sind jedoch unter engmaschigem Monitoring und multiprofessioneller Teamarbeit vermeidbar.
Die Autorin:
Dr. phil. Maria-Dorothea Heidler
Brandenburgklinik
Neurologisches Rehabilitationszentrum
(NRZ-N1)
Johann-Strauß-Str. 4, 16321 Bernau
heidler@brandenburgklinik.de
Begutachteter Beitrag/reviewed paper
Heidler M.-D. Dysphagie bei außerklinischen Intensivpatienten. Orthopädie Technik, 2017; 68 (8): 41–45
- Vergleichende Prüfung konventioneller und additiv gefertigter Prothesenschäfte in Anlehnung an DIN EN ISO 10328:2016 — 10. März 2026
- Easypreg – ein Faserverbundwerkstoff zum Tiefziehen — 9. März 2026
- Konservative Versorgung einer adulten Skoliose mit einem modularen Bausatz – ein Versorgungsbeispiel — 6. März 2026
- Heidler MD, Bidu L. Therapie bei beatmeten Patienten. Was müssen Sprachtherapeuten wissen und können? Forum Logopädie, 2015; 1 (29): 18–23
- Seidl RO, Nusser-Müller-Busch R, Ernst A. The influence of tracheotomy tubes on the swallowing frequency in neurogenic dysphagia. Otolaryngology – Head and Neck Surgery, 2005; 132: 484–486
- De Larminant V, Montravers P, Dureil B, et al. Alteration in swallowing reflex after extubation in intensive care patients. Critical Care Medicine, 1995; 23 (3): 486–490
- Heidler MD. Rehabilitation schwerer pharyngo-laryngotrachealer Sensibilitätsstörungen bei neurologischen Patienten mit geblockter Trachealkanüle. Neurologie & Rehabilitation, 2007; 13 (1): 3–14
- Seidl RO, Nusser-Müller-Busch R, Ernst A. The influence of tracheotomy tubes on the swallowing frequency in neurogenic dysphagia. Otolaryngology – Head and Neck Surgery, 2005; 132: 484–486
- Eibling DE, Gross RD. Subglottic air pressure: a key component of swallowing efficiency. The Annals of Otology, Rhinology, and Laryngology, 1996; 105 (4): 253–258
- Suiter DM, McCullough GH, Powell PW. Effects of cuff deflation and one-way tracheostomy speaking valve placement on swallow physiology. Dysphagia, 2003; 18: 284– 292
- Schröter-Morasch H. Klinische Untersuchung des Oropharynx und videoendoskopische Untersuchung der Schluckfunktion. In: Bartholome G, Schröter-Morasch H (Hrsg.). Schluckstörungen – Diagnostik und Rehabilitation. München: Elsevier, 2006: 173–208
- Hannig C. Radiologische Funktionsdiagnostik des Pharynx und des Ösophagus. Berlin: Springer, 1995
- Neurogene Dysphagien. Leitlinie der Deutschen Gesellschaft für Neurologie und der Deutschen Gesellschaft für Neurotraumatologie und Klinische Neurorehabilitation. http://www.bundesverband-klinische-linguistik.de/pdf/LL_Dysphagie.pdf (Zugriff am 26.09.2016)
- Hess DR. Facilitating speech in the patient with a tracheostomy. Respiratory Care, 2005; 50 (4): 519–525
- Passy V, Baydur A, Prentice W, et al. Passy-Muir tracheostomy speaking valve on ventilator-dependent patients. Laryngoscope, 1993; 103 (6): 653–658
- Larsen R, Ziegenfuß T. Beatmung. Indikationen – Techniken – Krankheitsbilder. 5. Aufl. Berlin: Springer, 2013
- Heidler MD, Bidu L, Friedrich N et al. Oralisierung langzeitbeatmeter Patienten mit Trachealkanüle. Medizinische Klinik – Intensivmedizin und Notfallmedizin, 2015; 110 (1): 55–60
- Frank U. Die Behandlung tracheotomierter Patienten mit schwerer Dysphagie. Eine explorative Studie zur Evaluation eines interdisziplinären Interventionsansatzes. Potsdam: Universitätsverlag, 2008
- Winklmaier U, Wüst K, Wallner F. Evaluation des Aspirationsschutzes blockbarer Trachealkanülen. HNO, 2005; 53: 1057–1062
- Denk DM, Bigenzahn W, Komenda-Prokop E et al. Funktionelle Therapie oropharyngealer Dysphagien. In: Bigenzahn W, Denk DM (Hrsg.). Oropharyngeale Dysphagien. Ätiologie, Klinik, Diagnostik und Therapie von Schluckstörungen. Stuttgart: Thieme, 1999: 66–96
- Heidler MD. Dekanülierungsmanagement in der Frührehabilitation. Ein Plädoyer für mehr Risikobereitschaft. Forum Logopädie, 2011; 3 (25): 22–25